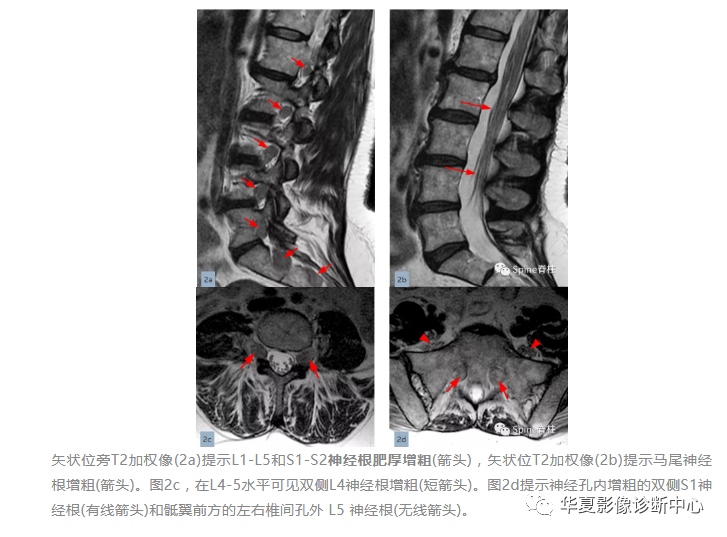
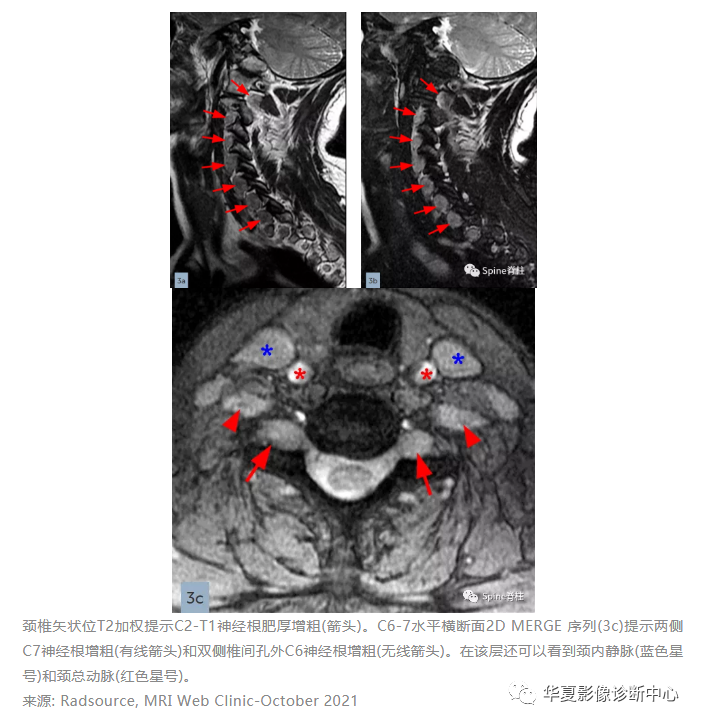
腓骨肌萎缩症(Charcot-Marie-tooth disease,CMT),又称遗传性运动感觉神经病(hereditary motor and sensory neuropathy,HMSN),是一组具有高度临床和遗传异质性的周围神经单基因遗传病。主要临床表现为进行性对称性肢体远端肌无力和肌萎缩,感觉障碍和腱反射减退或消失。
影像学特征
MRI是支持CMT临床诊断的有价值的辅助手段。神经根通常肥大增粗并伴有洋葱球征(详见上述病例),这表示肥厚性脱髓鞘。
哪些人患有CMT?
作为一组临床和遗传异质性神经病,CMT在全世界各地均有发生,总体发病率约在1/2500,但其同一致病突变在不同人群和种族中携带率不尽相同。与亚洲CMT相比,GJB1中的变异在欧洲CMT患者中的携带率更高。
CMT的会导致哪些症状出现?
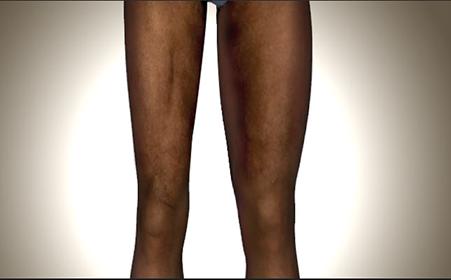
CMT多为儿童和青少年起病,典型的临床特点是双下肢最早受累,表现为远端肌肉进行性对称性肌无力,肌萎缩或肥大,腱反射减弱或消失,并伴随骨骼畸形,包括鹤腿样畸形、弓形足以及锤状趾等。患者运动能力出现严重损害,而感觉功能受累程度不一。
大多数CMT患者都有一定程度的身体残疾,但很少会影响到涉及呼吸等重要功能的肌肉,因此不会危及生命,大多数CMT患者的寿命与正常人无异。
CMT有哪些类型?
CMT有很多不同的类型,部分临床症状会因遗传方式、发病年龄以及是否涉及轴突或髓鞘而异。正是由于其临床异质性的存在,目前CMT的分类尚无专家共识。
根据发病年龄:分为婴儿早期(<2岁)、儿童(2至10岁)、青少年(10至20岁)、成人(20至50岁)和成年晚期(>50岁)。
根据电生理结果:CMT分为脱髓鞘和轴突神经病。
根据遗传方式:CMT具有常染色体显性、常染色体隐性或X连锁遗传方式。常染色体显性遗传模式是最常见的。
根据电生理学和病理学发现,以及关键的临床特征,CMT被命名为遗传性运动和感觉神经病(HMSN)并分类为:
①HMSN I:脱髓鞘亚型
②HMSN II:轴突亚型
③HMSN III:Dejerine Sottas病
④HMSN IV:Refsum病
⑤HMSN V:伴锥体束征
⑥HMSN VI:伴视神经萎缩
⑦HMSN VII:伴色素性视网膜炎
最新分类综合了分子遗传因素,主要分为以下几种:
①CMT1:由髓鞘异常引起。
其中CMT1A主要由外周髓鞘蛋白22(PMP22)基因的重复变异引起。该蛋白是髓鞘的重要组成部分,其过度表达会导致髓鞘结构和功能异常。相反,PMP22蛋白的表达不足会导致复发性脱髓鞘性神经病,称为遗传性压力易感性周围神经病(HNPP)。
CMT1B由编码髓鞘蛋白零(MPZ,也称为P0)的基因突变引起,P0蛋白是髓鞘的另一个关键成分。该基因大多数突变是点突变,迄今为止,已发现120多个不同的点突变。CMT1A和CMT1B的临床症状存在相似性。
其他不太常见的CMT1分别是由LITAF、EGR2、PMP22和NEFL基因内的突变引起的。
②CMT2:由外周神经细胞轴突异常引起,比CMT1少见。
有十几种亚型,每种亚型都与特定基因的突变有关。多在儿童期或青春期发病。临床症状与CMT1中的症状相似,但CMT2患者的残疾和感觉丧失程度通常比CMT1患者轻。某些类型的CMT2会由于声带或膈神经受累而导致言语或呼吸问题。
③CMT3或Dejerine-Sottas病:是一种特别严重的脱髓鞘性神经病,于婴儿期发病。
临床会出现严重的肌肉萎缩、身体虚弱、运动技能发育延迟和感觉问题,部分会发展为严重的残疾、感觉丧失和脊柱弯曲。由多个基因的突变引起,包括PMP22、MPZ和EGR2,同时存在显性遗传和隐性遗传模式。
④CMT4:包括脱髓鞘、轴突和运动神经病变的几个不同亚型,属于常染色体隐性遗传疾病。
每种亚型由不同基因的突变引起,特殊之处在于,该分型的不同突变可能会影响特定的种族人群,并产生不同的生理或临床特征。患有CMT4的人通常会在儿童时期出现腿部无力的症状,青春期发展为无法行走。
⑤CMTX1:是第二种最常见的CMT分型。
这种X连锁疾病是由GJB1基因突变引起的,GJB1编码连接蛋白32。该蛋白存在于髓鞘雪旺氏细胞中,包裹神经轴突并构成髓鞘。男性在儿童晚期或青春期开始表现出中度至重度的疾病症状;女性通常会出现比男性更轻微的症状或无症状表现。
什么原因导致了腓骨肌萎缩?
神经细胞通过向细胞中细长的轴突部分发送电信号来向远处的目标传递信息。髓鞘是轴突外部的包围层,其作用类似于电线上的绝缘层,有助于电信号的高速传输。如果轴突和髓鞘发生损坏,沿着神经和轴突的信号要么传送缓慢,要么信号微弱,继而导致周围神经细胞无法激活肌肉或将来自四肢的感觉信息传递回脊髓和大脑。
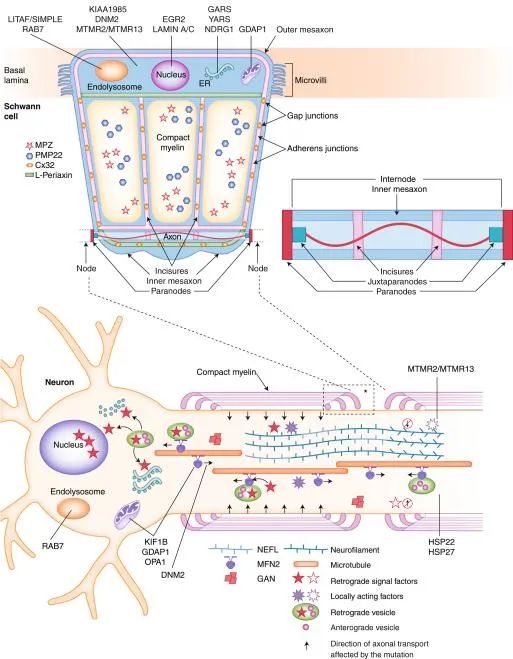
CMT胞内途径可能涉及到的蛋白质
CMT属于遗传疾病,其致病基因编码与周围神经轴突或髓鞘结构功能相关的蛋白质。在CMT中已经确定了80多个基因,每个基因都与一种或多种疾病相关,多个基因也可以与一种类型的CMT相关联。
临床最常见的为PMP22基因重复所致的CMT1A亚型,约占40%~50%,该基因位于17p12,易发生基因组重排。GJB1基因点突变所致的CMTX型约占10%,MZP基因突变所致的CMT1B型占2.5%~5%。
如何诊断CMT?
在临床诊疗工作中,对于临床表现不典型,无阳性家族史者,应尽早行神经电生理检查,做到早诊断,早治疗。神经电生理检查是诊断、疾病的疗效及预后判断有很好的指导作用。基因诊断是该基因可靠、准确的诊断方法,在发达国家,基因诊断正逐步成为确诊CMT的主要依据,如果条件许可,应尽早行基因检测,尤其是对有家族史的患者,进行家族系基因检测尤为重要,但仍有部分患者的致病基因目前尚不明确。
康旭的腓骨肌萎缩症产品,针对周围神经病相关基因的外显子区域进行二代测序,以协助临床进行此类疾病的鉴别诊断;还包括常见致病基因的拷贝数变异检测,作为二代测序产品的补充;另外提供相关产品的产前筛查。
|
产品编码 |
产品名称 |
检测内容 |
|
LM-NE0801 |
周围神经病及痉挛性截瘫检测包 |
相关基因外显子的二代测序+PMP22基因MLPA检测 |
|
LP-NE1202 |
腓骨肌萎缩症大片段变异检测-1 |
IGHMBP2基因MLPA检测 |
|
LP-NE1204 |
腓骨肌萎缩症大片段变异检测-2 |
GDAP1、MTMR2、SBF2、SH2TC2、EGR2、PRX基因MLPA检测 |
|
LP-NE1206 |
腓骨肌萎缩症大片段变异检测-3 |
PMP22基因MLPA检测 |
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#神经根#
92
#萎缩#
46
#肌肉萎缩#
93