肝内胆管癌靶向治疗首次重大突破!Pemigatinib横空出世
2020-03-05 国际肝胆资讯 国际肝胆资讯
复旦大学附属中山医院副院长周俭教授:“肝内胆管癌发病率约占原发性肝脏恶性肿瘤的15~20%,且呈上升趋势。大部分肝内胆管癌病人初次就诊时常伴有局部侵犯或远处转移而失去手术根治机会。以吉西他滨联合铂类的化疗方案被推荐为治疗晚期胆管癌的一线方案,客观反应率(ORR)为15~26%,且常发生耐药。目前,临床上缺乏其他有效的治疗药物和方案。” FGFR靶向药物的横空出世解决了胆管癌患者的燃眉之急,今
复旦大学附属中山医院副院长周俭教授:“肝内胆管癌发病率约占原发性肝脏恶性肿瘤的15~20%,且呈上升趋势。大部分肝内胆管癌病人初次就诊时常伴有局部侵犯或远处转移而失去手术根治机会。以吉西他滨联合铂类的化疗方案被推荐为治疗晚期胆管癌的一线方案,客观反应率(ORR)为15~26%,且常发生耐药。目前,临床上缺乏其他有效的治疗药物和方案。”
FGFR靶向药物的横空出世解决了胆管癌患者的燃眉之急,今天我们给大家分享治疗胆管癌的首个靶向新药——Pemigatinib。该药是针对FGFR亚型1/2/3的强效选择性口服抑制剂,二线治疗胆管癌患者的有效率ORR达35.5%,疾病控制率DCR为82%,即将于5月底于美国上市,成为胆管癌历史上第一个靶向药物!具有划时代的意义!
Pemigatinib:二线治疗FGFR2融合/重排的胆管癌患者,DCR为82%
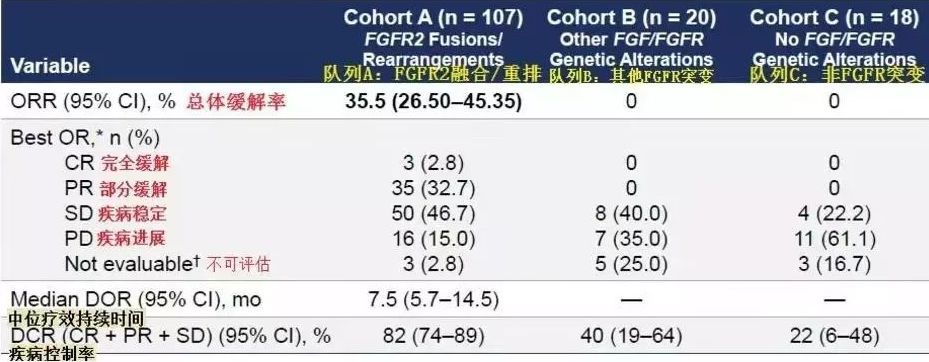
Pemigatinib二线治疗晚期胆管癌患者的FIGHT202研究更新数据显示,该研究共纳入146例经过≥1线治疗的晚期胆管癌患者,分为3个队列:A是FGFR2融合/重排(n=107),B是其他FGFR突变(n=20),C是非FGFR突变(n=18),1名患者未定。所有患者均接受Pemigatinib治疗(13.5mg qd 用2周歇1周)。
结果显示,A组ORR为35.5%,其中3例患者完全缓解(CR),CR率为2.8%,DCR为82%。B组和C组的ORR为0%。相比其他两个队列,队列A的患者对药物有效响应的比例大很多,有效时间也长得多。
A组的DOR中位数为7.5个月, PFS和OS中位数分别为6.9和21.1个月。相比其他两个队列,生存期得到大幅度延长,意味着的患者用Pemigatinib治疗效果非常不错。
中国首例胆管癌患者完成pemigatinib给药
基于上述试验结果,2019年11月,美国FDA正式受理pemigatinib用于治疗复发的FGFR2基因融合或重排的局部晚期胆管癌的NDA,并授予其优先审评资格。根据美国处方药使用者费用法案(PDUFA),预计pemigatinib在美国获批的日期为2020年5月30日。之前信达生物与pemigatinib的研发药厂Incyte达成战略合作,拥有pemigatinib在中国大陆、中国香港、中国澳门和中国台湾地区的开发和商业化权利。
今天信达生物宣布中国第一例患者已完成pemigatinib首次给药,本研究结果将用于pemigatinib在中国的新药上市申请(NDA),这是pemigatinib进入中国市场重要的里程碑事件,希望这样的好药可以早日国内上市,惠及更过胆管癌患者。
FGF/FGFR通路的异常激活可以使肿瘤细胞以“自给自足”的方式维持生长,所以FGFRs成为肿瘤治疗的新靶点。临床数据显示,胆道癌中有13%~20%的患者携带FGFR2融合。今天我们除了分享FGFR新药Pemigatinib之外,还给大家分享其他3款FGFR靶点的靶向药物。
Infigratinib:针对FGFR2融合/易位的患者,DCR为83.6%
Infigratinib(BGJ398)是一种口服给药的选择性FGFR-TKI(酪氨酸激酶抑制剂)。既往的一项研究纳入71名患有FGFR2融合/易位的患者,其中62%为女性患者,38%为男性患者。患者每日口服125mg的infigratinib,口服21天,28天为一周期。
总体患者人群中,18例(25.4%)的患者部分缓解PR,41例(57.7%)的患者疾病稳定SD。确认的ORR(客观缓解率)为26.9%,DCR(疾病控制率)为83.6%,中位DoR(缓解持续时间)为5.4个月,中位PFS(无进展生存期)为6.8个月,中位OS(总生存期)为12.5个月。

BLU-554:针对FGFR4作用靶点,DCR为68%
BLU-554作用靶点是FGFR4(与FGF19配对),是一种FGFR4的强效、选择性小分子抑制剂,由基石药业合作伙伴Blueprint Medicines研发。
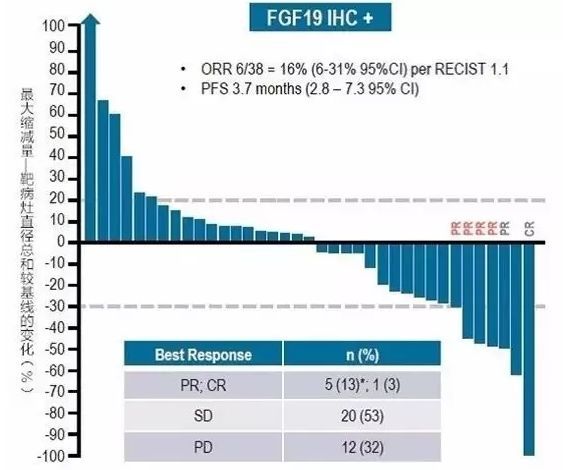
I期研究共纳入了77例患者按照RECISIST1.1(研究者评定的疗效)接受疗效评估。在38例FGF19免疫组化阳性(IHC+)患者中,确认的ORR为16%,包括1例CR,DCR为68%。18例(49%)患者肿瘤负荷减小。38例FGF19 IHC+患者的最大肿瘤减小(根据靶病灶缩减衡量)见图。基于77例患者的药物安全性分析显示:大多数不良事件(AE)为1或2级,副作用可控。
目前,BLU-554已经在中国开展了2期临床试验。
TAS-120:针对FGFR靶向耐药的患者
TAS-120为高选择性不可逆的泛FGFR抑制剂。在1期试验中,该药治疗28例FGFR2融合胆管癌患者的ORR为25%,DCR达到79%。其中4例患者对infigratinib或者其他FGFR2 抑制剂耐药,接受TAS-102治疗后,2例患者产生了部分反应,另外2例患者病情稳定,持续了5到17个月。我们期待更加成熟的数据。
基于此,FDA授予TAS-120孤儿药称号。目前该药正进行胆管癌及子宫内膜癌的剂量扩增试验。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#PE#
149
#肝内胆管癌#
152
#pemigatinib#
135
#IgA#
0
#胆管#
143
FGF新靶
184
666
184