PNAS:癌中之王的“阿喀琉斯之踵”——VISTA
2019-01-28 moon 转化医学网
虽然目前的免疫检查点抑制剂疗法对胰腺癌基本上无效,但美国科学家现在已经确定了一种免疫检查点分子,它可以代表这种肿瘤类型的有希望的免疫治疗靶点。德克萨斯大学MD安德森癌症中心领导的研究小组发现,与黑色素瘤相比,T细胞活化的V结构域免疫球蛋白抑制剂(VISTA)优先在胰腺癌中高水平表达。研究人员的研究还提供了与黑色素瘤相比较的原发性和转移性胰腺癌免疫浸润的详细分析,这可能进一步有助于指导针对胰腺癌治疗
它发病率不高、却有着极高的死亡率;
它5年生存率低于7%;
它夺走了歌王帕瓦罗蒂的生命;
它被人们称为“癌中之王”;
它——就是胰腺癌。
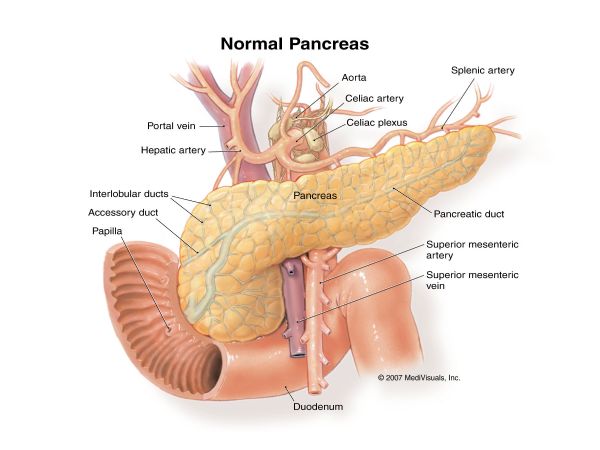
癌中之王的“阿喀琉斯之踵”
胰腺癌的治疗手段比较多样,有外科手术、化疗、放疗、介入治疗等,但治疗方法多样的背后,也残酷地说明了单一治疗方法疗效不佳。手术是至今唯一有可能治愈胰腺癌的方法,但很多患者在确诊时已经失去了根治性手术的机会。但是,癌中之王也有“阿喀琉斯之踵”。
2019年1月10日,德克萨斯大学MD安德森癌症中心在PNAS期刊上发表论文“Comparison of immune infiltrates in melanoma and pancreatic cancer highlights VISTA as a potential target in pancreatic cancer”,称“VISTA可能是有效治疗胰腺癌患者的相关免疫治疗靶点。”
虽然目前的免疫检查点抑制剂疗法对胰腺癌基本上无效,但美国科学家现在已经确定了一种免疫检查点分子,它可以代表这种肿瘤类型的有希望的免疫治疗靶点。德克萨斯大学MD安德森癌症中心领导的研究小组发现,与黑色素瘤相比,T细胞活化的V结构域免疫球蛋白抑制剂(VISTA)优先在胰腺癌中高水平表达。研究人员的研究还提供了与黑色素瘤相比较的原发性和转移性胰腺癌免疫浸润的详细分析,这可能进一步有助于指导针对胰腺癌治疗的免疫治疗策略。
近年来,免疫检查点治疗(ICT)改变了癌症治疗的面貌,但并非所有肿瘤类型都对现有的免疫检查点抑制剂反应良好。尽管黑色素瘤对免疫检查点抑制剂(如抗-CTLA-4和抗-PD-1抗体)表现出较好的临床反应,但临床研究表明,现有的ICT对胰腺癌的临床益处极小。
肿瘤免疫微环境在决定对ICT的反应中发挥着关键作用,因此更好地了解免疫渗透如何区别于ICT敏感(如黑色素瘤)和ICT抗性肿瘤类型(如胰腺肿瘤),可能对制定有效的治疗方法有所帮助。研究人员写道:“我们对这些结构不同的肿瘤类型中免疫浸润的分布没有清楚的认识,解剖这些差异可能有助于开发新的有效的胰腺癌治疗策略。” “肿瘤内免疫细胞与PDAC (胰腺导管腺癌) TME (肿瘤微环境)基质区域的差异分布可能对免疫检查点治疗的反应产生影响。”
为了更深入地了解胰腺肿瘤的免疫结构,研究小组比较了胰腺癌的免疫浸润。他们还比较了原发性未治疗和原发性新辅助治疗的PDAC和转移性PDAC的免疫浸润。
研究分析了肿瘤微环境(TME)免疫浸润局部化的位置。 “我们分析了TME中免疫浸润的微定位,以确定免疫细胞是否与肿瘤细胞或肿瘤内部紧密接触,或者位于肿瘤的基质成分中。”
该团队首先分析了23个未经治疗的手术切除的胰腺肿瘤中9种已经识别的免疫抑制基因的表达。结果表明,患者可分为两组,其中11例T细胞共抑制基因高表达,12例低表达。抑制性免疫检查点基因的表达与存活率呈负相关,因此具有低表达T细胞共抑制基因的肿瘤患者的中位生存期为37个月,而肿瘤高表达的患者仅为20个月。

(T细胞共抑制基因的表达与胰腺癌的总体存活相关)
胰腺肿瘤的特征在于高密度的基质和非恶性支持细胞,而黑素瘤具有最小的基质。该团队的分析发现,虽然胰腺肿瘤包含30%的恶性细胞和70%的基质,但黑色素瘤包括70%的肿瘤和30%的基质。当他们将免疫浸润与未经治疗的转移性黑色素瘤和未治疗的PDAC进行比较时,他们发现,正如预期的那样,黑色素瘤的CD3,CD4和CD8 T细胞,记忆T细胞,B细胞和调节性T细胞的密度高于胰腺肿瘤。
大约三分之一的胰腺肿瘤确实显示T细胞穿透率大致等于黑素瘤中发现的T细胞穿透率。然而,在这些胰腺肿瘤中,T细胞主要集中在基质中,而不是在肿瘤细胞区域内,而在黑素瘤肿瘤中它们均匀地分布在恶性细胞和基质之间。
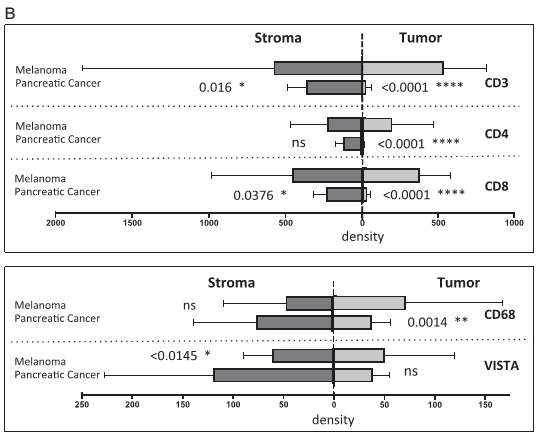
(与黑素瘤相比,人胰腺癌中的免疫浸润主要位于TME的基质成分中;T细胞主要存在于PDAC的基质组分中,对PDAC的肿瘤组分的渗透最小)
对29个未治疗的胰腺癌肿瘤和44个未治疗的黑素瘤的分析还发现,黑色素瘤表现出更高水平的表达抑制性检查点分子PD-1及其活化配体PD-L1的细胞,这是目前CTI治疗的目标。
更详细的评估显示,与胰腺肿瘤相比,黑色素瘤TME的肿瘤组分中表达CD68的巨噬细胞密度更高。尽管VISTA主要在巨噬细胞上表达,但作者指出,“尽管CD68 +巨噬细胞密度较低,但PDAC的VISTA表达密度明显较高,这凸显了VISTA作为潜在的免疫治疗靶点。”
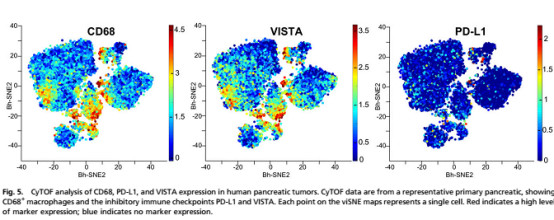
(红色表示高水平的标记表达;蓝色表示没有标记表达)
对手术前预处理的三种类型的胰腺肿瘤未治疗的原发性,治疗的转移性和原发性肿瘤进行单独比较,发现T细胞在转移性肿瘤中渗透性低,未治疗的原发性和转移性肿瘤中VISTA水平较高。
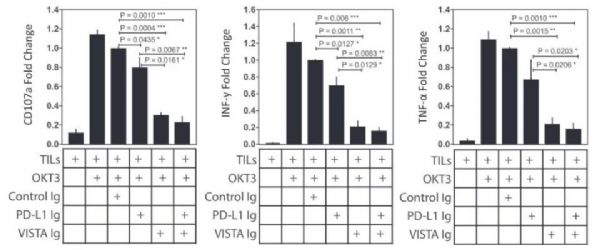
(VISTA的参与抑制TIL产生细胞因子)
对7个胰腺肿瘤样本的另一项分析发现,CD68阳性巨噬细胞具有不同的PD-L1和VISTA途径,分别起到抑制免疫应答的作用。对来自三名转移性胰腺癌患者的肿瘤的T细胞的研究表明,活性VISTA途径使肿瘤中的活性T细胞应答比PD-L1抑制更大程度地降低。这表明用PD-1 / PD-L1抑制治疗可能失败,因为未治疗的VISTA途径仍然抑制免疫应答。相反,阻断VISTA但不阻断PD-L1,抑制肿瘤浸润性T细胞产生细胞因子。 “因此,抗VISTA抗体可能是胰腺癌患者的有效免疫治疗策略,”他们总结道。
原始出处:Jorge Blando, Anu Sharma, Maria Gisela Higa, et al. Comparison of immune infiltrates in melanoma and pancreatic cancer highlights VISTA as a potential target in pancreatic cancer. PNAS. January 11, 2019
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#VISTA#
0
#PNAS#
69
阿喀琉斯?
95