Nat BME:基于Cas13的SARS-CoV-2RNA检测方法的临床验证
2020-08-26 MedSci原创 MedSci原创
由SARS-CoV-2病毒的传播引起的COVID-19大流行需要快速、敏感和廉价的诊断方法来促进疾病的控制。实时定量PCR和逆转录(RT-qPCR)测量病毒RNA的数量,仍然是SARS-CoV-2病毒
由SARS-CoV-2病毒的传播引起的COVID-19大流行需要快速、敏感和廉价的诊断方法来促进疾病的控制。实时定量PCR和逆转录(RT-qPCR)测量病毒RNA的数量,仍然是SARS-CoV-2病毒检测的金标准技术。但是,无法获得足够的RT-qPCR仪器,试剂和训练有素的仪器操作员,可能会限制该诊断工具的实用性,尤其是在资源有限的发展中国家。在实验室进行RT-qPCR后续确认之前,对COVID-19进行即时快速检测,作为初步筛选,将大大提高诊断能力,从而改善检疫和护理程序,最终有助于减少对医疗资源的压力。此外,还需要具有快速周转时间的COVID-19的精确即时检验平台,以恢复社会和经济活动。在当前的COVID-19暴发期间,作者报告了基于CRISPR–Cas13的两步法SHERLOCK系统对SARS-CoV-2病毒RNA的敏感和特异性检测的临床验证。
方法:SERSLOCK系统对SARS-CoV-2的检测依靠RT–RPA等温扩增感兴趣的病毒基因片段,然后进行CRISPR–Cas介导的扩增基因检测(在这种情况下,使用来自瓦德勒氏菌的Cas13a(LwaCas13a))。 CRISPR-Cas对扩增的基因序列的检测触发了分子的旁裂,用于荧光或侧流测量。作者首先设计并测试了总共四对RPA引物对和相应的CRISPR RNA(crRNA),它们针对SARS-CoV-2的尖峰(S),核蛋白(N)和复制酶多蛋白1ab(Orf1ab)基因。 S和Orf1ab基因的两个引物对(和crRNA)先前已通过合成RNA进行过验证。设计靶向N基因和Orf1ab另一个区域的其他两个引物对和crRNA,以匹配医院用于SARS-CoV-2检测的标准RT-qPCR分析中使用的基因区域。所有RPA引物和crRNA序列均被设计成对SARS-CoV-2病毒RNA具有特异性和选择性的引物和序列。
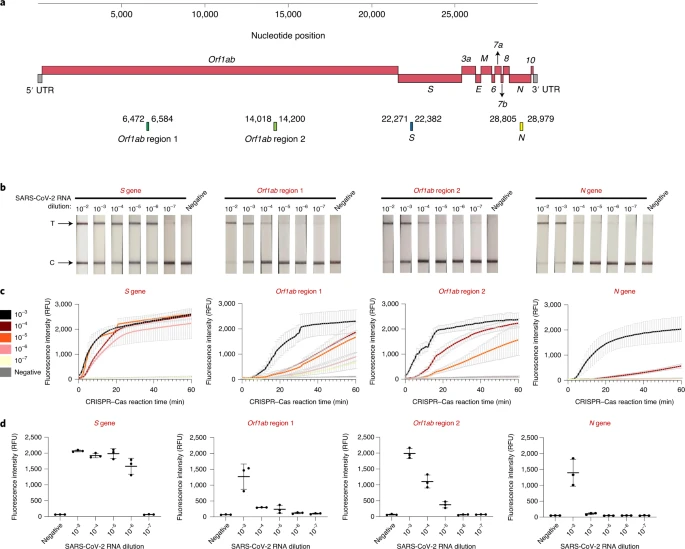
结果:作者对SARS-CoV-2检测的SHERLOCK方法(一种基于CRISPR-Cas的检测平台)的性能进行了严格评估。验证了总共154个临床COVID-19样品的SHERLOCK方法,发现它对荧光读数具有100%的特异性和96%的敏感性,对侧流读数具有88%的敏感性。该方法能够检测鼻咽和咽拭子样品(包括痰样品)的RNA提取物中的SARS-CoV-2,而与其他普通人类冠状病毒无交叉反应,并且能够在无症状情况下检测该病毒。SHERLOCK 方法对SARS-CoV-2检测的当前LoD和灵敏度与批准的即时医疗点基因诊断测试的性能相当 ,但不需要特定的工具。这有可能将SHERLOCK的实用性从即时检验扩展到在家测试,在执行安全的样本收集程序之前,可以更频繁,更便宜地执行该测试。
原文链接:Patchsung, M., Jantarug, K., Pattama, A. et al. Clinical validation of a Cas13-based assay for the detection of SARS-CoV-2 RNA. Nat Biomed Eng (2020). https://doi.org/10.1038/s41551-020-00603-x
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Cas13#
85
#SARS-CoV#
66
学习了!非常感谢!
141
#Nat#
72
学习
133
#Cas#
58
#检测方法#
86
#SARS#
54
学习了
117
好资料
0