Nat Commun:石莉红/竺晓凡合作团队解析先天性非溶血性贫血发病新机制
2024-07-14 iNature iNature 发表于上海
该研究在患病谱系中发现toll样受体8(TLR8)的功能获得性突变与遗传性非溶血性贫血有关。
遗传性非溶血性贫血是一组以红细胞缺陷为特征的罕见骨髓疾病。尽管已经探索了这些疾病的潜在发病机制,但仍未能完全理解致病突变过程。
2024年7月6日,中国医学科学院血液病医院(中国医学科学院血液学研究所)石莉红/竺晓凡合作团队在Nature Communications 在线发表题为“Erythroid-intrinsic activation of TLR8 impairs erythropoiesis in inherited anemia”的研究论文,该研究在患病谱系中发现toll样受体8(TLR8)的功能获得性突变与遗传性非溶血性贫血有关。TLR8在红系谱系中表达,且抑制红细胞生成,而在红系祖细胞阶段抑制TLR8能够促进红细胞生成。
从机制上讲,TLR8激活阻断了膜联蛋白A2(ANXA2)介导的STAT5质膜定位,并破坏了HuDEP2细胞中的EPO信号传导。TLR8抑制改善了来自健康供体和遗传性非溶血性贫血患者的RPS19+/- HuDEP2细胞和CD34细胞的红细胞生成。总得来说,该研究发现了一个与遗传性贫血相关的基因,以及TLR8在红细胞生成中的作用,为遗传性贫血的治疗方案研究奠定了基础。

贫血是儿童中最常见的血液学异常,可分为遗传性贫血和获得性贫血。遗传性贫血进一步细分为遗传性溶血性贫血和遗传性非溶血性贫血。红细胞缺陷(如膜或血红蛋白(Hb)紊乱和代谢异常),是遗传性溶血性贫血的主要原因,如遗传性球形红细胞增多症、β-地中海贫血和丙酮酸激酶缺乏症等疾病。而遗传性非溶血性贫血,如Diamond-Blackfan贫血、先天性铁粒幼细胞性贫血和先天性红细胞生成不良性贫血,可导致多种病因的骨髓红细胞增殖不足或无效红细胞生成。
编码核糖体蛋白的基因(如RPS19和RPL5)或参与核糖体生物合成的基因(如TSR2)的特定突变导致的Diamond-Blackfan贫血,是遗传性非溶血性贫血的最常见形式之一。先天性红细胞生成不良性贫血的特征是红细胞生成效率较低,主要由CDAN1、C15orf41、SEC23B、KIF1等基因突变引起,这些基因属于先天性贫血的异质性组,由于红细胞分化和增殖的干扰产生。此外,据报道,GATA1、EPO、TP53和ADA2等其他基因的突变也与遗传性非溶血性贫血有关。尽管如此,部分遗传性贫血患者的致病基因仍然是个谜。揭示这种遗传性贫血的发病机制可以更深入地了解疾病的发生机制及潜在的临床治疗方法。
红细胞生成是一个紧密协调的过程,主要包括两个阶段。初始阶段始于多能造血干细胞和祖细胞(HSPC),它们分化为红系定向祖细胞,称为爆发形成单位红细胞(BFU-E)和集落形成单位红细胞(CFU-E)。而后一阶段涉及红系前体细胞最终分化为去核网织红细胞,最终在循环中成熟为红细胞。细胞因子促红细胞生成素(EPO)是调节红细胞生成的主要因子之一。EPO和EPO受体(EPOR)之间的相互作用诱导EPOR的二聚化,随后激活Janus激酶/信号转导和转录激活因子(JAK/STAT)信号通路。尽管已经对EPO信号通路进行了充分研究,但尚未彻底阐明EPO信号通路的新介质。寻找干扰EPO信号传导的新调节因子对于解释红细胞生成的控制至关重要,也能够提供潜在的治疗靶点,增强贫血在各种情况下的临床治疗效果。
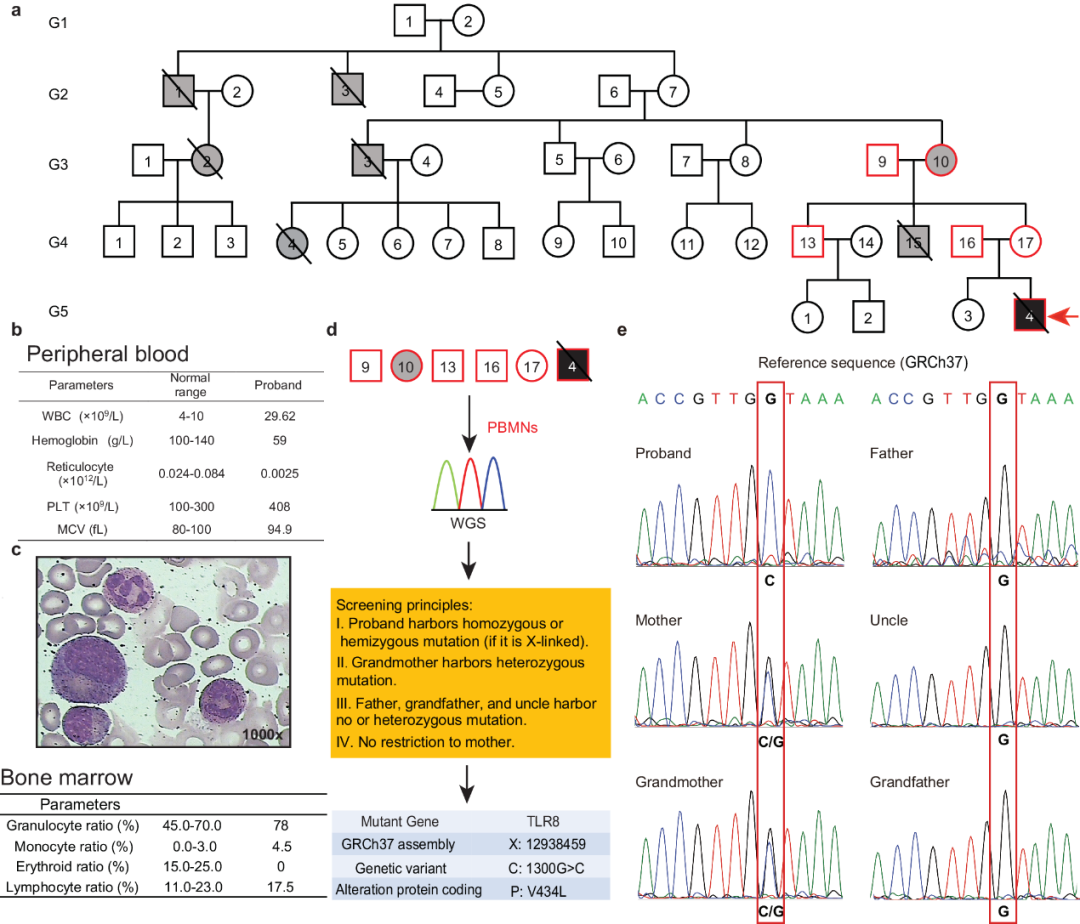
在出现遗传性非溶血性贫血的家族谱系中发现了TLR8V434L突变(摘自Nature Communications )
近期研究表明,HSPCs表达调节造血所必需的免疫信号传导的组成部分。就红细胞生成而言,成熟的红细胞表达toll样受体9,该受体在激活后促进红细胞吞噬和巨噬细胞清除。成红细胞表达S100a8,在RPS14单倍体功能不全的情况下抑制红细胞生成。因此,极易推测出红细胞能够表达调节红细胞生成的其他免疫因子。
TLR8是一种先天免疫受体感应单链RNA(ssRNA),主要由髓系细胞表达。通过分析一个患有遗传性非溶血性贫血的家族谱系,作者确发现TLR8中有一个功能获得性(GOF)突变,该突变损害了红细胞生成。进一步的研究表明,TLR8在BFU-E阶段的红系谱系中表达,红系TLR8的激活通过干扰红系祖细胞的分化、增殖和存活而损害红细胞生成。机理研究揭示了TLR8在ANXA2介导的质膜定位和STAT5激活中的作用,最终干扰EPO信号传导。抑制TLR8改善了健康供体和遗传性非溶血性贫血患者RPS19+/- HuDEP2细胞和CD34细胞的红细胞生成。总得来说,该研究发现了一种新的遗传性贫血致病基因,并为遗传性非溶血性贫血的发病机制和调节红细胞生成的网络提供了新见解。更重要的是,结果表明TLR8可能是治疗病理性红细胞生成的新靶点。
中国医学科学院血液病医院(中国医学科学院血液学研究所)石莉红研究员和竺晓凡主任医师为共同通讯作者,博士后梁静、万扬副主任医师、高洁主管技师和硕士研究生郑凌岳为共同第一作者。该项目获得国家重点研发计划、国家自然科学基金、中国医学科学院医学与健康科技创新工程和细胞生态海河实验室创新基金等的支持。中国医学科学院血液病医院(中国医学科学院血液学研究所)朱平研究员、清华大学尹航教授和南开大学陈果教授提供了重要支持与帮助。
参考消息:
https://www.nature.com/articles/s41467-024-50066-w
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#TLR8# #toll样受体8# #非溶血性贫血#
14