两款国产疫苗同时获批上市,老年人群将全面覆盖
2021-02-26 JACKZHAO MedSci原创
国家药品监督管理局附条件批准国药集团中国生物武汉生物制品研究所有限责任公司的新型冠状病毒灭活疫苗(Vero细胞)注册申请与准康希诺生物股份公司重组新型冠状病毒疫苗,这也意味着老年人群亦将得到全面覆盖。

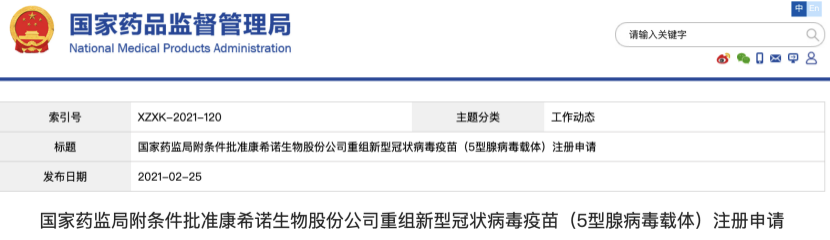
2月25日,国家药监局网站消息,国家药品监督管理局附条件批准国药集团中国生物武汉生物制品研究所有限责任公司的新型冠状病毒灭活疫苗(Vero细胞)注册申请与准康希诺生物股份公司重组新型冠状病毒疫苗(5型腺病毒载体)的注册申请,值得一提的是该疫苗也是首家获批的国产腺病毒载体新冠病毒疫苗。这两款疫苗均适用于预防由新型冠状病毒感染引起的疾病(COVID-19)。
国家药监局根据《疫苗管理法》《药品管理法》相关规定,按照药品特别审批程序,进行应急审评审批,附条件批准上市注册申请。国家药监局要求该疫苗上市许可持有人继续开展相关研究工作,完成附条件的要求,及时提交后续研究结果。

国药集团中国生物武汉生物制品研究所网站
2月21日,国药集团中国生物武汉生物制品研究所已正式向国家药监局提交附条件上市申请,并获得受理,从递交上市申请到正式获批仅用时4天。
国药集团中国生物武汉生物制品研究所2月24日发布的新冠灭活疫苗Ⅲ期临床试验期中分析数据显示,该疫苗接种后安全性良好,两针免疫程序接种后,疫苗接种者均产生高滴度抗体,中和抗体阳转率为99.06%,疫苗针对由新冠病毒感染引起的疾病(COVID-19)的保护效力为72.51%。
康希诺生物的重组新型冠状病毒疫苗(5型腺病毒载体)(商品名为“克威莎™”)是与军事科学院军事医学研究院生物工程研究所共同开发的。其已经在巴基斯坦、墨西哥、俄罗斯、智利、阿根廷5个国家开展了全球多中心Ⅲ期临床研究,已完成4万余受试者的接种及期中数据分析。
康希诺生物公告显示,经统计分析,重组新型冠状病毒疫苗(5型腺病毒载体)Ⅲ期临床试验期中分析数据结果显示:在单针接种疫苗28天后,疫苗对所有症状的总体保护效力为65.28%;在单针接种疫苗14天后,疫苗对所有症状总体保护效力为68.83%。疫苗对重症的保护效力分别为:单针接种疫苗28天后为90.07%;单针接种疫苗14天后为95.47%。此次只需单针接种的康希诺疫苗获批上市,适种对象为18岁以上人群,这也意味着老年人群亦将得到全面覆盖。
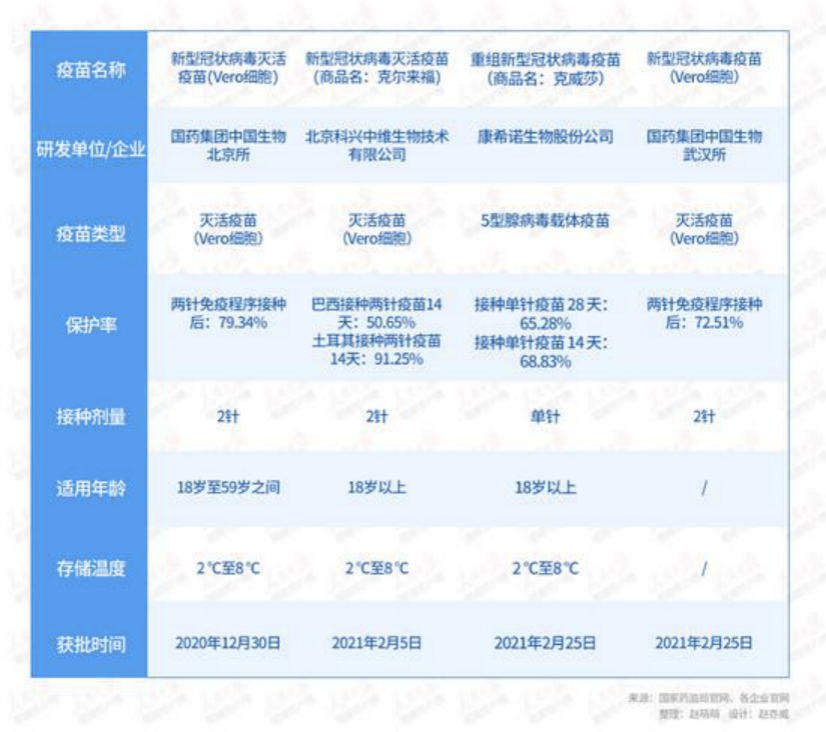
四款国产疫苗概况,健康时报整理
2020年12月30日,国家药监局附条件批准国药集团中国生物北京生物制品研究所有限责任公司的新冠病毒灭活疫苗(Vero细胞)注册申请。该疫苗也成为首家获批的国产新冠病毒灭活疫苗。
2021年2月5日,北京科兴中维生物技术有限公司新冠病毒灭活疫苗(商品名:克尔来福®)获得附条件批准上市。
加上2月25日刚刚批准的两款疫苗,至此我国已有四款上市的国产新冠疫苗。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#获批上市#
101
#国产疫苗#
0
#老年人群#
70
棒棒
128
好文章!
122