肺癌,哪些病理类型提示险恶?
2022-08-10 e药安全 e药安全
按照最新版国内外指南,对于IB期术后存在高危险因素的患者,推荐进行多学科综合评估,结合评估结果和患者意愿后可以考虑术后辅助化疗。
肺友交流群(协作病理解读)
NSCLC患者即使接受了肿瘤完全切除术,仍存在术后复发、转移的风险。超过50%的肿瘤复发或转移发生于术后前2年,但术后3~5年复发和转移风险仍偏高,直到术后5年后肿瘤复发和转移风险才显著降低,分期越晚,复发转移风险更高[1]。因此需要在术后进行药物或其他形式的治疗,以进一步提高长期生存,这些术后的治疗手段统称为辅助治疗。
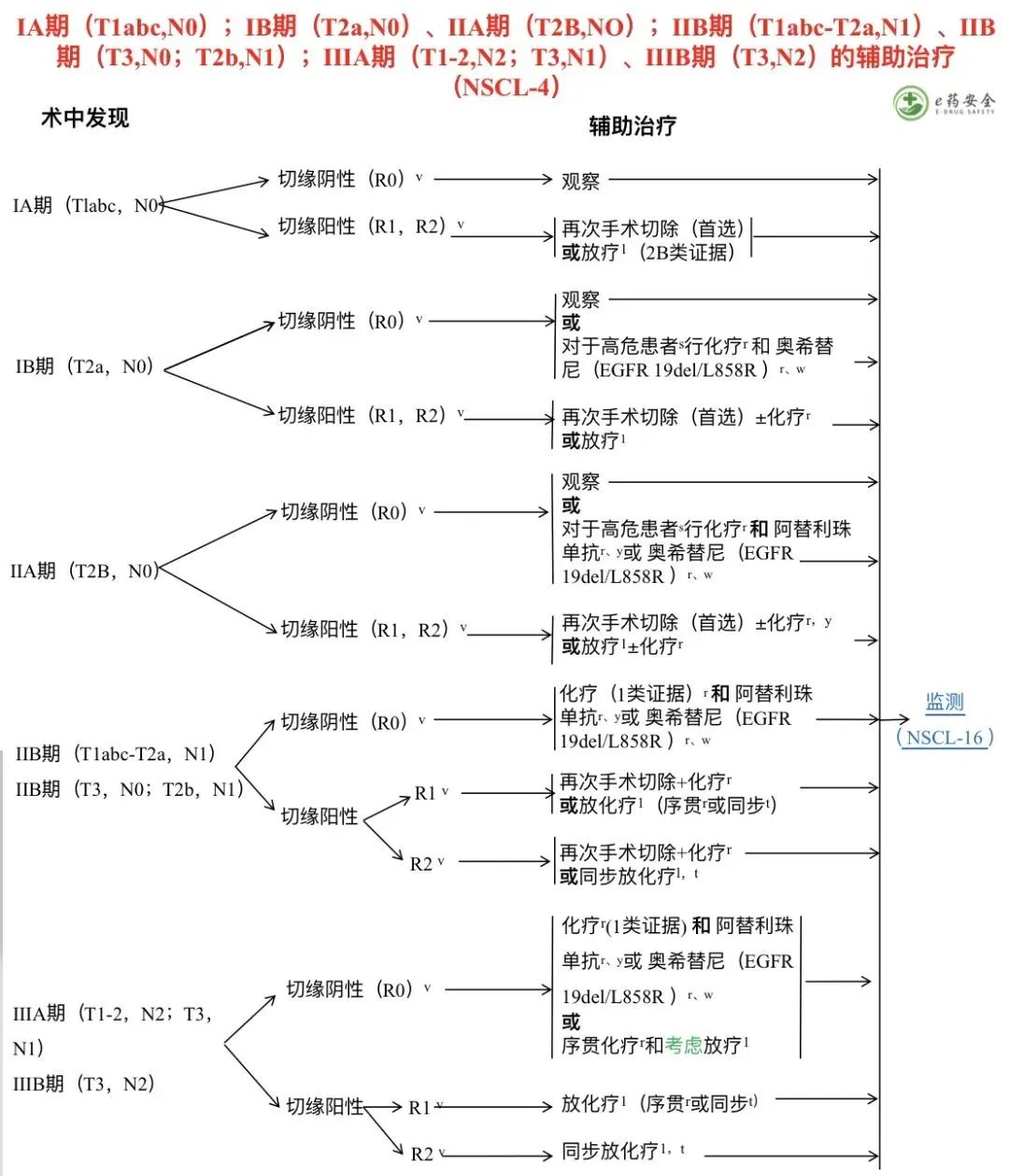
目前,国内外指南对于IA期患者均不推荐进行术后辅助治疗。对于IB期是否进行辅助化疗,各临床研究结果不一致,目前仍存在争议,各指南推荐也存在差异(见下图)。
《NCCN非小细胞肺癌指南2022.V3版》推荐对高危患者进行辅助化疗;
《I~IIIB期非小细胞肺癌完全切除术后辅助治疗指南2021版》[1]推荐对于其中存在高危因素的患者,推荐进行多学科综合评估,结合评估意见以及患者意愿,可考虑术后辅助化疗(1类证据,推荐)。
《CSCO非小细胞肺癌指南2022版》:IB期非小细胞肺癌(包括有高危因素的肺癌),由于缺乏高级别证据的支持,一般不推荐辅助化疗;
因此对于IB期术后存在高危险因素的患者,推荐进行多学科综合评估,结合评估结果和患者意愿后可以考虑术后辅助化疗。

CSCO指南
NCCN指南
NCCN指南列举了6大高危因素,低分化肿瘤(包括肺神经内分泌肿瘤[ 不包括分化良好的神经内分泌肿瘤])、血管浸润、楔形切除、肿瘤 >4 cm、脏层胸膜受累和淋巴结状态不明(Nx)。除此之外,临床上还发现一些与预后不良的新高危因素,如实体/微乳头型腺癌、气道内播散、脉管内癌栓等。今天,我们对新高危因素与不良预后之间联系进行分享。
NCCN丨非小细胞肺癌临床实践指南2022.3版①,②
CSCO丨非小细胞肺癌诊疗指南(2022)
I-IIIB期非小细胞肺癌完全切除术后辅助治疗指南(2021版)
病理亚型(实体/微乳头)
肺癌术后病理提示有微乳头成分,预后更不好?
WHO将浸润性肺腺癌按照生长方式分为5型:附壁型(A)、腺泡型(B)、乳头型(C)、微乳头型(E)、实体型(D)[每2个高倍镜视野至少有5个癌细胞胞浆内有粘液];腺癌的变异型:浸润性粘液腺癌、胶样型、胎儿型、肠型腺癌。
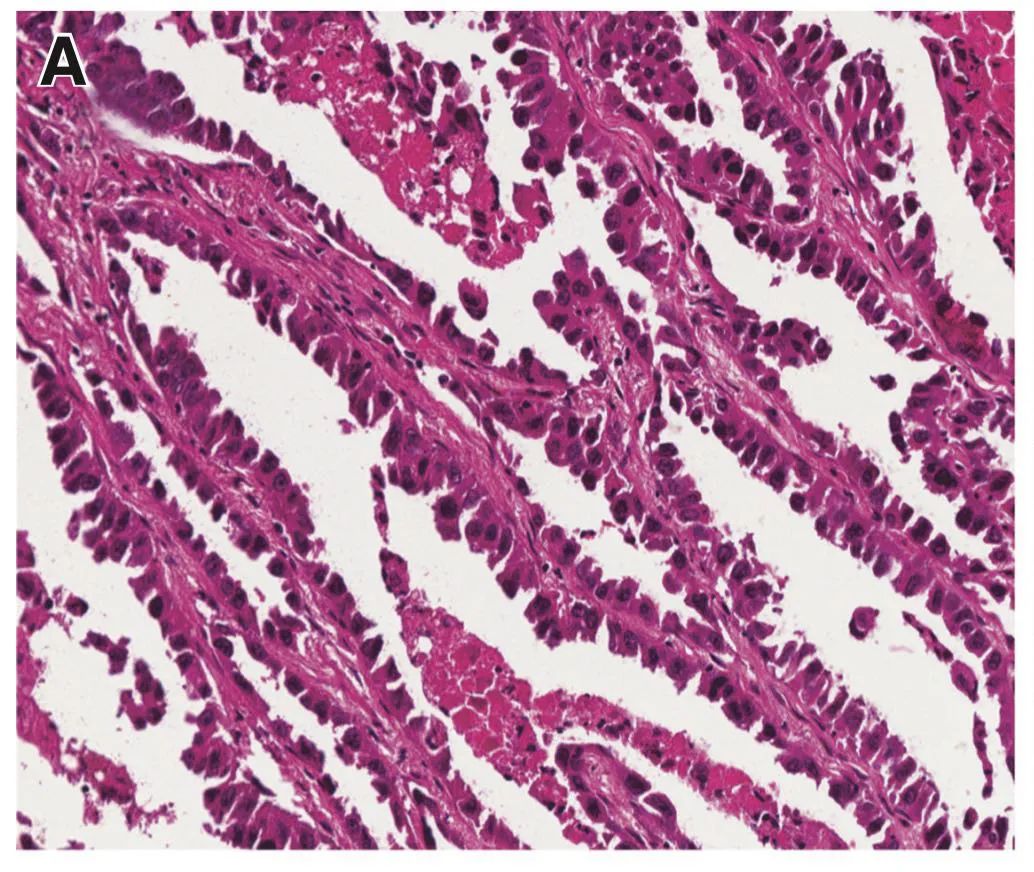
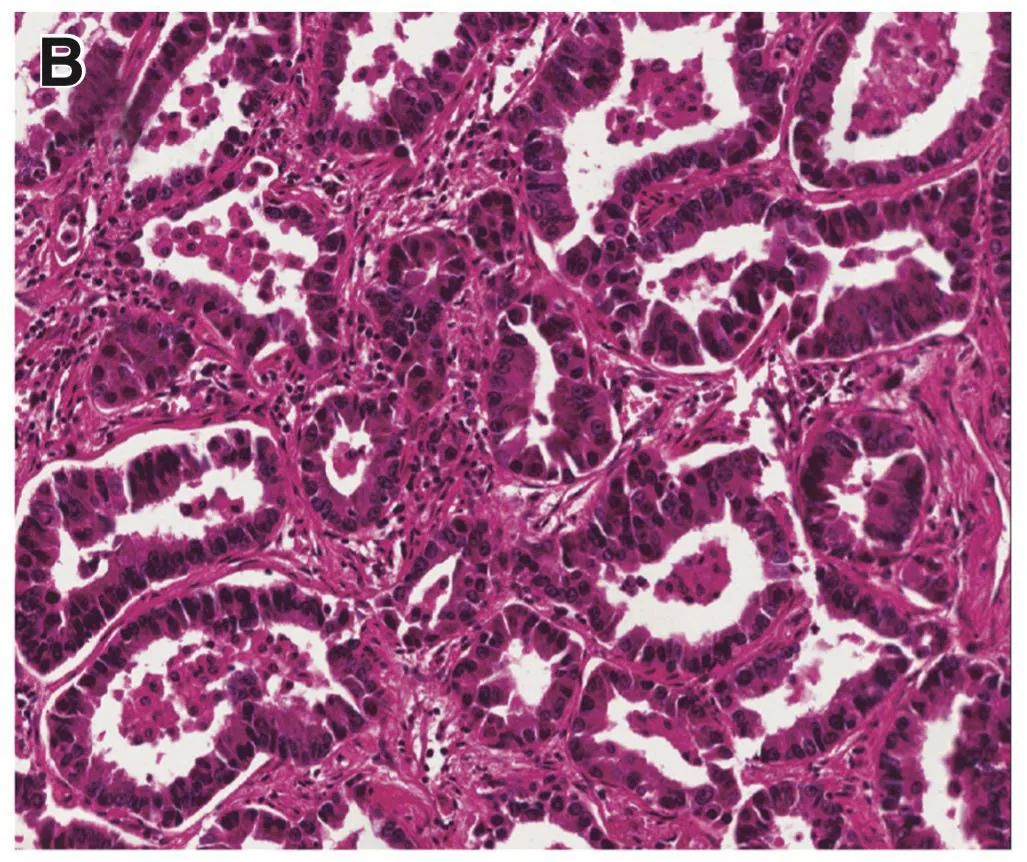
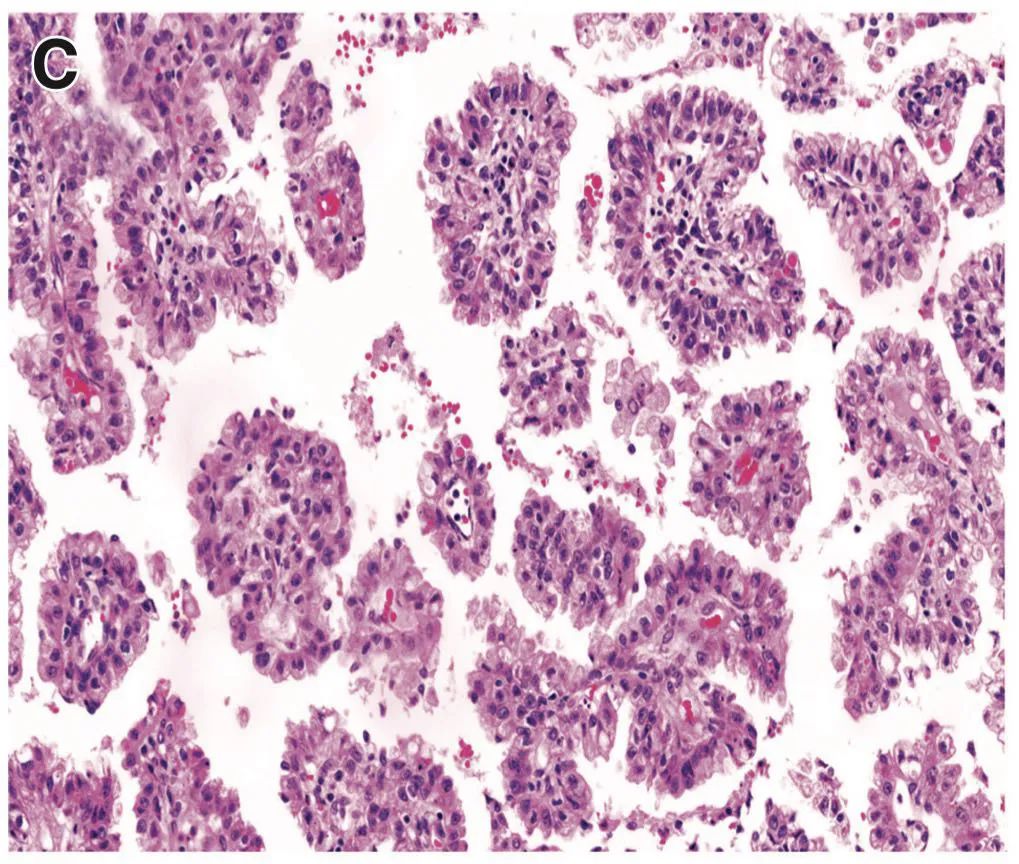
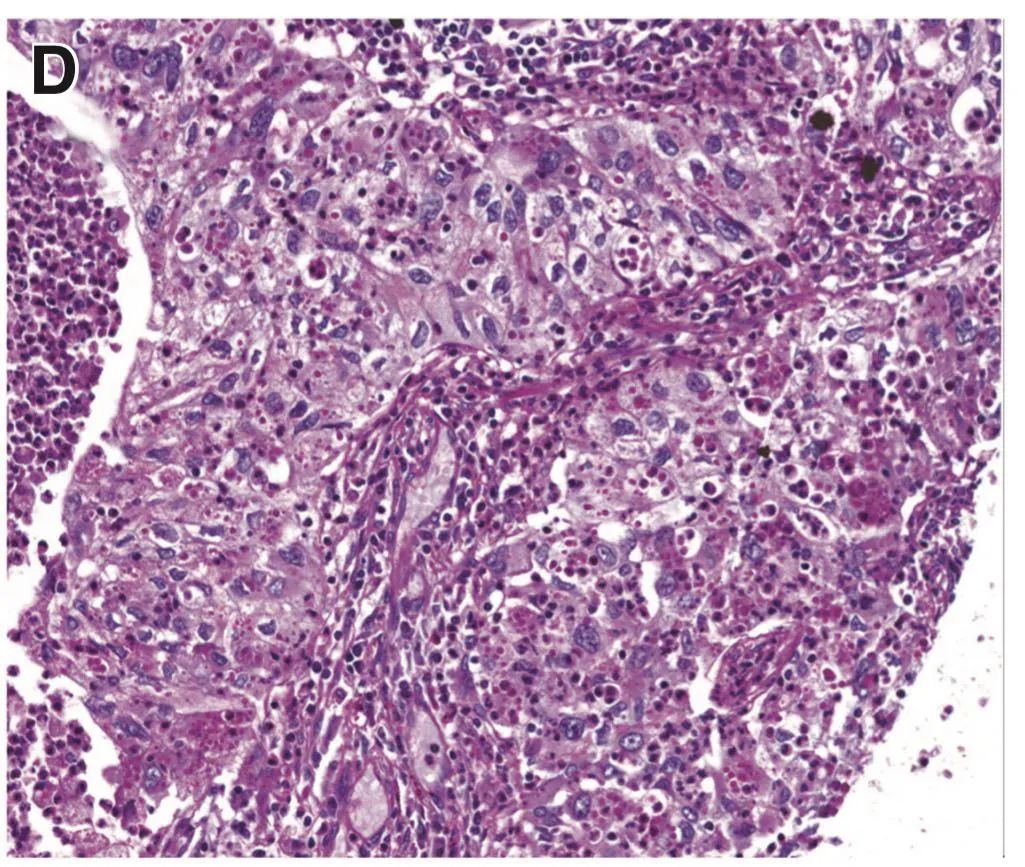
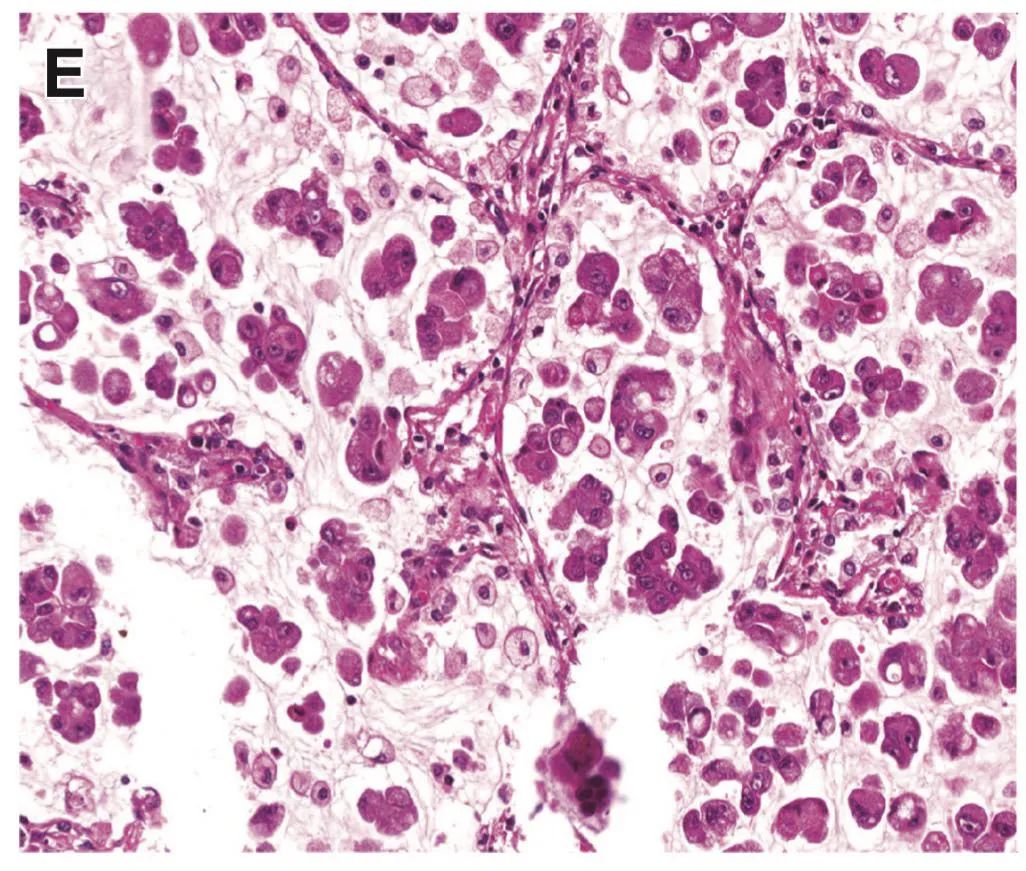
2012年《JCO》发表了肺腺癌病理亚型对预后的影响[2],研究对487名I-IV期肺浸润性腺癌患者进行了回顾性研究,所有患者均接受了手术治疗。结果表明, 乳头、微乳头和实体型患者预后较差,中位OS分别仅有48.9个月、44.9个月和58.1个月,远远差于腺泡和附壁型患者的67.3个月和78.5个月,随后有大量的研究证实,含有实体和微乳头的患者,即使其比例在5%左右,也足以对患者的预后造成影响。
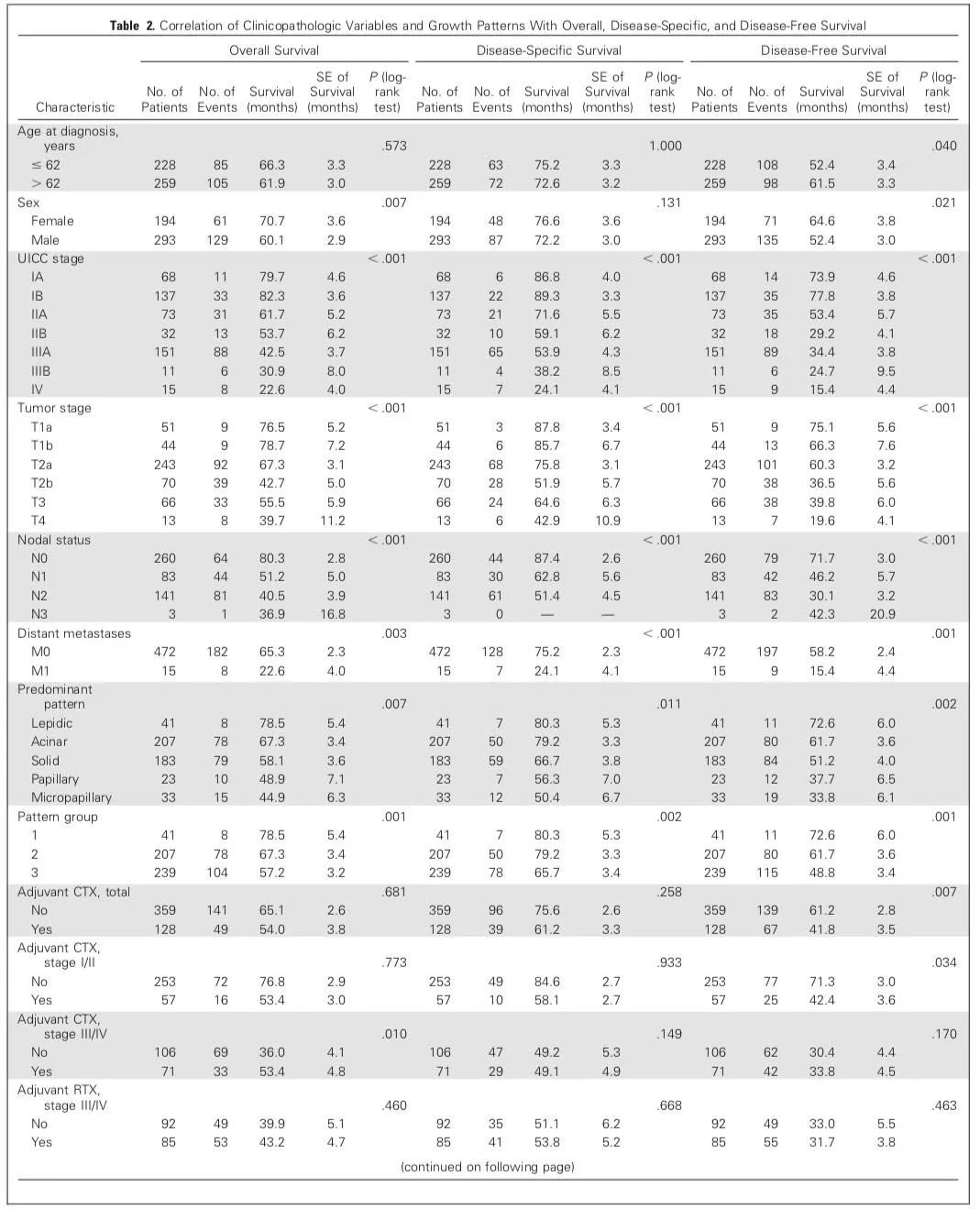
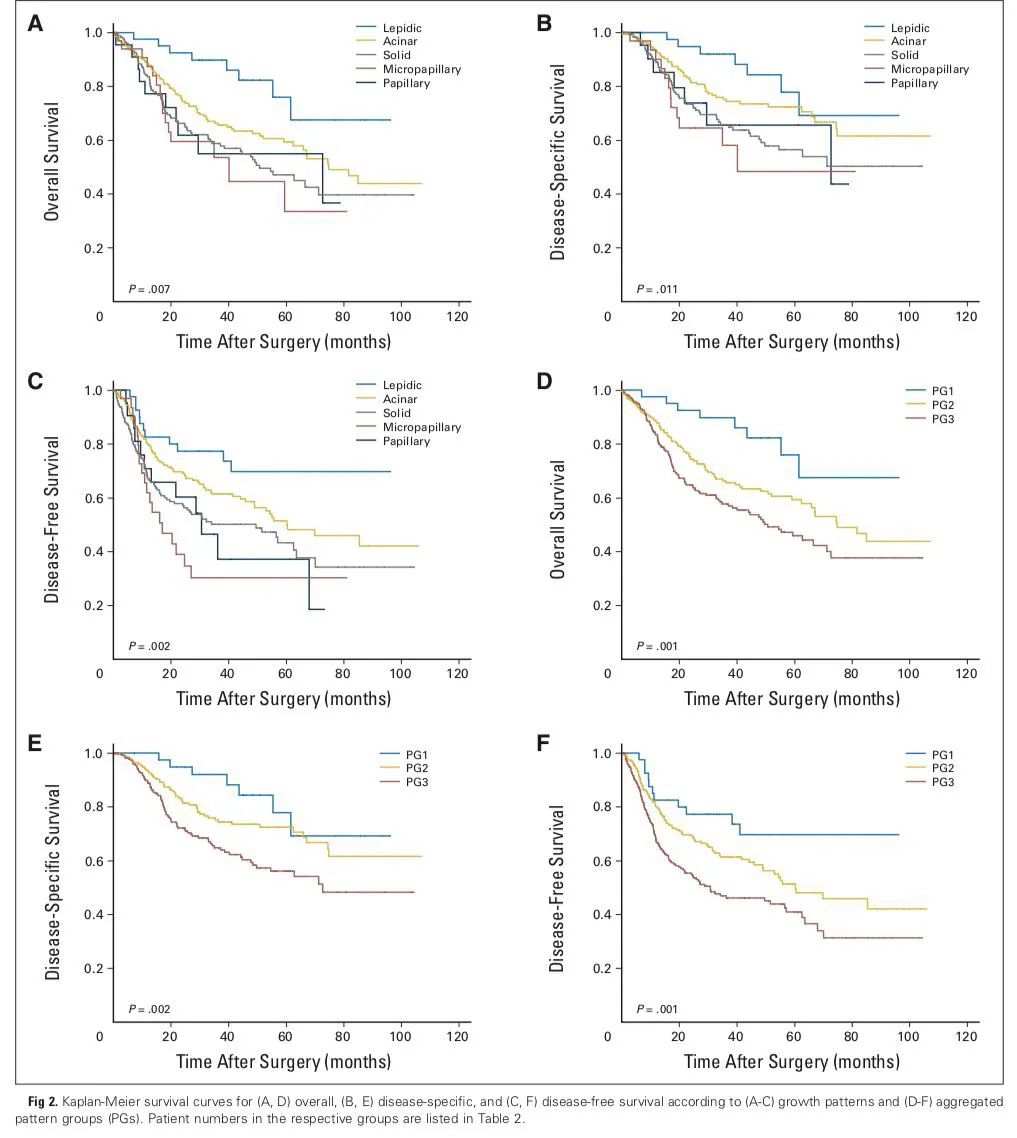
OS、DFS、DSS
备注:PG1,附壁为主型腺癌;PG2,腺泡为主型;PG3,乳头、微乳头、实体为主型
2021年韩国学者在《Thoracic Cancer》发表的研究表明[3]:在存在“最小量(≤5%)”的S/MP 亚型的肺腺癌IA期患者中,即使是完全切除后,也可能会发生侵袭性临床病理特征和不良预后结果。因此,S/MP亚型是术后预后不良的重要风险因素之一;在进行术后辅助化疗时,需要考虑该风险因素。
研究共纳入了506名I、II和IIIA期的肺浸润性腺癌患者的病历和病理报告进行了回顾性研究,所有患者均接受了根治性手术治疗。结果表明,S/MP 亚型存在于 48.8% (247/506) 的患者中。总体而言,9.9% (50/506) 的患者以 S 亚型为主,0.2% (1/506) 的患者以 MP 亚型为主,25.5% (129/506) 的患者肿瘤中 S/MP 的比例在 5% 以下。
分析显示,S/MP 亚型的存在与年龄、男性和吸烟等因素显著相关。具有S/MP亚型组(S/MP+)患者的肿瘤大小(2.5 [1.0-10.0] cm)显著大于没有 S/MP (S/MP-)亚型的患者组(1.8 [0.6-9.0] cm)。
同时,S/MP+ 组患者淋巴结转移的频率更高(28.3% vs 4.6%),胸膜(44.5% vs 21.6%)、淋巴管(25.9% vs 5.8%)和血管(12.6% vs 2.3%)浸润也更频繁。
两组患者的 CT 特征表明,纯磨玻璃结节和部分实性结节在 S/MP- 组中的发现率在更高,而实性结节是 S/MP+ 组的发现率更高。在部分实性结节中, S/MP 亚型的存在与结节中的高实性成分显著相关,因此这些结果表明,CT 中的实性成分是术前预测 S/MP 亚型的重要放射学因素。
中位随访时间32.8(3.5-74.4)个月。总体而言,S/MP+组的FFR(未复发持续时间)和 DSS (疾病特异性生存期)均显著低于 S/MP-组(图2a);在亚组分析中,S/MP+组每个分期FFR均显著低于S/MP-组(图2b)。值得注意的是, 与肿瘤大小相比(I期),S/MP亚型的存在可能是更强的预后因素(图2d)。
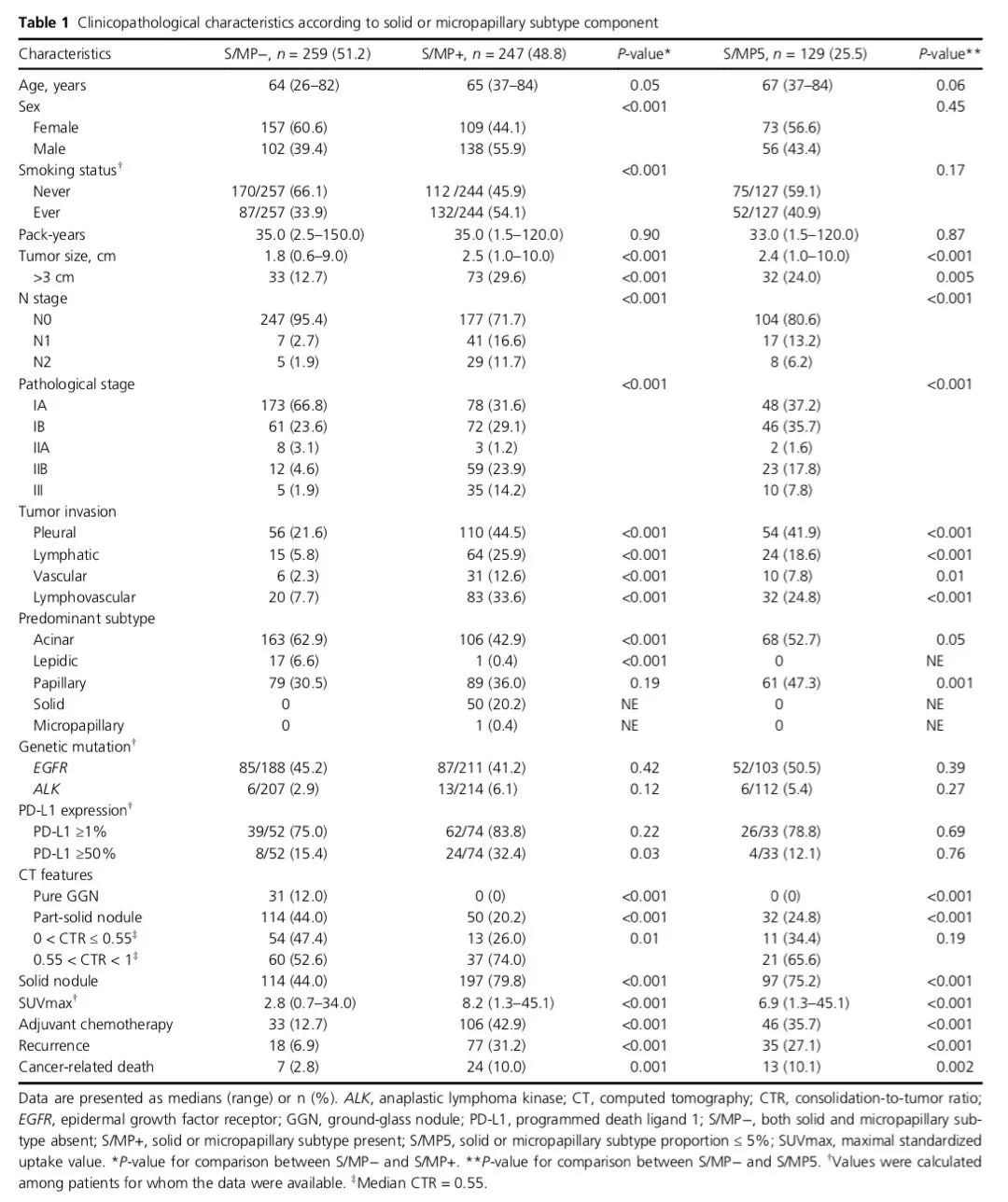
图1:S/MP亚型临床病理特征
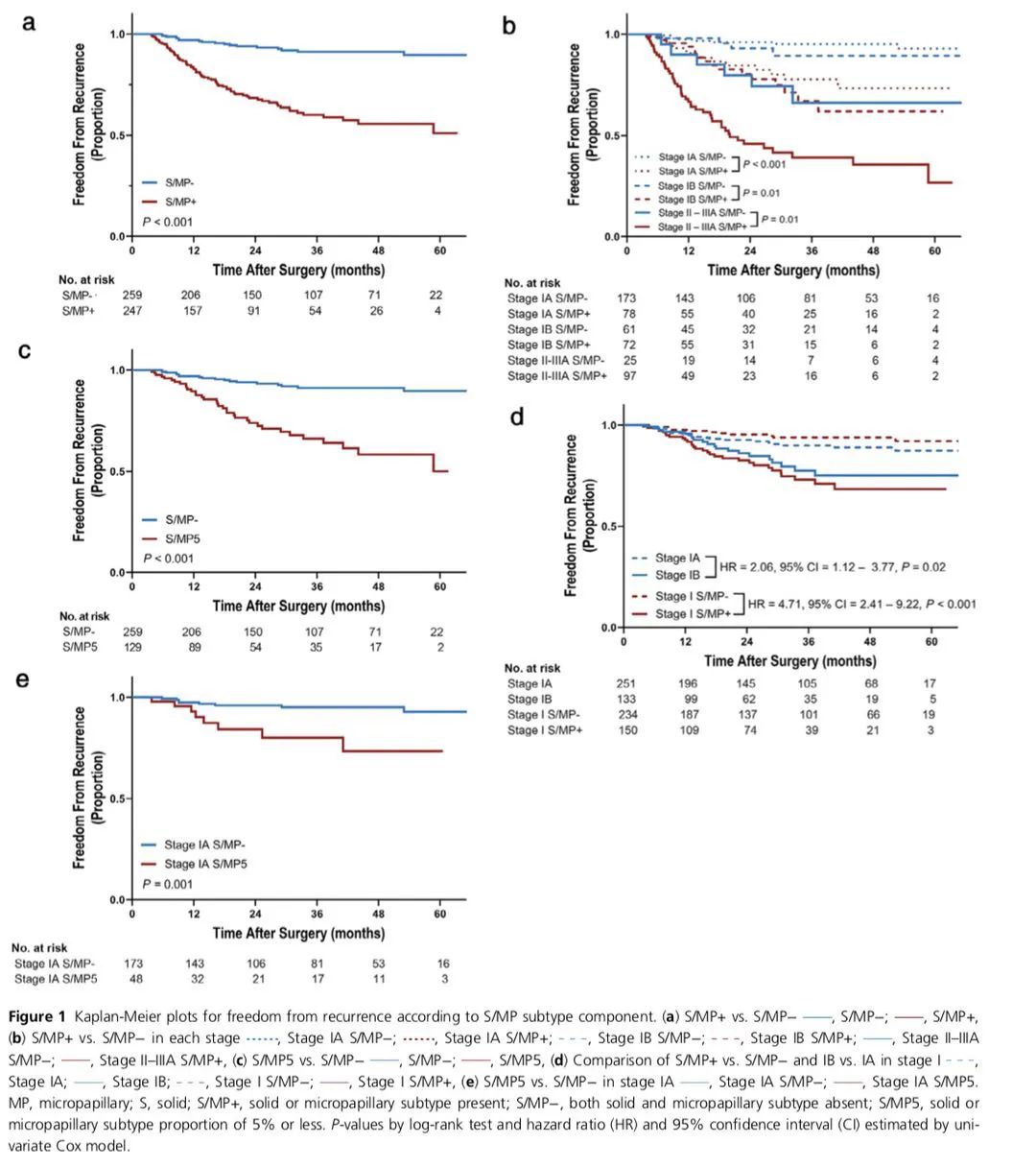
图2:FFS
备注:MP, micropapillary,微乳头型;S, solid,实体型;S/MP5, 实体/微乳头亚型占比≤5%
气道播散(STAS)
早期肺癌术后病理提示有气道播散,更易发生转移?
2018年《JTO》发表了存在气道播散的T1期肺腺癌,肺叶切除相较亚肺叶切除预后更好[4]。研究纳入了1497例患者,其中肺叶切除970例,亚肺叶切除527例,两组患者均为T1N0M0肺腺癌,且经过倾向性匹配。使用竞争风险方法分析患者结局。在亚肺叶切除患者中评估了手术切缘距离和肿瘤直径比值对复发模式(局部复发或远处转移)的影响。5名病理学家评估了使用术中冰冻标本判定STAS的可行性(敏感性、特异性和医生间一致性)。
结果表明:倾向性匹配后(349对)的多元素分析(349对)发现,STAS阳性患者接受亚肺叶切除有更高的复发率和肺癌特异性死亡率,但这一现象不存在于STAS阴性患者中。不论切缘距离和肿瘤比值是多少,STAS阳性患者接受亚肺叶切除术后都有更高的局部复发率(切缘距离和肿瘤比值≥1和<1的5年累积复发率为16%和25%)。STAS阴性患者中,局部复发更容易出现在切缘距离和肿瘤比值<1的患者中(5年累积复发率7%)。使用术中冰冻诊断STAS的敏感性和特异性分别为71%和92%,且非常可靠和稳定。




2020年《Lung Cancer》发表了气腔内播散(STAS)在IA期部分实性肺腺癌中的预后意义[5]。研究回顾了2009年2月至2016年12月间接受根治性肺切除术的IA期部分实性腺癌患者的病历。分析STAS的临床病理特点及其对术后复发和生存的影响。在115例接受楔形切除术的IA期部分实性腺癌患者中,有20例(17.4%)存在STAS。
结果表明:多因素分析显示STAS的存在[HR(危险比),9.447;p = 0.002]和更多的侵袭性成分(HR,1.097;p = 0.034)是复发的独立危险因素。具有STAS的患者和不存在STAS的患者5年无复发率分别为62.4%和97.9%(p < 0.001),5年无病生存率分别为58.5%和97.9%(p < 0.001)。STAS的存在与年龄较大(p = 0.030)、男性(p = 0.023)、腺泡型为主的腺癌(p = 0.004)、含微乳头型(p < 0.001)、淋巴血管侵犯(p < 0.001)和侵袭性病理成分较大(p < 0.001)有关。
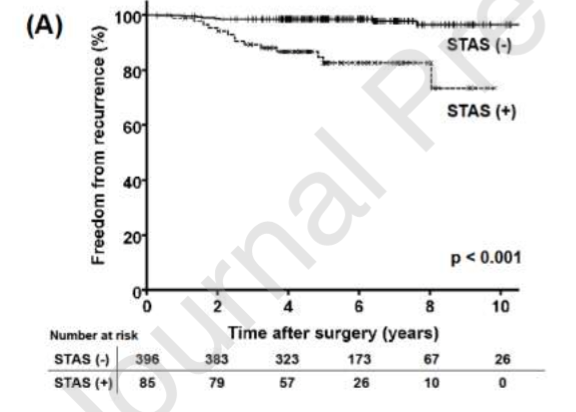
FFR
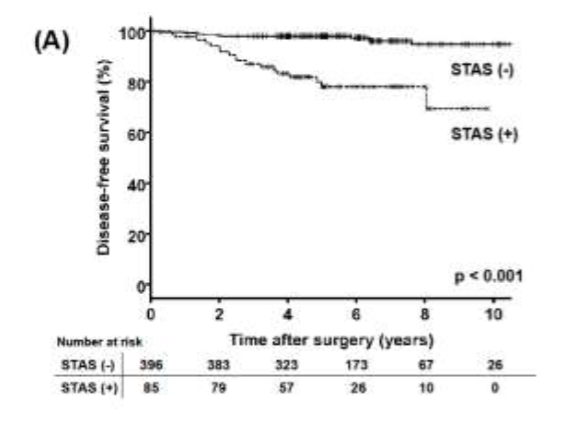
DFS
脉管内癌栓(LVI)
既往研究表明,脉管侵犯(LVI) 和胸膜侵犯 (VPI) 是 I 期非小细胞肺癌 (NSCLC) 的危险因素。然而,只有VPI被纳入当前的TNM分期。2018年上海胸科医院在《lung cancer》发表了LVI和VPI对I期肺癌患者的预后影响[6]。研究回顾性分析了2633名术后病理分期是I期的肺癌患者。222 名病理诊断为LVI,836 名病理诊断为VPI。结果表明:与没有LVI的患者相比,有LVI的患者的 5 年无复发生存率 (RFS) 和总生存率 (OS) 显著降低(61.2% 对 82.0%,p < 0.001;73.3% 对 88.1%,p < 0.001);存在VPI患者也出现了相同的结果(70.1% 对 85.9%,p < 0.001;82.3% 对 90.0%,p < 0.001)。
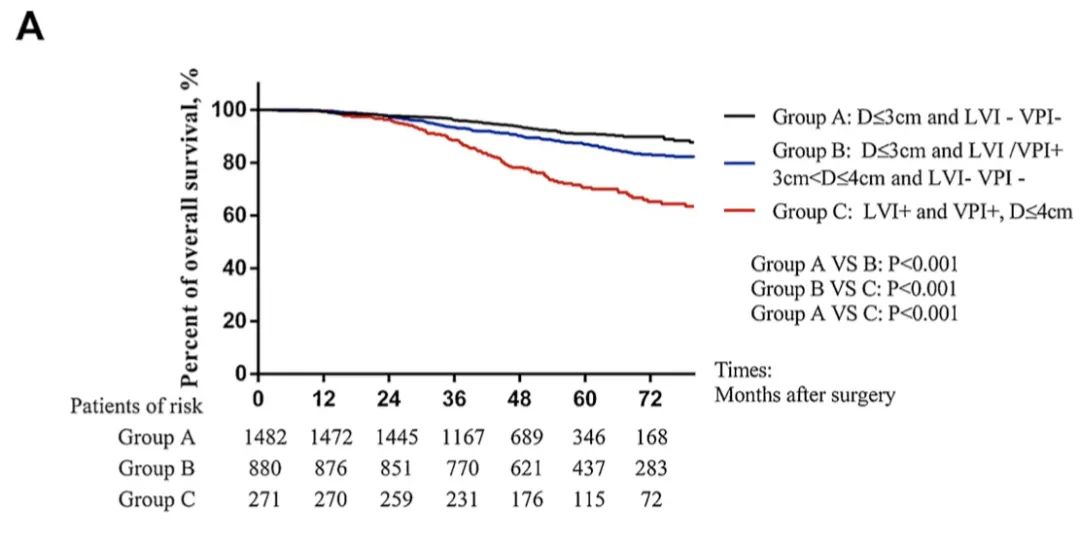
OS

RFS
小 结
按照最新版国内外指南,对于IB期术后存在高危险因素的患者,推荐进行多学科综合评估,结合评估结果和患者意愿后可以考虑术后辅助化疗。
参考文献
[1]中国抗癌协会肺癌专业委员会,中华医学会肿瘤学分会肺癌学组,中国胸部肿瘤研究协作组.Ⅰ~ⅢB期非小细胞肺癌完全切除术后辅助治疗指南(2021版)[J].中华医学杂志,2021,101(16):1132-1142.
[2]Warth A, Muley T, Meister M, et al. The novel histologic International Association for the Study of Lung Cancer/American Thoracic Society/European Respiratory Society classification system of lung adenocarcinoma is a stage-independent predictor of survival. J Clin Oncol. 2012 May 1;30(13):1438-46. doi: 10.1200/JCO.2011.37.2185.
[3]Choi SH, Jeong JY, Lee SY, et al. Clinical implication of minimal presence of solid or micropapillary subtype in early-stage lung adenocarcinoma. Thorac Cancer. 2021 Jan;12(2):235-244. doi: 10.1111/1759-7714.13754.
[4]Eguchi T, Kameda K, Lu S, et al. Lobectomy Is Associated with Better Outcomes than Sublobar ReP in Spread through Air Spaces (STAS)-Positive T1 Lung Adenocarcinoma: A Propensity Score-Matched Analysis. J Thorac Oncol. 2019 Jan;14(1):87-98. doi: 10.1016/j.jtho.2018.09.005.
[5]Chae M, Jeon JH, Chung JH, et al. Prognostic significance of tumor spread through air spaces in patients with stage IA part-solid lung adenocarcinoma after sublobar reP. Lung Cancer. 2021 Feb;152:21-26. doi: 10.1016/j.lungcan.2020.12.001.
[6]Wang S, Zhang B, Qian J, et al. Proposal on incorporating lymphovascular invasion as a T-descriptor for stage I lung cancer. Lung Cancer. 2018 Nov;125:245-252. doi: 10.1016/j.lungcan.2018.09.024.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













