全球基因治疗的临床概况
2024-10-10 小药说药 小药说药 发表于上海
本文介绍基因治疗发展历程,包括不同阶段及临床概况、地区分布等。过去十年获批产品增多,未来发展前景广阔。
前言
基因治疗的概念是在20世纪70年代初提出来的,最初的概念是引入一个正常的基因来取代一个突变基因,虽然现在有更多的替代方法,如基因编辑和碱基编辑,但它仍然是我们高度依赖的主要策略之一。
2012年欧洲批准Glybera,这是西方国家首个基因治疗产品,也是全球首个针对基因疾病的基因治疗。尽管Glylbera在商业上并不成功,但它打开了基因治疗的大门。在随后的几年里,一些基因治疗产品陆续涌入市场,Strimvelis于2016年在欧洲获得批准,CAR-T疗法(Kymriah和Yescarta)和Luxturna分别于2017年获得美国食品和药物管理局(FDA)的批准。
据弗若斯特沙利文数据显示,2015年以来,全球基因治疗行业开始高速发展。到2016年,全球和国内基因治疗市场规模分别为5,040万美元、1,500万元;2020年全球基因市场规模有所增长,达到20.8亿美元。据预计,2025年,全球市场和国内市场将分别达到近305.4亿美元和178.9亿元。基因治疗成为继小分子药物、抗体药物之后的生物医药的第三次产业革命。
基因治疗的发展阶段
基因治疗从发明到初步应用以及目前的蓬勃发展,经历了下面的四个阶段:
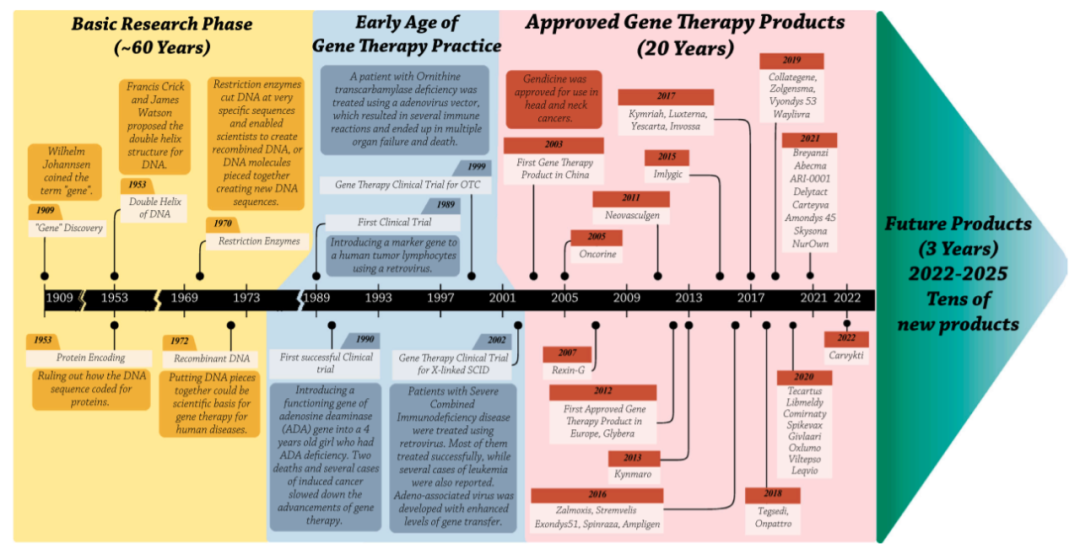
基础研究阶段(1909-1973)
最早,Wilhelm Johannsen创造了“基因”一词,然后在大约半个世纪后,Francis Crick和James Watson发现了DNA的双螺旋结构。细菌中基因转移的基本原理在20世纪60年代被发现,随后被发展为真核生物转染技术。到20世纪70年代,限制酶和连接酶的应用构成了基因操纵的基础,重组DNA技术使研究人员能够将选定的治疗基因引入工程载体。随着发现病毒转移遗传物质的能力,病毒载体已成为一种有前途的有效基因转移工具。这些技术进步使科学家能够创建将特定遗传物质转移到靶细胞中的基因治疗载体。
早期的基因治疗临床实践(1989–2003)
基因治疗的第一次临床实践开始于1989年,一种逆转录病毒被用于在肿瘤浸润淋巴细胞上表达新霉素抗性标记物,该标记物用于黑色素瘤免疫治疗中追踪浸润淋巴细胞。1990年,宾夕法尼亚大学的科学家对一名四岁的女孩Ashanti Desilva进行了第一次成功的基因治疗临床试验。她被诊断为严重联合免疫缺陷(SCID),研究人员使用逆转录病毒载体将腺苷脱氨酶(ADA)的正常拷贝转移到她的T细胞。目前她已经可以正常生活。
然而,病毒载体的使用伴随着一些不良事件,如插入突变和免疫反应,这阻碍了临床基因治疗的进展。2000年,巴黎的欧洲研究人员报告了一项X连锁SCID基因治疗的成功临床试验。然而,20名接受治疗的儿童中有5名在后期发展为白血病,这是因为在载体引入转基因后激活了一种癌基因。与此同时,1999年,Jesse Gelsinger,一名18岁的男孩,被诊断患有一种罕见的代谢性疾病,他自愿成为接受编码鸟氨酸转氨酶基因治疗的患者。然而不幸的是,其因大规模凝血障碍和随后的多器官衰竭而死亡,成为基因治疗的第一位死亡患者。尽管这些挫折减缓了基因治疗的进展,但它们也展示了基因治疗的潜力及其光明的未来。
繁荣发展阶段(2003-2022)
2003年,中国国家食品药品监督管理局(SFDA)批准了Gendicine,这是首款用于头颈部癌症的基因治疗产品。两年后,SFDA批准了Oncorine,这是第一种用于鼻咽癌的溶瘤病毒。十年后的2012年,欧洲药品管理局(EMA)批准了首个针对脂蛋白脂酶缺乏症的基因治疗产品Glybera,临床试验数量几乎翻了一番。
首个体外基因治疗产品Strimvelis于2016年获得EMA批准。2017年,FDA批准了两种嵌合抗原受体(CAR)T细胞产品Kymriah和Yescarta,这是为未来产品铺平道路的关键里程碑。Luxturna是FDA批准的首个用于Leber先天性黑蒙(LCA)的体内AAV基因治疗产品,并于2017年获得批准。2019年,FDA批准了迄今为止最昂贵的药物Zolgensma,这是一种AAV产品,适用于儿童脊髓性肌肉萎缩症。批准的基因治疗产品数量每年都在增加。
未来的发展(2022–2025)
根据之前的临床试验和目前批准的产品,这一前景广阔的医学领域似乎比以往任何时候都发展得更快,预计在不久的将来会有数十种新的产品获批。我们正在逐步将基因治疗纳入更广泛的疾病治疗领域。
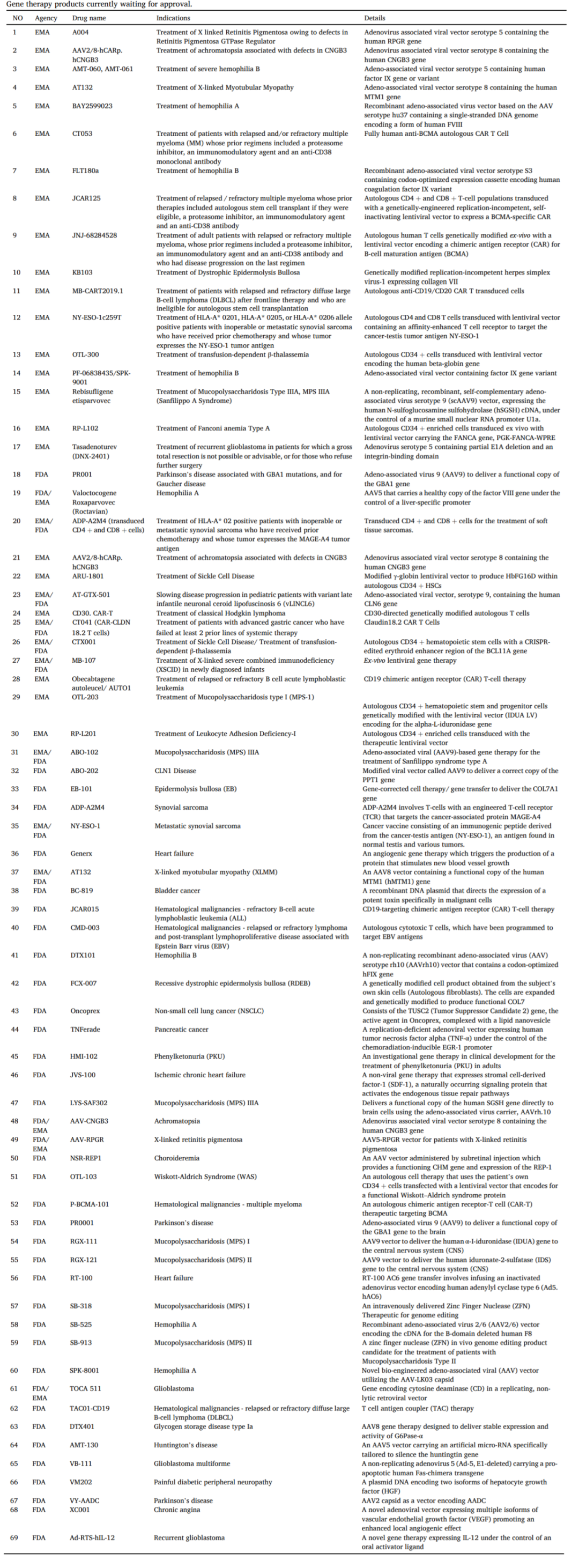
癌症基因治疗的临床概况
目前基因治疗的临床应用可分为三个主要领域:癌症、遗传性疾病和传染病。
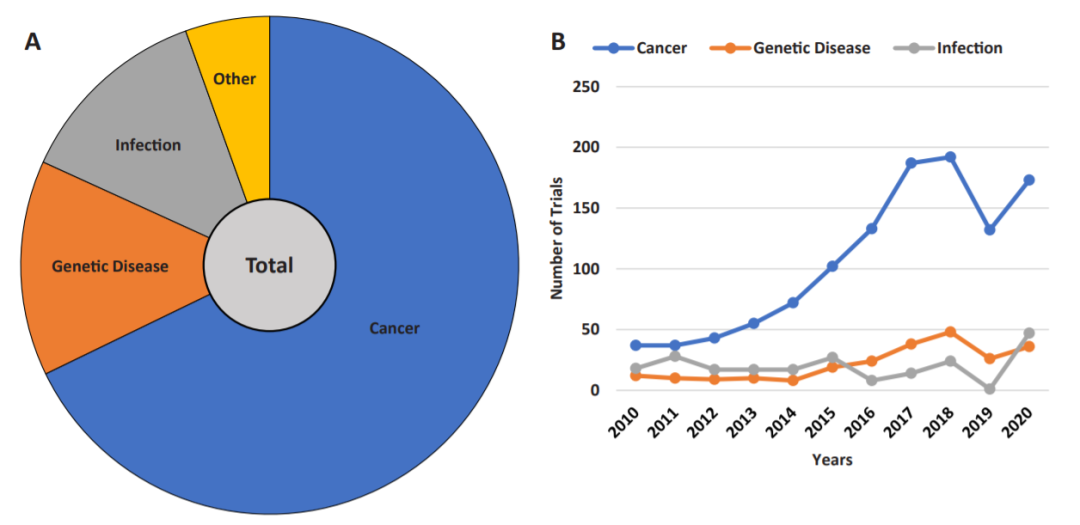
虽然基因治疗被认为是对某些遗传疾病的治疗,但癌症是基因治疗最常见的疾病。从2010年到2020年,癌症相关临床试验占所有研究的大多数。血液学癌症是研究最多的癌症,其次是胃肠道和神经系统癌症。
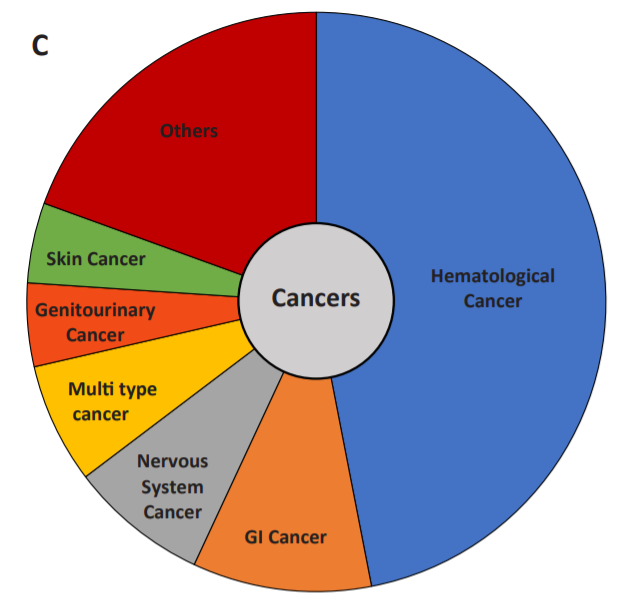
CAR-T细胞是免疫治疗中最知名和最成功的基因治疗应用之一。从目前针对癌症的临床试验来看,大多数试验都处于第一阶段。第2阶段临床试验的数量也很高,但只有少数进行了随后的第3阶段试验。
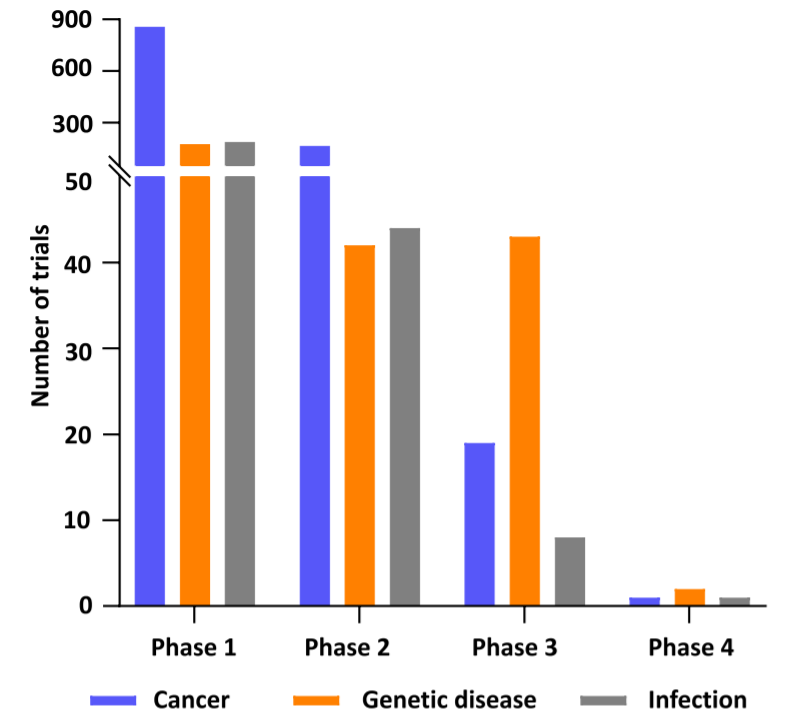
迄今为止,已批准几种基因治疗产品用于治疗癌症,包括gendicine、oncorine、rexin-G、imlygic、delytact和八种CAR-T细胞,包括kymriah、yescarta、tecartus、breyanzi、abecma、ARI-0001、carteyva和carvykti。
遗传疾病基因治疗的临床概况
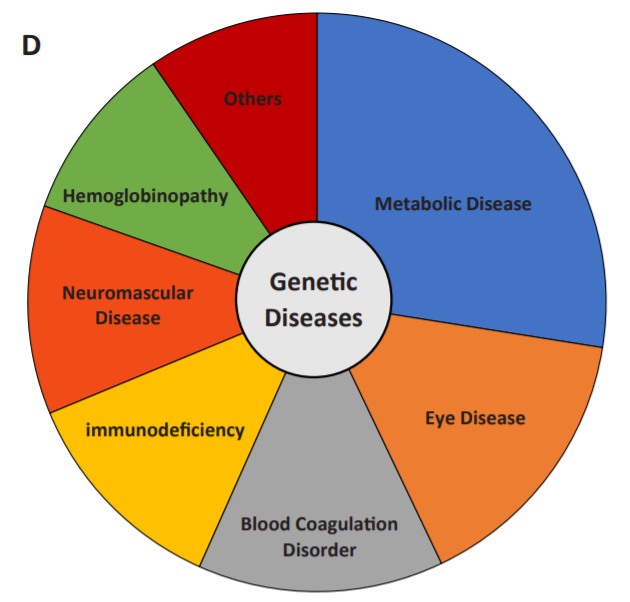
与癌症不同,大多数这类疾病,如地中海贫血、Deschene肌营养不良(DMD)和囊性纤维化,都是遗传性的。半数以上的临床试验集中于代谢障碍、眼部疾病和凝血障碍。进一步,临床试验最多的遗传疾病是SMA、DMD、血友病B、ADA-SCID和β-地中海贫血。
与癌症相比,遗传性疾病的3期临床试验比例更高。LCA、SMA、ATTR淀粉样变、原发性高草酸尿症、淀粉样神经疾病、DMD、脂蛋白脂酶缺乏症、家族性乳糜微粒血症综合征和高甘油三酯血症是3期试验中正在研究的遗传性疾病。此外,还有两项4期临床试验,包括两种FDA和EMA批准的基因治疗产品,Spinraza和Zolgensma治疗SMA。
尽管遗传性疾病临床试验的总数少于癌症,但目前批准用于遗传性疾病的产品数量更高(20对13)。迄今为止,已批准ADA-SCID、DMD、SMA、LCA、B型地中海贫血和多种代谢疾病的产品。
传染病及其他基因治疗的临床概况
人们一直在努力寻找治疗一些最严重传染病的方法,如AIDS或疟疾,基因治疗也不例外。尽管它们只占基因治疗临床试验的一小部分,但随着新冠肺炎大流行的出现,自2019年12月以来启动了29项针对新冠肺炎的试验。艾滋病、新冠肺炎、疟疾、埃博拉、丙型肝炎、人乳头瘤病毒感染和乙型肝炎是临床试验次数最多的传染病。
大多数临床试验使用疫苗接种策略来诱导对相应疾病的免疫力。只有少数处于晚期阶段的基因疗法,即使用DNA作为乙肝病毒载体的基因疗法。从获批的产品来看,基因治疗策略在有效解决传染病方面还有很长的路要走。
此外,除了癌症、遗传病和传染病外,基因治疗的研究也已用于外周血管疾病、骨关节炎、糖尿病视网膜病变、黄斑变性、冠状动脉疾病、心肌缺血和梗死、糖尿病神经病变、过敏性鼻炎、心力衰竭和增生性瘢痕。
基因治疗临床实验的地区分布
20世纪90年代初,美国国家卫生研究所进行了第一次成功的基因治疗临床试验。尽管自那时以来,美国的基因治疗临床试验比任何其他国家都多,但中国率先批准了首个可商业化的基因治疗产品(Gendicine)。20世纪90年代末,欧洲的几个国家是最早实施基因治疗的国家之一。
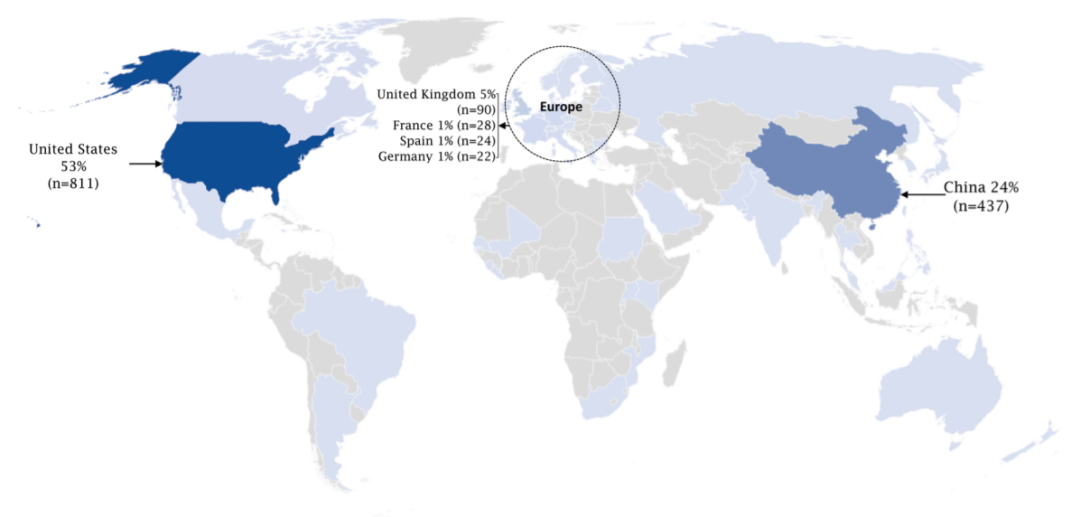
目前,美国和中国主导了基因治疗临床试验,约占所有试验的80%。近年来,包括英国、法国、西班牙和德国在内的其他几个国家在这一前景广阔的领域表现出色。在多个国家的研究所或大学的合作下,正在进行的临床试验越来越多。2010年至2020年,基因治疗临床试验的数量翻了一番。
小结
基因治疗从进入临床实践至今已有约三十年。纵观上个世纪基因治疗的发展趋势,我们已经进入了一个新时代,过去十年获批的基因治疗产品数量不断增加就是证明。并且随着遗传学及生物技术的发展突破,如CRISPR-CAS基因编辑,使得基因疗法可治疗疾病的种类更为广阔。
对基因治疗临床试验的十年趋势分析表明,虽然基因疗法主要用于癌症和遗传性疾病,但包括艾滋病、疟疾和人乳头瘤病毒等多项传染病临床试验都已进入临床晚期研究阶段。在过去10年,体外基因治疗已经取得了一定的进展,目前的管线众多,而体内基因治疗也将会在未来十年迎来新的发展高潮。
参考文献:
1.Gene therapy clinical trials, where do we go? An overview. Biomed Pharmacother.2022 Sep;153:113324
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#基因治疗# #发展阶段# #临床概况#
65