Am J Clin Dermatol:特应性皮炎的眼部并发症
2019-09-28 MedSci 网络
加利福尼亚大学旧金山分校皮肤病学系的Beck KM1和旧金山市Francis I. Proctor基金会眼科的Seitzman GD等人近日在Am J Clin Dermatol杂志上发表了一篇综述文章,这篇综述的目的是提高皮肤科医生对各种特应性皮炎(AD)疗法的潜在眼部不良反应的认识,包括皮质类固醇、钙调神经磷酸酶抑制剂、白细胞介素-4受体α(IL-4Rα)拮抗剂和光疗法等。
加利福尼亚大学旧金山分校皮肤病学系的Beck KM1和旧金山市Francis I. Proctor基金会眼科的Seitzman GD等人近日在Am J Clin Dermatol杂志上发表了一篇综述文章,这篇综述的目的是提高皮肤科医生对各种特应性皮炎(AD)疗法的潜在眼部不良反应的认识,包括皮质类固醇、钙调神经磷酸酶抑制剂、白细胞介素-4受体α(IL-4Rα)拮抗剂和光疗法等。
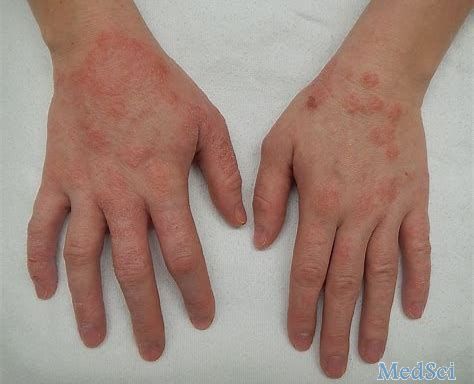
治疗特应性皮炎(AD)的治疗方法可能具有永久性影响视力的不良眼部效应。这些疗法潜在的短期和长期风险包括使用局部皮质类固醇引起的眼压升高和使用dupilumab引起的结膜炎。由于这些不良反应中的一些可能在永久性视力损害发生之前不会出现症状,因此皮肤科医生必须了解这些风险,并主动确保其患者采取适当的措施来预防这些风险。
原文出处:
Beck, K.M., et al., Ocular Co-Morbidities of Atopic Dermatitis. Part II: Ocular Disease Secondary to Treatments. Am J Clin Dermatol, 2019.
本文系梅斯医学(MedSci)原创编译整理,转载需授权!
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#眼部#
93
#并发#
66