梅斯盘点:2021年度眼科界十大研究进展
2021-12-30 MedSci原创 MedSci原创
2021年,眼科同样进展迅速,梅斯医学为您盘点眼科领域十大进展。既有创新药物的问世,也有前沿的基因治疗应用进展,还有眼科重大疾病的治疗突破。
2021年,眼科同样进展迅速,梅斯医学为您盘点眼科领域十大进展。既有创新药物的问世,也有前沿的基因治疗应用进展,还有眼科重大疾病的治疗突破。
1、首个专为眼内设计的双特异性抗体两项nAMD全球III期试验达到主要终点
Faricimab是首个专为眼内设计的双特异性抗体靶向作用于引起多种视网膜疾病的两条通路——血管生成素-2(Ang-2)和血管内皮生长因子-A(VEGF-A)。
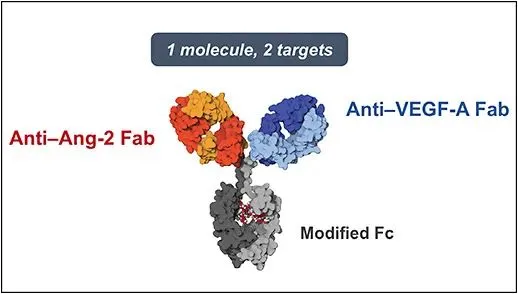
Faricimab在两项nAMD全球III期试验达到主要终点:接受Faricimab (治疗间隔最长达16w)治疗的患者视力获益非劣于对照组阿柏西普(q8w)的患者,这或可在将来降低此类患者注射频率,减轻生活负担,同时Faricimab耐受性良好,在两项研究中均未发现新的不良安全信号。
2、抗VEGF新品Brolucizumab有望突破当前抗VEGF药物应用的瓶颈
Beovu是一种人源化单链抗体片段(scfv),靶向所有类型的血管内皮生长因子-A(VEGF-A),活性药物成分为brolucizumab(RTH258),这单链抗体片段因其体积小、组织渗透性增强、系统循环的快速清除、药物递送特性而在药物开发中受到高度关注,在脉络膜视网膜血管疾病患者中,抑制VEGF途径可抑制新生血管病变的生长,缓解视网膜水肿,改善视力。最新公布的KITE和KESTREL研究显示新一代小分子抗VEGF药物Brolucizumab 6mg在第52周的最佳矫正视力(BCVA)平均值变化不亚于Aflibercept;同时Brolucizumab注射次数较少,且能够有效降低IRF/SRF,在改善解剖结构等方面也具有明显的优势;未来Brolucizumab有望突破当前抗VEGF药物应用的瓶颈,最终减轻患者治疗压力和社会的经济负担。
3、姚克教授团队全球首个培养皿里长出的“先天性白内障”
浙江大学医学院附属第二医院眼科中心、浙江大学眼科医院姚克教授团队在生命科学领域权威期刊nature子刊《npj Regenerative Medicine》(影响因子10.364)发表题为“Modeling Congenital Cataract in Vitro using Patient-Specific Induced Pluripotent Stem Cells”的研究论文。该研究将不同基因突变的先天性白内障患者来源的诱导多能干细胞(iPSCs)诱导分化成再生晶状体,发现与健康个体来源的再生晶状体相比,患者特异性再生晶状体均表现出不同程度的混浊,且其混浊程度、蛋白聚集程度、混浊发展进程等均与患者白内障严重程度及病程一一对应。本研究在世界范围内首次建立了能够模拟患者特异性表型的先天性白内障体外疾病模型,为今后开展白内障机制研究及药物筛选提供了理想平台。
4、张明昌教授团队:世界首例人工生物角膜移植十年报告发表
华中科技大学同济医学院附属协和医院眼科张明昌教授团队在眼科领域著名杂志《Cornea》发表论文“Ten-Year Follow-up of Lamellar Keratoplasty Treatment With Acellular Porcine Corneal Stroma: A Case Report”,该论文报告了世界首例人工生物角膜移植的十年随访情况。
5、陈有信团队发表《应用5G技术实施远程视网膜激光光凝治疗糖尿病视网膜病变》于JAMA Ophthalmology的封面文章
2021年7月8日,北京协和医院眼科陈有信教授团队以original investigation的形式,在眼科领域著名杂志《JAMA Ophthalmology》(最新影响因子7.389)发表论文“Application of 5G Technology to Conduct Real-Time Teleretinal Laser Photocoagulation for the Treatment of Diabetic Retinopathy”,首次报告了应用5G技术实施远程视网膜激光光凝治疗糖尿病视网膜病变的研究。
6、国际近视研究学会白皮书(II)发布,中国专家参与

国际权威眼科学期刊Investigative Ophthalmology & Visual Science 近期推出国际近视研究学会白皮书(II)(International Myopia Institute(IMI)White Papers II)。这份报告汇集了全球近视防治领域顶级专家意见,共有超过134位全球顶尖专家参与编写,包括眼科临床医生、公共卫生专家以及基础科学研究者等。中国大陆共有4位学者参与编写,分别是何明光教授(中山大学眼科中心/墨尔本大学)、邹海东教授和何鲜桂教授(上海市第一人民医院/上海市眼病防治中心)和蓝卫忠教授(中南大学爱尔眼科学院)。
7、全球首个老花治疗眼药水获批上市
老花眼影响全球近20亿人,并且目前没有可供患者使用的有效药物解决方案。现在,患者只能选择配戴老花镜,对很多患者来说并不方便。而接受不可逆转的侵入性外科手术又有与手术相关的内在风险。Vuity是一款毛果芸香碱的创新优化眼科配方。它的主要作用机制是收缩瞳孔,从而增强景深,改善近视力和中距视力。同时保持瞳孔对不同光照情况下的正常反应。

临床结果显示Vuity均达到了主要终点:与安慰剂相比,药物组治疗患者中获得3行或更多行(在阅读图表上读3行的能力)比例显著高于安慰剂组,近距离视觉显著改善,而远视力不受影响。15分钟起效,持续时间至少三小时,最长可达六小时。安全性方面,该研究中,任何接受Vuity治疗的患者中均未观察到治疗时期的严重不良事件,其中最常见的非严重不良事件(>5%)是头痛。大多数副作用是轻微和短暂的,只有1.2%的患者因不良事件而停药。研发人员表示,这款眼药水,虽然目前的目标人群是40岁至50岁有轻度至中度老花眼的患者,但正计划在老年患者身上进行药物试验研究。
8、首个眼科体内基因治疗药物NR082治疗LHON注册性临床试验完成首例患者入组给药
首个眼科体内基因治疗药物NR082治疗LHON注册性临床试验完成首例患者入组给药,该临床试验(G.O.L.D.)是一项多中心、1/2/3期两阶段临床研究,该项研究将在ND4线粒体基因突变引起的Leber遗传性视神经病变(LHON)患者中评价NR082基因治疗的安全性、耐受性和有效性。NR082是国内首个获得临床试验许可的眼科体内AAV基因治疗药物,并已于2020年9月获得美国FDA孤儿药认定。
Leber遗传性视神经病变(LHON)是一种母系遗传的线粒体疾病,多发于14-21岁的青年男性,患者表现为双目视力受损至失明。这一疾病由德国眼科医生 Theodor Leber于1871年首先发现,目前全球患者约60万人,其中中国10万人。90%的LHON是由3个线粒体DNA突变所导致的, G11778A (ND4基因)、G3460A(ND1基因)、T14484C(ND6基因),其中ND4的G11778A突变最多,约占50%~80%。由于该突变使细胞线粒体生物呼吸链功能受损,造成ATP生成减少,使患者视神经节细胞产生氧化应激,导致细胞凋亡。目前临床上尚无针对Leber遗传性视神经病变的有效疗法或治愈手段。
9、体内基因编辑治疗先天性失明,Editas公布首个人体试验结果
Editas Medicine公司公布了其体内基因编辑疗法EDIT-101,在治疗Leber先天性黑矇10(LCA10)的1/2期临床试验的初步数据。在安全性方面,试验未观察到严重不良事件和剂量限制性毒性。同时,在两名接受中等剂量治疗的成人患者中发现支持临床获益的疗效信号。
先天性黑矇(LCA)是一类遗传性视网膜退化疾病,它是遗传性儿童失明最常见的原因。LCA的症状在出生后第一年就会出现,导致显著视力丧失,以至于完全失明。LCA10是LCA中最常见的类型,占20-30%,它的病因是CEP290基因上的突变。
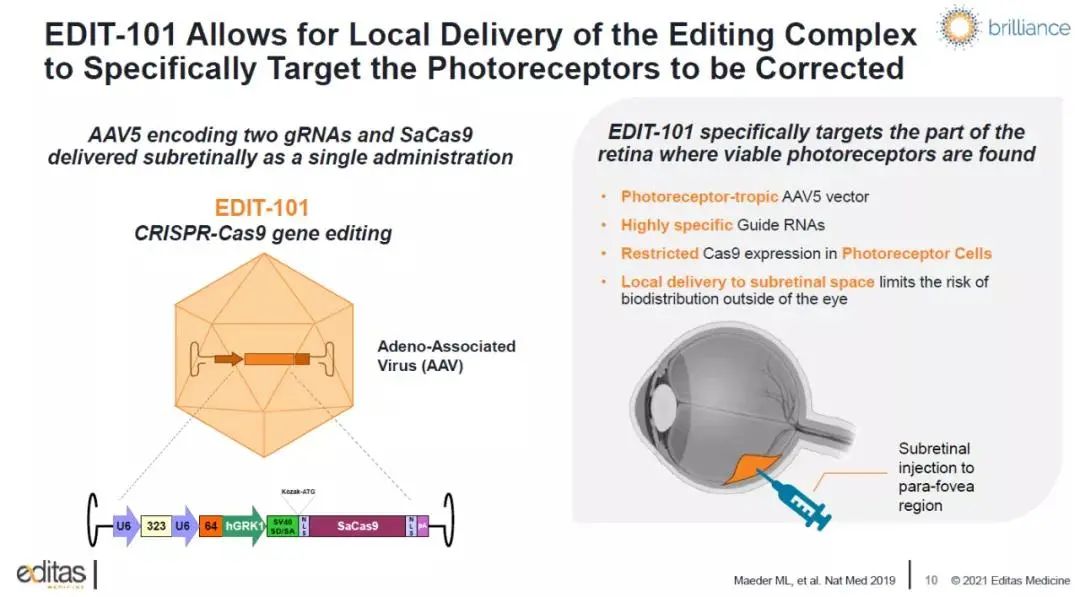
▲ EDIT-101的作用机理(图片来源:Editas Medicine公司官网)
EDIT-101将编码Cas9核酸酶变体SaCas9的基因和两个指导RNA(gRNA)装进AAV5载体中,通过视网膜下注射将基因编辑系统递送到感光细胞中。gRNA指导的基因编辑可以修复CEP290基因上的致病突变,从而改善感光细胞功能,为患者带来临床益处。
10、Nanoscope Therapeutics将在视网膜协会年会上公布光遗传学基因治疗视网膜色素变性致盲患者的阳性数据
Nanoscope Therapeutics Inc. 宣布其针对ABCA4 突变盲人的光遗传基因疗法临床研究结果将于 2021 年 9 月 29 日至 10 月 2 日在芝加哥举行的视网膜协会第 54 届年度科学会议上发表。
Sai Chavala 博士的题为“ABCA4 突变视网膜变性患者的光遗传学视力恢复”的演讲定于 2021 年 10 月 1 日星期五上午 11:03 在芝加哥丽思卡尔顿酒店的大宴会厅举行。视网膜协会成立于 1968 年,其目的是为了与视网膜疾病和损伤的诊断、护理和治疗有关的教育和科学目的。
德克萨斯基督教大学UNT健康科学中心医学院教授Chavala 博士将介绍使用 Nanoscope 的多特征视蛋白 (MCO) 基因疗法进行玻璃体内给药的视网膜色素变性 (RP) 患者的研究结果。ABCA4基因突变的RP患者接受单次基因治疗的玻璃体内注射,随访52周,所有患者的视力和功能均得到改善,无严重不良事件。
Nanoscope 的光遗传学疗法使用专有的 AAV2 载体将 MCO 基因传递到视网膜细胞中,在那里它们表达对环境光敏感的多色视蛋白,用于在不同颜色环境中恢复视力。该疗法可在医疗办公室进行,专注于疾病表型,无论基因突变如何,都能治疗视网膜退行性疾病,如 RP。
MCO-010 目前正在美国进行一项随机、双盲的 2b 期多中心试验 (NCT04945772)。预计将于 2022 年第四季度取得结果。MCO-010 具有美国食品和药物管理局针对 RP 和 Stargardt 病的孤儿药资格,已知这些疾病与 ABCA4 突变有关。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












了解前沿知识,更好提升自己
96
深受启发
84
学习了
92
学习了
96
牛
82
#梅斯#
81
#研究进展#
107
认真学习了
118