Angew:可释放一氧化氮光敏剂实现 “氧节流”型光动力疗法,诱导免疫原性癌细胞死亡
2024-06-22 BioMed科技 BioMed科技 发表于威斯康星
报道了两种被两个或四个一氧化氮(NO)释放片段取代的锌(II)酞菁,即ZnPc-2NO和ZnPc-4NO,它们可以抑制线粒体呼吸,从而为PDT保留更多的细胞内氧气。
光动力疗法(PDT)利用活性氧(ROS)根除癌症细胞。它的有效性取决于氧含量,而氧含量在缺氧的肿瘤微环境中是稀缺的。为此,香港城市大学Pui-Chi Lo和Kwan T. Chow等人报道了两种被两个或四个一氧化氮(NO)释放片段取代的锌(II)酞菁,即ZnPc-2NO和ZnPc-4NO,它们可以抑制线粒体呼吸,从而为PDT保留更多的细胞内氧气。使用HT29人结直肠癌细胞和A549人肺癌细胞,研究证明,这两种偶联物在与细胞内谷胱甘肽相互作用时都会释放NO,可以降低细胞耗氧量和三磷酸腺苷的产生,并改变线粒体膜电位。它们还可以缓解癌症细胞的缺氧状态,降低缺氧诱导因子蛋白HIF-1α的表达。在光照射下,即使在缺氧条件下,这两种缀合物也能产生ROS并诱导细胞毒性,克服了PDT的氧依赖性。有趣的是,ZnPc-2NO的光动力作用引发损伤相关分子模式的释放,诱导树突状细胞的成熟并引发抗肿瘤免疫反应。通过一系列体外和体内实验,研究证明了这种节省氧气的PDT可引起的免疫原性细胞死亡。相关工作以“Inducing Immunogenic Cancer Cell Death through Oxygen-Economized Photodynamic Therapy with Nitric Oxide-Releasing Photosensitizers”为题发表在Angew。

【文章要点】
NO可以抑制细胞色素氧化酶(复合物IV)的酶促功能,抑制细胞呼吸。因此,它是一种很有前途的对抗肿瘤缺氧的药物。到目前为止,已经开发了几种NO供体,如有机硝酸盐、金属NO络合物(如硝普钠、SNP)、N-亚硝胺和亚硝基硫醇。NO供体通常被封装在基于聚合物或金属有机框架的纳米载体中。然而,这些纳米材料的制造通常涉及繁琐的程序,而且这些纳米材料也可能对健康组织构成潜在危害。而到迄今为止很少研究报道了分子对应物以释放NO。因此,作者试图通过设计两种释放NO的分子光敏剂来缓解肿瘤缺氧以增强PDT。这些缀合物由酞菁锌(II)核组成,并且酞菁锌核被两个或四个谷胱甘肽(GSH)响应性NO供体取代,分别形成ZnPc-2NO和ZnPc-4NO(图1)。
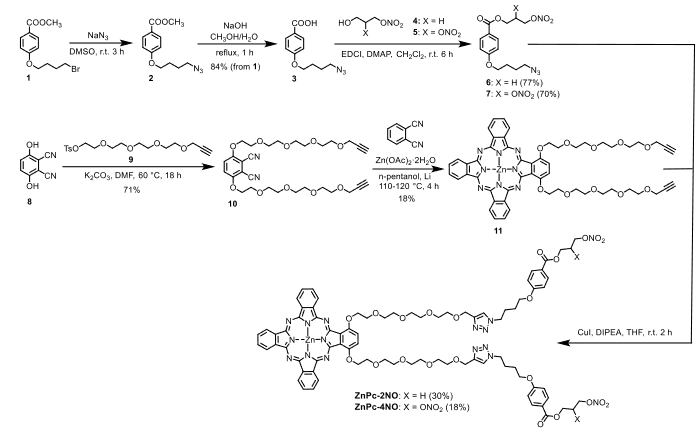
图1 ZnPc-2NO和ZnPc-4NO的合成路径
在进入癌症细胞后,这些缀合物与富集的细胞内GSH反应,释放NO,NO可抑制细胞呼吸,从而降低耗氧率(OCR)和三磷酸腺苷(ATP)的产生,最终逆转肿瘤缺氧状态。释放的NO也可能导致线粒体功能障碍和缺氧诱导因子1α(HIF-1α)下调,以增强PDT。有趣的是,在研究过程中,研究还发现ZnPc-2NO这种光敏剂的光动力作用可以诱导癌症细胞的免疫原性细胞死亡(ICD)。它诱导损伤相关分子模式(DAMP)的释放,包括钙网蛋白(CRT)、ATP和高迁移率组蛋白盒-1(HMGB1),触发树突状细胞(DC)的成熟和促炎细胞因子的产生。因此一系列体外和体内实验显示,通过ZnPc-2NO诱导的缺氧PDT可引发抗肿瘤免疫反应(图2)。
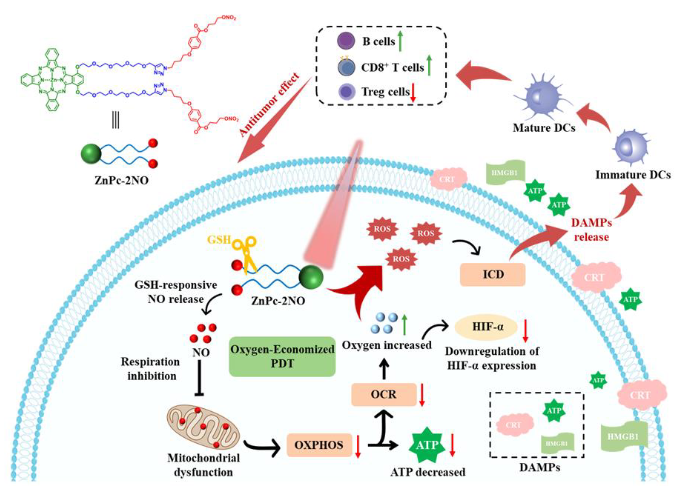
图2 ZnPc-2NO的抗肿瘤机制示意图
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202404561
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#活性氧# #肿瘤微环境# #光动力疗法# #免疫原性细胞死亡#
0