GPRC5D,多发性骨髓瘤免疫治疗新靶点
2023-02-07 聊聊血液 聊聊血液 发表于上海
目前多发性骨髓瘤领域的大多数CAR T细胞临床试验都将BCMA作为抗原靶点,FDA已经批准两种BCMA CAR T 产品上市,但BCMA CAR T的复发仍然是其主要障碍。
目前多发性骨髓瘤领域的大多数CAR T细胞临床试验都将BCMA作为抗原靶点,FDA已经批准两种BCMA CAR T 产品上市,但BCMA CAR T的复发仍然是其主要障碍,包括由于 BCMA 抗原表达缺失导致的复发。因此尽管BCMA靶向治疗取得了可喜的结果,仍需要探索骨髓瘤的新靶点。
GPRC5D是一种 G 蛋白偶联受体,在多发性骨髓瘤患者的骨髓瘤细胞系和骨髓浆细胞中表达,在正常细胞中仅表达于皮肤角化组织,是多发性骨髓瘤的替代免疫治疗靶抗原。新英格兰医学杂志近期报道了一项美国 I 期早期、剂量递增研究,这是首次正式发表的关于 GPRC5D CAR T 细胞治疗RRMM 患者的疗效数据。研究给予多发性骨髓瘤患者GPRC5D CAR T细胞(MCARH109)治疗,患者中包括既往接受过抗BCMA治疗的患者。结果不良事件呈剂量依赖性,在最高剂量下仅1例患者发生4级细胞因子释放综合征和4级神经毒性作用;但2例患者发生新发小脑疾病,研究人员认为小脑疾病可能是由 MCARH109 对大脑下橄榄核(GPRC5D富集的区域)的在靶(on-target)作用引起的。17例患者中的12例 (71%) 实现总体缓解,包括既往接受过抗BCMA治疗的患者。
OriCAR-017
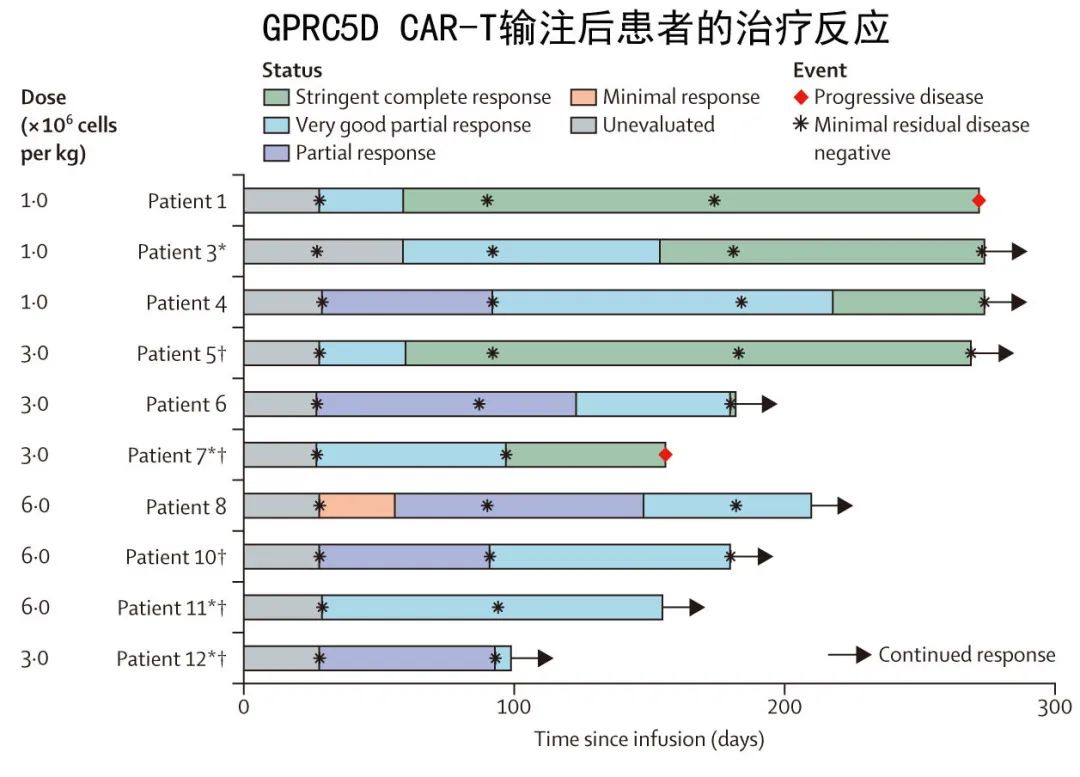
近期《Lancet haematology》报道了浙江大学医学院附属第一医院/良渚实验室黄河教授团队GPRC5D CAR-T(OriCAR-017)治疗RRMM的I期研究结果,证实GPRC5D CAR-T在RRMM患者中的良好安全性和初步有效性。研究共纳入10例RRMM患者,中位年龄64岁,60%有高危遗传学因素(del17p有30%,t(4:14)有50%),既往中位治疗5.5线,40%有髓外病变,80%为II-III期,50%为BCMA CAR-T后复发。安全性方面,该研究在3个剂量组均无剂量限制性毒性,无严重不良事件;常见≥3级不良反应主要是血液系统毒性,但恢复迅速。所有患者均发生了低级别的CRS,其中9例为1级,1例为2级,无神经毒性报道。包括5例BCMA CAR-T后复发的患者在内,10例患者的ORR为100%,其中6例(60%)获得sCR,4例(40%)获得VGPR;中位PFS未达到,9个月PFS率估计值为87.5%。
评论
Nico Gagelmann和Jennifer Brudno教授同期在《Lancet haematology》发表评论认为,两项研究的间接比较显示,GPRC5D CAR T 细胞治疗均具有令人鼓舞的疗效,但安全性特征存在差异。缓解率很有前景,尤其是考虑到既往接受过 BCMA 治疗的患者在两项试验中均有很好的代表性。当然两项研究的中位随访时间相当短,从而无法了解缓解持久性和生存期。尽管两项试验中纳入的患者均接受过多线治疗,但 OriCAR-017 研究中的患者暴露于单抗的程度低于接受MCARH109研究,可能是由于彼时CD38单抗在中国的可及性不足。此外,OriCAR-017研究中的患者很少(20%)既往接受过自体造血干细胞移植,而欧美几乎所有患者均在CAR T细胞治疗前接受过自体移植。患者人群的差异性可能限制了研究间的可比性,这些差异可能解释了 OriCAR-017 的结果更优,当然差异也可以归因于基于双表位纳米抗体的 CAR 结构的优越疗效。此外在OriCAR-017研究中没有患者发生类似MCARH109那样的在靶小脑毒性效应,但尚不清楚 OriCAR-017 CAR 结构是否不会引起这些疾病,还是否根本未捕获这些效应。
OriCAR-017和MCARH109的研究结果表明,用GPRC5D CAR T 细胞治疗是多发性骨髓瘤可行的治疗方法,值得进一步研究,且在既往暴露于BCMA治疗患者中的活性尤其有前景。但对于这种新抗原靶点,多大程度的在靶毒性作用会成为CAR T细胞治疗的障碍,还尚待观察。总的来说, 这些早期研究的结果存在局限,需要更大型、多中心和多国研究在不同的患者组中评估该策略。
除了上述两项研究,另一个GPRC5D CAR T产品(CC-95266) 的 I 期研究中期结果表明,ORR和CR率分别为90%和47%,也有极好的疗效。

评论
《Nature Reviews Clinical Oncology》近日也发表了Sham Mailankody教授等针对三个GPRC5D产品的评论文章(Sham Mailankody教授是第一个GPRC5D CAR T产品MCARH109的主要研究者),他们认为这3项 GPRC5D CAR T 细胞研究的初步数据都非常令人鼓舞,但也需要更长时间的随访来确定缓解的持久性。重要的是,所有3项研究均允许入组既往暴露于 BCMA 靶向治疗的患者,而缓解率似乎不受既往暴露的影响。CAR T 细胞相关毒性(包括细胞因子释放综合征和神经毒性)的发生率与 BCMA CAR T 细胞产品基本一致,但GPRC5D CAR T细胞似乎也会引起味觉障碍(高达15%)和低度皮肤和指甲毒性(高达65%),这在靶向 BCMA 的 CAR T 细胞中通常不会发生,可能是因为皮肤和硬角质化组织中细胞亚群的 GPRC5D 表达。在接受最高剂量 MCARH109 的患者中报告了2例迟发型小脑毒性,该不良事件可能与脑干下橄榄核内 GPRC5D 的低水平表达有关,GPRC5D将信号传递至小脑;而CC-95266或 OriCAR-017 均未报告小脑毒性。
GPRC5D T 细胞参与治疗在各研究中均显示了良好的反应,但疾病复发仍然很常见,而当下对潜在机制知之甚少。MCARH109研究的初步结果表明,GPRC5D表达缺失可能是部分患者疾病复发的潜在机制。
考虑到 GPRC5D T 细胞参与治疗的令人鼓舞的疗效,有一个问题仍然存在:在 MM 的治疗策略中,接下来研究含GPRC5D治疗的方向在哪里?目前尚无公认的标准方法,但由于与含GPRC5D的治疗相比BCMA治疗已有长期数据,因此 BCMA T 细胞衔接器通常被公认为三类暴露(triple-class-exposed)MM 患者的当代免疫治疗选择。在没有随机比较的情况下,GPRC5D T 细胞衔接器很可能是 BCMA 靶向治疗后疾病复发患者的治疗选择。
总的来说,GPRC5D似乎是 MM 患者的高活性免疫治疗靶点,GPRC5D T细胞衔接器的可用性可能会扩大患者可用的治疗选择,当然确定定使用这些药物的最佳环境以及进一步评估和减轻潜在的在靶、肿瘤外毒性仍有许多工作要做。
参考文献
1. Mingming Zhang, Guoqing Wei, Linghui Zho,et al. GPRC5D CAR T cells (OriCAR-017) in patients with relapsed or refractory multiple myeloma (POLARIS): a first-in-human, single-centre, single-arm, phase 1 trial.Lancet Haematol . 2023 Feb;10(2):e107-e116. doi: 10.1016/S2352-3026(22)00372-6.
2. Nico Gagelmann, Jennifer Brudno .GPRC5D-targeting chimeric antigen receptors: a new treatment for multiple myeloma?Lancet Haematol . 2023 Feb;10(2):e82-e83. doi: 10.1016/S2352-3026(22)00385-4.
3. Karthik Nath, Bruno A Costa, Sham Mailankody. GPRC5D as a novel immunotherapeutic target in multiple myeloma.Nat Rev Clin Oncol . 2023 Feb 1. doi: 10.1038/s41571-023-00735-4
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










总的来说,GPRC5D似乎是 MM 患者的高活性免疫治疗靶点,GPRC5D T细胞衔接器的可用性可能会扩大患者可用的治疗选择,当然确定定使用这些药物的最佳环境以及进一步评估和减轻潜在的在靶、肿瘤外毒性仍有许多工作要做
0