J Invest Dermatol:天疱疮:从疾病机制到可用药途径
2022-02-16 医路坦克 MedSci原创
天疱疮是理解抗体介导的人类自身免疫性疾病机制的范例。本综述将总结天疱疮的疾病途径和临床试验研究。

天疱疮是理解抗体介导的人类自身免疫性疾病机制的范例。在天疱疮中,以IgG4为主的自身抗体通过直接干扰桥粒蛋白的相互作用和随后破坏桥粒和信号通路而导致表皮内起疱。天疱疮疾病机制的揭开已经确定了许多临床试验的机会,这些试验有望为这些潜在的危及生命的疾病找到更安全和更有效的治疗方法。本综述将总结天疱疮的疾病途径和临床试验研究。
天疱疮是一组罕见的,可能危及生命的疾病,临床上表现为松弛的水疱和糜烂。天疱疮的微观标志是棘层松解或角质形成细胞(KC)细胞间粘附的丧失,伴随着与KC细胞表面结合的自身抗体。自身抗体靶向粘膜显性寻常型天疱疮(PV)中的桥粒粘附分子桥粒芯糖蛋白(DSG)3和粘膜皮肤PV中的靶DSG3加DSG1,引起基底上水泡,而浅表皮肤水泡由叶天疱疮(PF)中的DSG1自身抗体引起。罕见的非典型PV变体可能显示desmocollin(DSC)3自身抗体,靶向其他自身抗原的自身抗体可协同损害上皮粘附,但只有DSG3和DSG1自身抗体提供证据支持其引起PV和PF特定疾病表现的必要性和充分性。在天疱疮病理生理学共识模型中,DSG自身抗体与DSG3和/或DSG1结合,DSG3和/或DSG1通过DSG相互作用的空间位阻破坏KC的粘附(解释了Nikolsky征,在这个征中,正常皮肤可以通过剪切力诱发水泡),桥粒组装和拆卸受损导致DSG耗尽的桥粒,以及增加皮肤起泡的KC信号通路失调。与类天疱疮不同,天疱疮中的水疱形成不依赖于补体或Fc效应子功能。因此,天疱疮的研究集中于表征抗DSG B细胞和抗体以及调节自身抗体的致病作用的信号传导途径。总体而言,信号抑制为天疱疮治疗提供了重要的辅助手段,但可能不足以克服高滴度自身抗体的致病性。
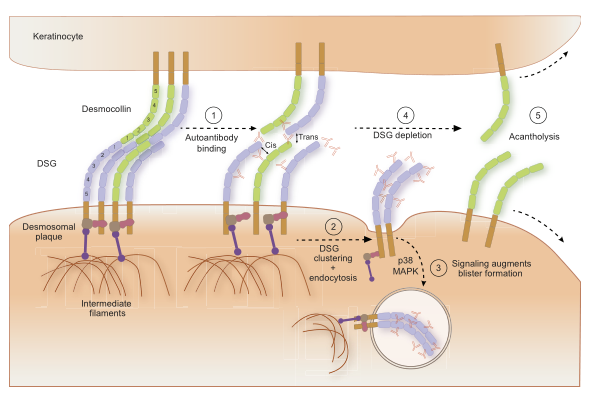 图1.天疱疮的疾病途径
图1.天疱疮的疾病途径
DSGs与细胞质斑块蛋白相互作用,并与相邻角质形成细胞上的桥粒粘连蛋白进行反式相互作用,主要通过细胞外钙粘蛋白1结构域中的残基介导桥粒粘附。
- 自身抗体与DSG结合可直接干扰顺式或反式黏附相互作用,削弱桥粒黏附。
- DSG在天疱疮IgG结合后聚集,并在p38-MAPK依赖的过程中内化。
- DSG转运受p38-MAPK和蛋白激酶C最直接的调控,其他信号通路可能协同作用促进水泡的形成。
- DSG聚集性和胞吞作用破坏桥粒组装和促进拆解,导致DSG耗尽桥粒,桥粒粘附减弱,棘球松解。
- DSG聚集和内吞作用破坏桥粒组装,促进解体,导致DSG耗尽桥粒,桥粒粘附减弱,棘层松解。DSG,桥粒晶状体蛋白(Desmoglein)。
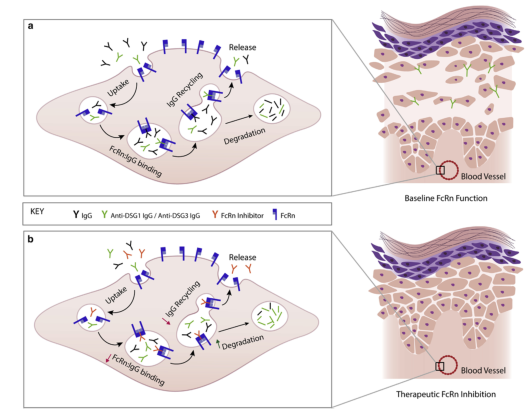
静脉注射免疫球蛋白通过饱和FcRN增加自身抗体的分解代谢,抑制Fc介导的炎症和抗原提呈,可显著降低天疱疮患者的自身抗体滴度和治疗失败,支持其治疗效果。
天疱疮中的B细胞耗竭,利妥昔单抗抗CD20B细胞耗竭是自皮质类固醇出现以来天疱疮治疗上最大的进步,导致食品和药物管理局(FDA)在2018年批准利妥昔单抗治疗PV。在一项随机对照试验中,接受一线维持剂量利妥昔单抗和皮质类固醇治疗的患者中,90%的患者在第24个月时至少2个月的激素完全缓解(CR),而单独使用大剂量强的松治疗的患者中,这一比例为28%。随后的3期试验(NCT02383589;Werth等人,2021年)显示,到第52周,接受维持量利妥昔单抗和类固醇治疗的患者中,有40.3%的患者在停用类固醇至少16周后获得CR,相比之下,接受霉酚酸酯和类固醇治疗的患者中,这一比例为9.5%。
新型B细胞靶向剂:针对BAFF-R的单克隆抗体Ialumab(VAY736)能耗尽记忆B细胞的晚期过渡期。伊阿卢单抗(NCT01930175)的随机对照试验显示,与安慰剂治疗的对照组相比,7名天疱疮患者第12周的PDAI平均评分降低了73%。天疱疮没有进一步的临床开发计划。Rilzabrutinib(PRN1008)是一种Bruton酪氨酸激酶抑制剂,可在不耗尽B细胞的情况下损害浆细胞分化和抗体产生。在2b期研究(NCT02704429)中,15名PV患者中有10名(67%)皮肤透明或接近透明,40%的患者在服用24周的利扎布替尼(Rilzabrutinib)作为辅助药物并达到每天0.5毫克/公斤的皮质类固醇后获得CR(Murrell等人,2020年)。
天疱疮治疗的理想方法是仅持久地耗尽致病的抗DSG B细胞,而保留提供免疫保护的正常B细胞。在FDA批准的可诱导B细胞癌持久缓解的嵌合抗原受体技术(Tisagenlecleucel)的基础上,开发了一种名为DSG3嵌合自身抗体受体T(CAART)细胞的精确细胞免疫疗法。患者T细胞被设计表达由DSG3EC1-4胞外区组成的嵌合自身抗体受体,它包含所有已知的致病性PV自身抗体表位,与CD137-CD3Z激活和共刺激结构域相连(Ellebrecht等人,2016;Lee等人,2020)。DSG3-CAART的设计目的是专门消耗抗DSG3 B细胞,同时产生能够长期存活的记忆CAART细胞,潜在地提供持久的保护,防止抗DSG3 B细胞复发。DSG3 CAART治疗粘膜占优势的PV的1期试验目前正在招募中(NCT04422912)。
在天疱疮中使用利妥昔单抗去除B细胞可以实现完全但短暂的疾病缓解;更持久或更安全地去除致病性B细胞或抗体的治疗是正在进行的临床开发的重点。
文献来源: Ellebrecht CT, Maseda D, Payne AS,Pemphigus and Pemphigoid: From Disease Mechanisms to Druggable Pathways.J Invest Dermatol 2021 Oct 28
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#疾病机制#
50
#EST#
39