亲和素-生物素系统,如何减少干扰,更好地应用于免疫检测
2020-04-14 Stephen Jennel 生物医学知识局
(链霉)亲和素-生物素是免疫检测中常用的信号放大系统。亲和素是蛋清中常见的糖类蛋白,由四个相同的亚基组成。
1. 什么是亲和素-生物素系统
(链霉)亲和素-生物素是免疫检测中常用的信号放大系统。亲和素是蛋清中常见的糖类蛋白,由四个相同的亚基组成。每一个亚基都包含一个生物素结合位点,因此一个理论上正常的亲和素能够结合4个生物素。亲和素与生物素具有非常强烈的亲和力,其解离常数大约是1.3*10-15M,是已知自然界中最强的非共价相互作用之一。亲和素的蛋白质结构非常稳定,即使在浓度高达8M的尿素溶液中,也能够维持结构的完整性,保持对生物素的亲和力。并且在结合生物素后,亲和素-生物素结构的稳定性进一步增强,研究表明,即使在浓度为8M的盐酸胍中,亲和素-生物素复合物依然能够稳定存在。另外,亲和素-生物素的结合与抗体-抗原的结合类似,有极高的特异性,能够在复杂的溶液环境中相互结合,因此,亲和素-生物素系统广泛应用在免疫检测中。其中应用最为广泛的方式是将亲和素包被在磁珠表面,生物素标记抗体。
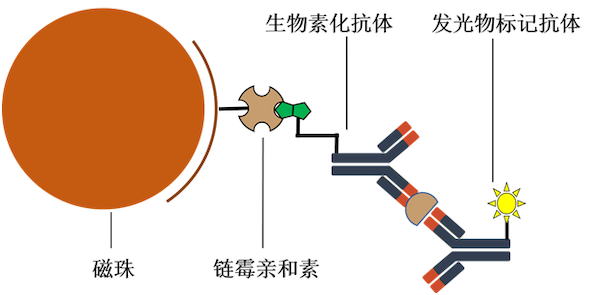
△生物素磁珠,生物素化抗体免疫检测示意图
2. 亲和素,链霉亲和素,以及中性亲和素
亲和素蛋白是碱性糖蛋白,分子量约为67kDa,蛋白质等电点约为10。由于蛋白质等电点较高,在pH中性条件下,亲和素带正电。并且亲和素存在寡糖成分(主要由甘露糖和N-乙酰氨基葡萄糖组成的异质结构),容易与细胞表面、核酸、凝集素等物质产生非特异性结合,造成本底过高的问题。链霉亲和素是由链霉菌中表达纯化出的蛋白,与亲和素类似,链霉亲和素也由四聚体组成,每个单体都可以以极高的亲和力结合一个生物素。不同的是,链霉亲和素没有糖链,分子量比亲和素略低,大约为53kDa,蛋白质等电点在6.8~7.5之间,非特异性吸附也比亲和素要小很多。
另外一种广泛使用的亲和素是中性亲和素(NeutrAvidin)。中性亲和素实际是去除糖链后的亲和素,分子量约为60kDa,蛋白质等电点为6.3。由于去除了糖链,中性亲和素的非特性得到了极大的降低,同时又保留了亲和素对生物素极高的亲和力。

△几种亲和素的性质对比
3. 生物素及其衍生物结构
生物素又被称为维生素H,或者维生素B7,是一种水溶性维生素,其功能是在人体内参与脂肪、糖、蛋白代谢等重要物质的生化反应。生物素广泛存在与动物肝、肾、酵母、牛乳中。
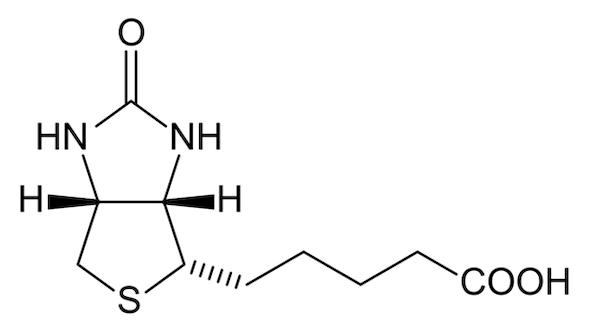
△生物素分子结构图
生物素分子量约为244,能够以共价键的形式,标记在抗体蛋白的表面,而不影响蛋白质的生物活性。因此广泛应用于蛋白标记,进而通过亲和素-生物素系统对标记蛋白进行分离、富集、检测。
如今通过不同的改造方式,生物素有各种各样的衍生物,生物素标记蛋白的技术也日趋成熟。生物素衍生物结构基本上由生物素双环结构,戊酸侧链,间隔臂,以及反应基团组成。其中间隔臂的亲疏水性,长度对于蛋白的标记效率,标记后生物素与亲和素后续反应性有重要影响。如链霉亲和素与生物素结合位点是一个口袋型结构,深度大约有0.9纳米。因此,生物素的间隔臂长度,直接影响到标记在蛋白表面的生物素是否能够进入亲和素反应口袋中。在某些应用中,长间隔臂的生物素具有更高的分析灵敏度。

△生物素衍生物结构示意图
△常用生物素臂长及分子量
4. 生物素干扰
生物干扰是亲和素-生物素系统检测中普遍存在的问题。采用亲和素-生物素系统进行免疫检测时,如果待测样本中存如果存在高浓度的游离生物素,将与生物素化抗体竞争结合亲和素的结合位点,进而影响检测结果。
作为水溶性B族维生素,生物素在人体内主要经过肾脏代谢。正常人体血液中生物素浓度范围大约在0.28~0.55ng/mL,远低于各类免疫检测试剂盒中声称的产生干扰的生物素浓度。但是日常补充生物素的人群不在少数,根据一项统计数据,美国大约有15%的人群日常补充生物素。而一篇发表在ClinicalChemistry上的研究文献显示,正常人在口服100mg生物素后1.5小时,血液中生物素浓度达到峰值,平均为762.52ng/mL,24小时后,浓度下降至平均71.59ng/mL,高于许多检测试剂盒声称的生物素干扰浓度下限。而且依据不同的生物素摄入量,以及不同检测试剂的性能,口服生物素后对检测的干扰可能持续至48小时。
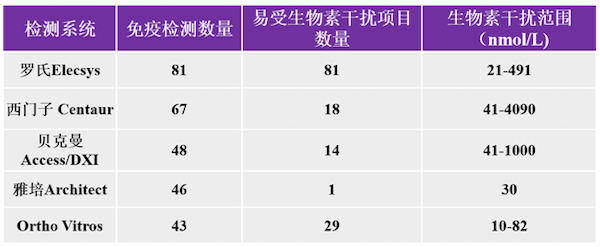
△各大系统受生物素干扰统计分析。(注,为美国FDA注册项目)
由于基本上不采用生物素亲和素系统,雅培的免疫检测试剂一直以无生物素干扰作为卖点之一。实际上在2011年注册的维生素D检测试剂中,雅培采用了生物素标记的维生素D作为竞争衍生物,与鼠抗生物素抗体标记的吖啶酯作为标记物进行检测,因此也会在一定程度上受到生物素干扰。
5. 抗生物素干扰的方法
理论上所有采用亲和素-生物素系统的检测试剂盒都会受到生物素干扰。目前有几种方法可以降低生物素干扰,或者提高试剂对生物素干扰的耐受性。
最简单直接的方法是提高亲和素的加入量,如加大亲和素磁珠的浓度,以提高反应体系对生物素的载量,但是这种做法通常会增加试剂的成本,而且改善的程度有限。另外一种有效的方法是提前将亲和素组分和生物素化组分提前预混,让亲和素先与生物素化抗体反应,进而减少样本中游离生物素对反应的干扰。诊断试剂盒一般是采用链霉亲和素磁珠-生物素反应体系,因此在解决生物素干扰的问题上,各大公司一直在创新进步,希望能够从技术上彻底解决这一问题。例如,近日公布的一项专利显示,某一公司诊断开发出一种抗生物素干扰的抗体,能够特异性结合游离生物素,而对标记在抗体表面的生物素不结合,因此可以作为抗干扰组分添加至反应体系中,通过结合样本中游离的生物素而减少干扰。另外一种方法是采用抗生物素抗体替代亲和素类蛋白。如美国一家初创公司就开发出了特定的抗生物素抗体,其对生物素的亲和力与亲和素类蛋白相当,但是与游离生物素的亲和力则要低100万倍。
-总结-
虽然生物素干扰一直存在,也尚未得到完全解决。但是众多厂家依然在化学发光免疫检测中使用(链霉)亲和素-生物素系统,一个原因是早期开发过程中采用了此类模式,如果摈弃或改变这种模式,无异于重新开发试剂,调整仪器系统,并且需要重新进行注册申报,需要花费大量的人力物力,以及消耗非常长的时间。另一个原因是采用这种模式能够简化试剂开发生产流程,并且在一定程度上降低试剂成本。不管出于何种原因,(链霉)亲和素-生物素系统依然广泛应用于免疫检测中,但是生物素干扰是一个不容忽视的问题。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#生物素#
83