苏州大学陈倩教授《AM》:共组装叶黄素/尼达尼布纳米颗粒,创新AMD治疗策略!
2024-02-14 BioMed科技 BioMed科技 发表于陕西省
苏州大学功能纳米与软物质研究院陈倩教授发现共同组装的叶黄素/尼达尼布纳米颗粒在小鼠体内显示出显著改善的稳定性,并实现了至少两个月的长期持续药物释放。
年龄相关性黄斑变性(AMD)已成为全球性的老年性疾病,临床上主流的治疗方法是频繁的抗血管内皮生长因子(VEGF)玻璃体内注射,但这种方法与威胁视力的并发症相关。在此背景下,血管生成抑制剂尼达尼布(nintedanib)和强效抗氧化剂叶黄素(lutein)可以通过多种非共价相互作用共同组装成纳米颗粒。有趣的是,苏州大学功能纳米与软物质研究院陈倩教授发现共同组装的叶黄素/尼达尼布纳米颗粒(L/N NPs)在小鼠体内显示出显著改善的稳定性,并实现了至少两个月的长期持续药物释放。更有趣的是,在具有更完整屏障系统的兔眼球中,L/N NPs仍然能够成功分布在视网膜和脉络膜中长达一个月。在激光诱导的小鼠脉络膜新生血管(CNV)模型中,通过微创的结膜下给药,L/N NPs能够成功抑制血管生成、慢性炎症,并清除氧化应激,其治疗效果与标准的抗VEGF玻璃体内注射相当甚至更好。因此,具有长期持续药物释放行为的结膜下注射L/N NPs代表了一种有前景和创新的AMD治疗策略。这种微创给药方式,结合其有效抑制血管生成、减少炎症和对抗氧化应激的能力,对于改善患有这种致残性眼病的患者的治疗结果和生活质量具有巨大潜力。该研究以题为“Emerging Co-Assembled and Sustained Released Natural Medicinal Nanoparticles for Multi-target Therapy of Choroidal Neovascularization”的论文发表在《Advanced Materials》上。

图1展示了一种新型的共组装叶黄素/尼达尼布纳米颗粒(L/N NPs)的示意图,这种纳米颗粒通过微创的结膜下注射方式,实现了对药物的长期持续释放,有效分布在脉络膜中。这些纳米颗粒具有抗血管生成、抗氧化、抗纤维化和抗炎的多重治疗作用,能够在激光诱导的小鼠脉络膜新生血管(CNV)模型中显著抑制CNV的发展,恢复视觉功能,并减少促炎和促血管生成因子的分泌。研究结果表明,L/N NPs在治疗湿性年龄相关性黄斑变性(AMD)方面展现出了与标准抗VEGF玻璃体内注射相当的治疗效果,甚至在某些方面表现更好,为AMD的治疗提供了一种有前景的创新策略。
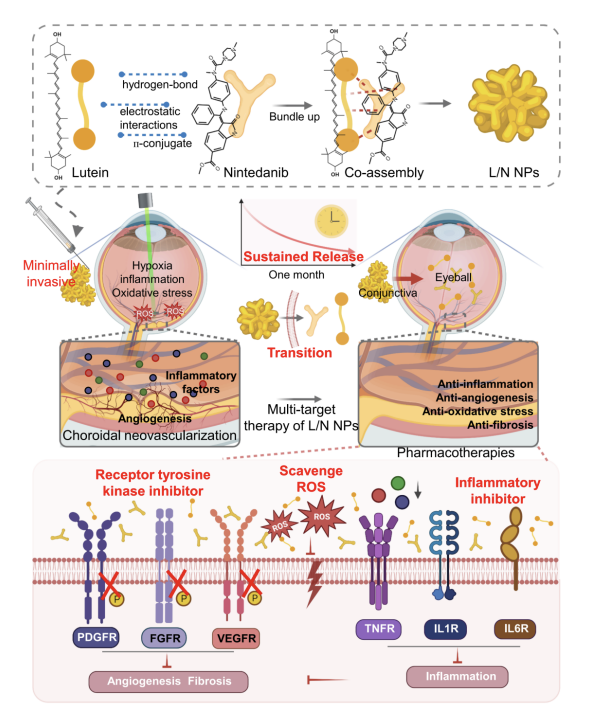
图1. 共组装L/N NPs的长期持续释放用于CNV的多靶点治疗示意图
【共组装L/N NPs的特性分析】
图2详细展示了共组装的叶黄素/尼达尼布纳米颗粒(L/N NPs)的制备和特性。通过改变叶黄素和尼达尼布的摩尔比例,研究者们观察到L/N NPs的尺寸分布、药物释放行为、形态以及稳定性。结果显示,当叶黄素和尼达尼布的比例为1:1时,纳米颗粒显示出最佳的尺寸分布和稳定性。此外,L/N NPs在体外释放实验中表现出长达两个月的药物释放能力,且在小鼠和兔子模型中,这些纳米颗粒能够在眼内持续释放药物至少一个月。这些发现证实了L/N NPs作为一种新型药物递送系统,在AMD治疗中具有潜在的应用价值,能够实现药物的长期稳定释放,同时保持良好的生物相容性和治疗效果。
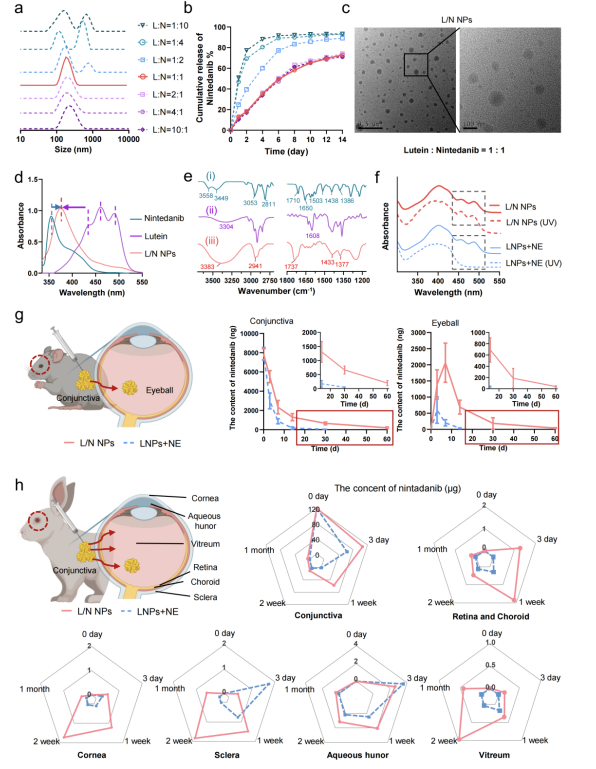
图2. 共组装L/N NPs的特性分析
【L/N NPs在眼内的生物相容性评估】
图3探讨了AHF对细胞凋亡和迁移的影响。研究首先构建了一个由过氧化氢(H2O2)诱导的角质形成细胞(HEK-a)氧化损伤模型,然后通过Annexin V-FITC/PI共染色系统评估了AHF在保护细胞免受凋亡和恢复伤口再上皮化能力方面的效果。流式细胞术定量检测结果显示,AHF处理组的凋亡细胞比例显著降低,细胞活力测试也显示AHF处理后细胞活力显著提高。此外,通过共聚焦激光扫描显微镜和流式细胞术检测细胞内ROS水平,发现AHF显著降低了H2O2诱导的氧化损伤后细胞内的ROS水平。在细胞迁移方面,使用小鼠成纤维细胞(L929细胞)建立了细胞划痕愈合模型,观察了AHF对细胞迁移的影响。结果显示,AHF显著促进了L929细胞的迁移能力,即使在高氧化应激条件下。这些结果表明,AHF能够有效抑制细胞凋亡,促进细胞迁移,从而在体外促进细胞增殖和迁移。
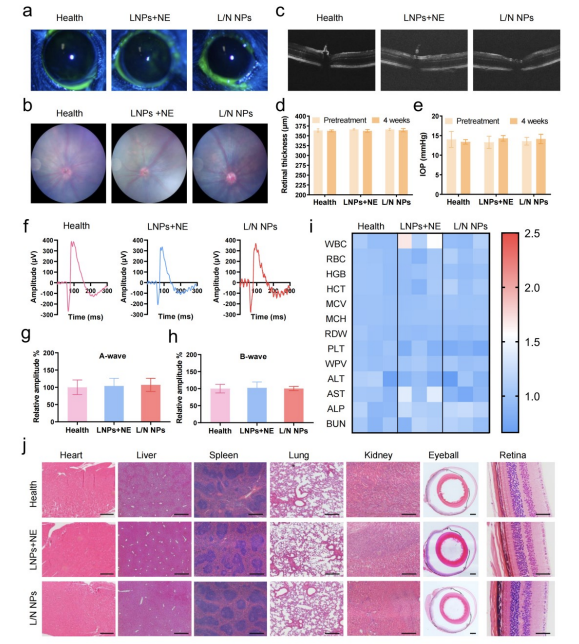
图3.L/N NPs在眼内的生物相容性评估
【L/N NPs的多靶点治疗效果】
图4展示了共组装叶黄素/尼达尼布纳米颗粒(L/N NPs)在多靶点治疗效应方面的研究。通过一系列实验,包括划痕实验、Transwell迁移实验和Matrigel®三维凝胶中的管状结构形成实验,研究者们评估了L/N NPs对人类脐静脉内皮细胞(HUVECs)的增殖、迁移和血管生成活性的影响。结果表明,L/N NPs能够有效抑制HUVECs的增殖和迁移,显著减少管状结构的形成,这表明L/N NPs具有显著的抗血管生成能力。此外,L/N NPs还显示出抗纤维化和抗氧化的特性,能够有效减轻氧化应激和炎症反应,这些特性对于AMD的治疗尤为重要。综合这些发现,L/N NPs作为一种多靶点治疗策略,展现出了在治疗脉络膜新生血管(CNV)方面的潜力,为AMD的治疗提供了新的希望。
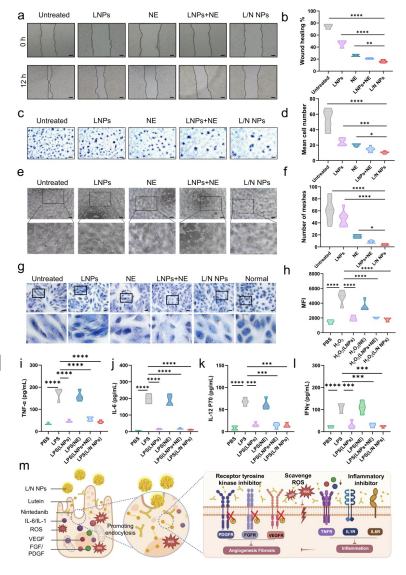
图4. L/N NPs的多靶点治疗效果
【L/N NPs治疗激光诱导CNV的疗效评估】
图5通过激光诱导的脉络膜新生血管(CNV)小鼠模型,评估了共组装叶黄素/尼达尼布纳米颗粒(L/N NPs)的治疗效果。实验中,小鼠被随机分为不同治疗组,包括未治疗组、LNPs组、NE组、L/N NPs组和抗VEGFA组(作为对照)。通过荧光素血管造影(FFA)和光学相干断层扫描(OCT)等技术,研究者们监测了不同治疗后CNV的血管渗漏、厚度变化以及视网膜功能。结果显示,L/N NPs治疗组在减少CNV血管渗漏和厚度方面表现出显著效果,与抗VEGFA组相比,治疗效果相当甚至更好。此外,L/N NPs治疗还改善了小鼠的视觉功能,减少了促炎和促血管生成因子的分泌。病理分析进一步证实了L/N NPs在减轻CNV症状和促进视网膜健康方面的有效性。这些结果表明,L/N NPs作为一种微创给药方式,通过持续释放药物,能够有效抑制CNV的发展,为AMD的治疗提供了一种有前景的新策略。
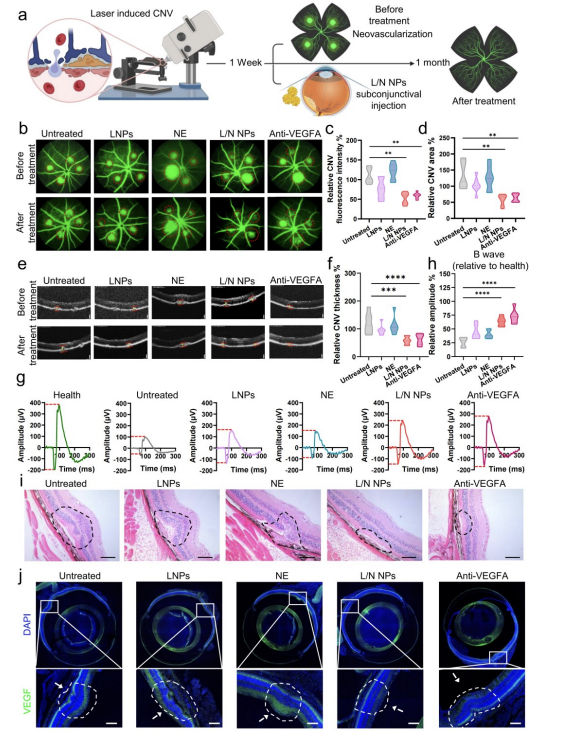
图5. L/N NPs治疗激光诱导CNV的疗效评估
【小结】
该论文的结论是,共组装的叶黄素/尼达尼布纳米颗粒(L/N NPs)通过微创的结膜下注射方式,展现出了显著的稳定性和长期持续的药物释放能力。这些纳米颗粒在小鼠和兔子模型中成功地分布在眼内,特别是在脉络膜中,持续时间至少达到一个月。L/N NPs在激光诱导的小鼠脉络膜新生血管(CNV)模型中,能够有效抑制血管生成、纤维化、炎症反应,并清除氧化应激,取得了与标准抗VEGF玻璃体内注射相当甚至更好的治疗效果。这些发现表明,L/N NPs作为一种新型的药物递送系统,具有改善AMD患者治疗结果和生活质量的巨大潜力,为AMD的治疗提供了一种有前景的创新策略。
原文链接:
https://doi.org/10.1002/adma.202314095
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#AMD# #叶黄素# #尼达尼布纳米颗粒#
90