Am. J. Hematol:CAR T细胞治疗在复发原发性中枢神经系统淋巴瘤患者中显示出较高的长期缓解率
2024-04-14 daikun MedSci原创 发表于上海
该研究旨在通过对更大样本量的患者进行更长时间的随访,以更好地评估CAR T细胞在原发性中枢神经系统淋巴瘤(PCNSL)治疗中的价值,CAR T细胞治疗表现出较高的完全缓解率和长期缓解率。
原发性中枢神经系统淋巴瘤(PCNSL)的预后较差,特别是复发或难治性的患者,中位生存期仅为6.8个月,尽管高剂量化疗联合自体干细胞移植(ASCT)对部分患者有挽救治疗作用,但实际接受ASCT的患者比例较低,整体生存率不高,在系统性大B细胞淋巴瘤治疗中,CAR T细胞疗法表现出良好的效果,能诱导约40-50%的患者获得长期缓解,然而,在PCNSL治疗中,由于免疫细胞相关神经毒性综合征(ICANS)的风险,目前应用有限,目前关于CAR T细胞治疗PCNSL的研究样本量较小,随访时间短,且缺乏与其他治疗方案的比较,因此,该文旨在通过对更大样本量的患者进行更长时间的随访,以更好地评估CAR T细胞在PCNSL治疗中的价值。

方法
研究对象包括27例在2020年至2023年间接受白细胞分离并准备接受CAR T细胞治疗的复发或难治性PCNSL患者,以及247例作为对照的同样难治性PCNSL患者,但未接受CAR T细胞治疗,研究的主要终点是白细胞分离后的无进展生存期(PFS)、总生存期(OS)和CAR T细胞输注后的无复发生存期(RFS)。
研究结果
缓解情况:CAR T细胞治疗后的1个月,76%的患者达到客观缓解,包括32%完全缓解和44%部分缓解,随访中,64%的患者达到最佳完全缓解。CAR T细胞组的中位PFS显著长于对照组(8.4个月 vs 3个月,p<0.001)和中位OS显著长于对照组(21.2个月 vs 4.7个月,p<0.001)。根据CAR T细胞治疗后的最佳反应,比较了不同反应状态患者的RFS曲线,结果显示,达到完全或部分缓解的患者1年RFS为79%,而未达到缓解的患者为0%,两组差异显著(p<0.001);根据CAR T细胞治疗前患者的肿瘤状态,比较了不同状态患者的RFS曲线,结果显示,在完全或部分缓解状态下接受CAR T细胞治疗的患者1年RFS为79%,而在疾病稳定或进展状态下接受治疗的患者为24%,两组差异显著(p=0.02)。
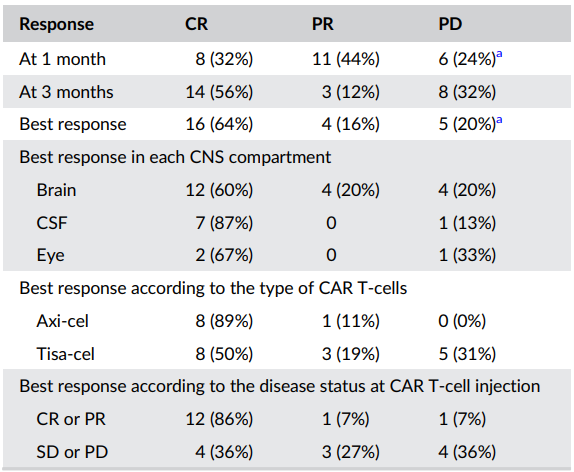


安全性
92%的患者出现了细胞因子释放综合征,其中2例为3-4级,68%的患者出现了神经毒性,包括17例(68%)接受axi-cel治疗的患者和9例(56%)接受tisa-cel治疗的患者,其中有5例(20%)出现3级或更高级别的神经毒性,神经毒性通常在CAR T细胞输注后5天出现,而细胞因子释放综合征通常在输注后1天出现,细胞因子释放综合征的中位解决时间为4天,而神经毒性的中位解决时间为6天,3例患者出现了4级神经毒性,其中1例死亡,1例在6个月后完全恢复,1例在9个月后仍在恢复中,36%的患者出现了3级或更高级别的血液学毒性,持续超过28天,36%的患者在CAR T细胞输注后一个月内需要入住ICU。
结论
CAR T细胞治疗在复发或难治性原发性中枢神经系统淋巴瘤患者中,表现出较高的完全缓解率和长期缓解率,在该文章中,约46%的患者获得了长期缓解,优于其他治疗方案,对于CAR T细胞治疗,获得反应前保持最佳缓解状态对预后至关重要,在完全或部分缓解状态下接受CAR T细胞治疗的患者预后较好。毒性反应方面,细胞因子释放综合征和神经毒性是最常见的,大多数为轻度,但有一定比例的严重毒性,因此,密切监测和处理毒性反应是必要的。CAR T细胞治疗在原发性中枢神经系统淋巴瘤患者中的有效性令人鼓舞,但其长期生存率和安全性仍需要更多前瞻性随机对照试验来进一步证实,综合来看,CAR T细胞治疗为复发或难治性PCNSL患者提供了新的治疗选择,特别是对于那些对常规治疗无效的患者。
原始出处
Choquet S, Soussain C, Azar N, et al. CAR T-cell therapy induces a high rate of prolonged remission in relapsed primary CNS lymphoma: Real-life results of the LOC network. Am J Hematol. 2024; 1-10. doi:10.1002/ajh.27316.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#原发性中枢神经系统淋巴瘤# #CAR-T细胞治疗#
83