JCO:恒瑞医药ADC药物SHR-A1811治疗HER2表达或突变实体瘤,76.3%客观缓解率!
2024-06-23 MedSci原创 MedSci原创 发表于威斯康星
靶向HER2的抗体药物偶联物(ADC)SHR-A1811治疗人表皮生长因子受体2(HER2)表达或突变晚期实体瘤的I期研究结果。
恒瑞医药子公司苏州盛迪亚有限公司的ADC创新药、注射用SHR-A1811被国家药品监督管理局药品审评中心第6次纳入突破性治疗品种,包括HER2低表达的复发或转移性乳腺癌,HER2阳性的复发或转移性乳腺癌,既往含铂化疗失败的HER2突变的晚期非小细胞肺癌,既往经奥沙利铂、氟尿嘧啶和伊立替康治疗失败、HER2阳性结直肠癌,以及既往至少一线抗HER2治疗失败的HER2阳性晚期胃癌或胃食管结合部腺癌、用于既往接受过一种或一种以上治疗方案的HER2阳性不可切除或转移性胆道癌。
注射用SHR-A1811是自主研发的、以HER2为靶点的抗体药物偶联物(ADC)。可通过与HER2表达的肿瘤细胞结合并内吞,在肿瘤细胞溶酶体内通过蛋白酶剪切释放毒素,诱导细胞周期阻滞从而诱导肿瘤细胞凋亡。SHR-A1811的设计理念是希望在维持Enhertu(DS-8201a)卓越疗效的同时,能进一步“减毒”:①增强毒素结合连接子的稳定性以避免毒素的不受控释放。②尽量不改变对拓扑异构酶I的抑制程度,尤其避免大幅提高其抑制活性。③较大程度地提升毒素的渗透性(PAMPA),以增强旁观杀伤。④在能较大程度提高渗透性的前提下,尽量选择亲水性高的毒素以匹配可能的高DAR值选项。⑤在保证疗效的前提下,尽量采用较低DAR值,减少毒素进入人体内的总量。
2024年6月20日,《临床肿瘤学杂志》(Journal of Clinical Oncology)公布了靶向HER2的抗体药物偶联物(ADC)SHR-A1811治疗人表皮生长因子受体2(HER2)表达或突变晚期实体瘤的I期研究结果。
在这项全球性、多中心、首次人体I期临床试验中,旨在评估SHR-A1811在重度预处理的HER2表达或突变晚期实体瘤中的安全性、耐受性、抗肿瘤活性和药代动力学。入组患者接受了SHR-A1811以1.0至8.0 mg/kg的剂量静脉注射,每3周1次。试验的主要终点是剂量限制性毒性、安全性和推荐的II期剂量。
在2020年9月7日到2023年2月27日期间,307例患者接受了SHR-A1811治疗,这些患者之前接受过中位数为3种的转移性治疗方案。
研究结果显示,在接受SHR-A1811治疗的所有患者中,客观缓解率(ORR)为59.9%(184/307)。在HER2阳性乳腺癌患者中,ORR为76.3%(90/118);在HER2低表达乳腺癌患者中,ORR为60.4%(55/91);在98例非乳腺肿瘤患者中,ORR为45.9%(39/85)。
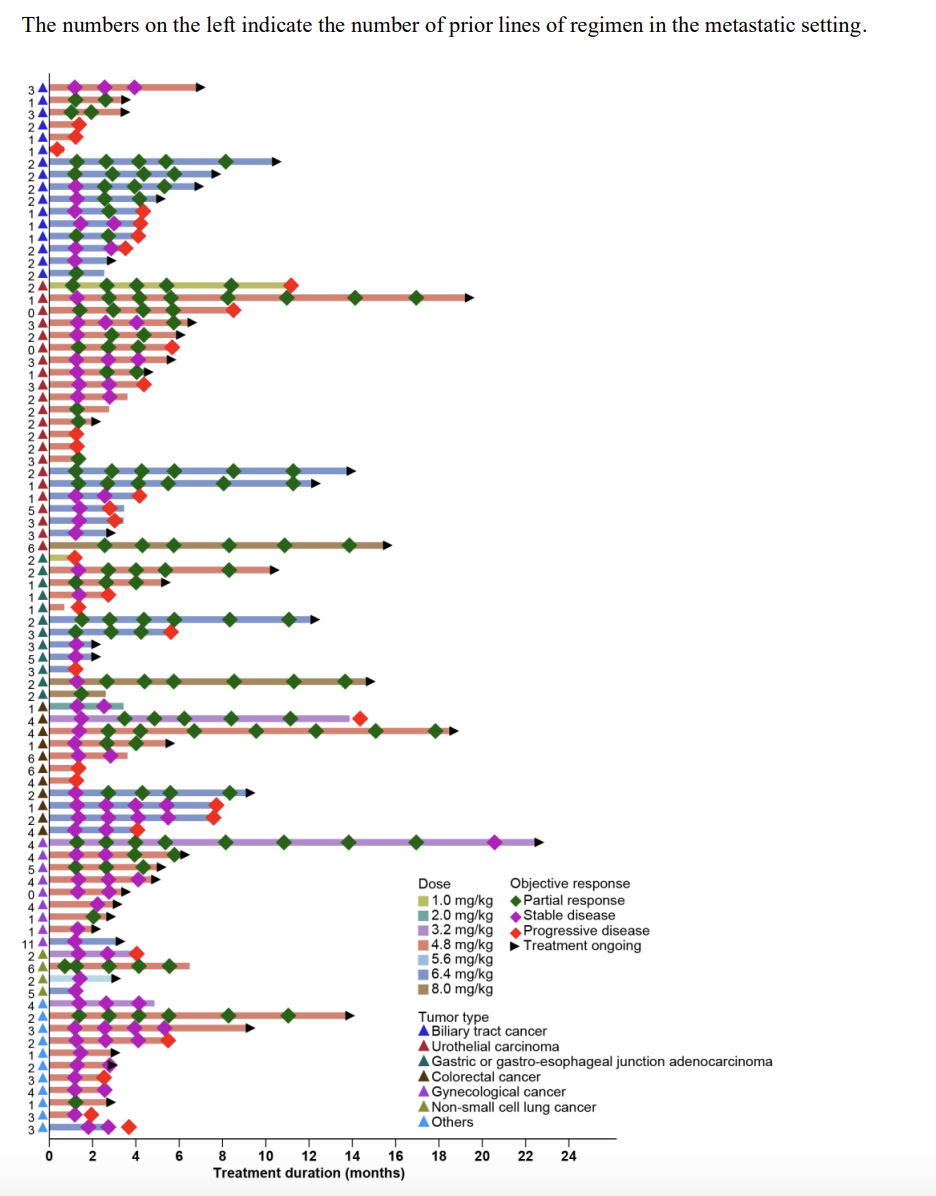
截止为2023年2月28日,6.4 mg/kg组中有1例患者出现剂量限制性毒性(全细胞减少症和结肠炎)。最常见的3级或以上不良事件(AE)包括中性粒细胞计数下降(38.8%)和白细胞计数下降(22.8%)。只有8例(2.6%)患者发生间质性肺病。
小结
SHR-A1811在重度预处理的晚期实体瘤中表现出可接受的耐受性、有希望的抗肿瘤活性和良好的药代动力学特征。针对不同的肿瘤类型,推荐的II期剂量为4.8或6.4 mg/kg。
原始出处:
Safety, Efficacy, and Pharmacokinetics of SHR-A1811, a Human Epidermal Growth Factor Receptor 2-Directed Antibody-Drug Conjugate, in Human Epidermal Growth Factor Receptor 2-Expressing or Mutated Advanced Solid Tumors: A Global Phase I Trial,J Clin Oncol . 2024 Jun 20:JCO2302044. doi: 10.1200/JCO.23.02044
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#乳腺癌# #胆道癌# #ADC药物# #SHR-A1811#
39