CSCO:聚盛会,谱新篇——专家共话胃癌腹膜转移治疗进展及实践
2017-09-27 周爱萍 中国医学论坛报
近年来,腹膜转移作为转移性胃癌的治疗热点和难点问题在临床治疗中备受关注。2017年5 月,《胃癌腹膜转移防治中国专家共识》的刊发,规范了胃癌腹膜转移的诊断、分期、预防和治疗,对此类患者的规范诊治起到了有益的指导和帮助作用。2017年9月26日中国临床肿瘤学会(CSCO)年会召开期间,S-1(爱斯万?)卫星会同期顺利召开。邀请中山大学附属肿瘤医院徐瑞华教授、周志伟教授担任主席,北京大学肿瘤医院张小田
集结专家力量,推动胃癌腹膜转移诊疗规范化进程
胃癌是严重威胁人类健康的一种恶性疾病,全球胃癌每年新增95万例,其中中国患者就占了将近一半。腹膜转移是晚期胃癌患者死亡的首要原因之一,将近20%的胃癌患者在术前或术中诊断中有腹膜转移,超过50%的T3/4期患者在根治性切除术后发生腹膜转移,且腹膜转移患者预后极差。
为了规范胃癌腹膜转移的诊断和治疗,制定合理有效的多学科综合治疗方案,中国抗癌协会胃癌专业委员会组织国内胃癌领域权威专家制定了《胃癌腹膜转移防治中国专家共识》(以下简称“共识”)。本共识以循证证据及临床现实为基础,以综合国内胃癌领域专家认知为原则而撰写,对临床实践具有重要的指导意义。
本共识主要涉及以下5方面内容:
发生机制
胃癌腹膜转移的发生机制尚不完全明确,“种子土壤”学说是目前认可度较高的发生机制理论。
诊断与分期
影像学诊断胃癌腹膜转移难度较大,推荐CT作为胃癌腹膜转移的主要检查手段;诊断性腹腔镜检查是有创检查,适用于进展期胃癌的治疗前诊断、术前治疗后的疗效评价;腹腔游离癌细胞检查主要采用腹水或腹腔灌洗液细胞学检查,阳性结果可作为Ⅳ期胃癌的独立诊断标准;血清标志物的敏感性与阳性预测值较差,仅作为辅助诊断。结合我国目前现状,推荐采用日本胃癌学会制定的腹膜转移分期标准(PX:有无腹膜转移不明者;P0:无腹膜转移;P1:有腹膜转移)。
胃癌腹膜转移的风险因素包括TNM 分期T3/4 及N+、淋巴结外浸润、Borrmann分型Ⅲ/Ⅳ以及Lauren分型弥漫型,其预防措施除外科无瘤技术及预防性腹腔热灌注化疗外,口服氟尿嘧啶类药物[替吉奥(S-1)]单药或联合奥沙利铂的术后辅助化疗是降低术后复发和转移的有效手段。ACTS-GC研究5年结果证实,S-1术后辅助化疗较单纯手术显着降低了患者5年死亡风险[5 年总生存率(OS)分别为71.7%和61.1%,风险比(HR)=0.669,95%可信区间(CI),0.540~0.828],腹膜转移发生风险降低31%。G-SOX研究证实,S-1+奥沙利铂(SOX)方案一线治疗晚期胃癌腹膜转移患者获益更大。目前,S-1+奥沙利铂(SOX)方案是最受关注的胃癌围手术期化疗方案,有多项相关研究正在进展过程中。
治疗
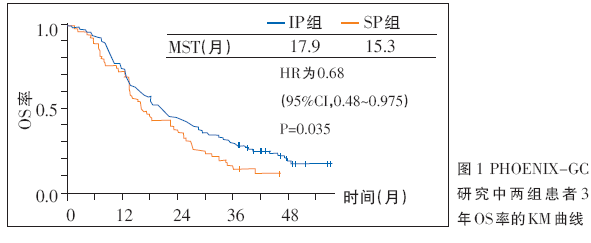
全身系统化疗是晚期胃癌的一种有效治疗方式,优于最佳支持治疗。腹腔灌注化疗(IP)可以提高局部药物浓度,降低全身副反应,由于腹膜转移是全身系统性疾病的局部反应,因此全身系统化疗仍为核心方案,腹腔灌注化疗为补充。2016年美国临床肿瘤学会(ASCO)年会报告的PHOENIX-GC研究,是全球唯一治疗胃癌腹膜转移有效的Ⅲ期研究,其结果显示,在全分析集(FAS)人群中,SP(S-1+顺铂)组和IP[紫杉醇(PTX)腹腔灌注联合S-1+PTX全身化疗]组的OS未见显着统计学差异(P=0.080)。但在符合方案集(PPS)中,则显示出统计学差异(P=0.022),特别是在中量腹水的患者中,两组的差异明显(13.0个月对6.8个月,HR=0.38)。在校正患者腹水量等不平衡因素后,FAS人群的OS 在SP 组显着优于IP 组(HR=0.59,P=0.0079)。对患者继续随访,进一步分析显示,在FAS 人群、PPS 人群以及校正后的FAS人群中,IP组的3年OS率显着优于SP组(图1),确证了IP方案控制腹水对腹膜转移患者预后的意义。
并发症的处理
当胃癌腹膜转移患者出现癌性腹水和肠梗阻等并发症时,患者生活质量及预后较差。针对并发症,目前治疗手段包括对症治疗和抗肿瘤治疗。总之,腹膜转移一直以来是胃癌治疗的难点,《胃癌腹膜转移防治中国专家共识》的出台对国内胃癌腹膜转移的预防和规范诊治可以起到有益的指导和帮助作用。希望广大临床工作者能够在疾病早期关注高危患者,有效预防腹膜转移的发生,对于已发生腹膜转移的患者做到及早发现,通过多学科综合诊治方案,提高疗效,延长生存并改善生活质量。
晚期胃癌转化治疗的新希望
全身系统化疗是Ⅳ期胃癌患者的主要治疗手段,但目前,虽然患者化疗缓解率较高,但中位生存期(MST)徘徊在13~15个月左右,并且由于患者耐药或毒性反应,化疗不能持续长期进行。姑息性手术也是可供选择的治疗方案之一,但其对于改善患者生存的作用仍然存在争议。REGATTA研究显示,对于伴有单一不可治愈因素的晚期胃癌患者(腹膜转移者占75%),直接手术贯序化疗与单纯化疗相比并无明显生存获益。
近年来,随着晚期结直肠癌转化治疗、外科准确病期评估及有效药物应用的发展,转移性胃癌治疗外科手术原则,已从单纯切除原发病灶转变为“根治性”切除原发病灶及所有转移病灶,从而延长患者生存期乃至治愈部分患者。因此,对于晚期胃癌,随着新型化疗药物的应用及化疗方案的优化,包括新辅助化疗、转化治疗及围手术期化疗在内的联合化疗受到越来越多的关注。
新辅助化疗是通过术前化疗,使可切除患者的肿瘤降期并抑制微转移;转化治疗是指不可切除患者在化疗有效后,实施R0手术切除肿瘤,而围手术期化疗是指在手术前后实施的化学治疗。
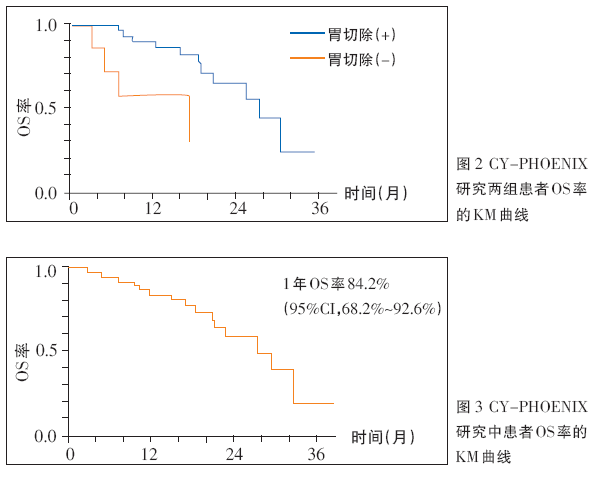
日本JCOG0405研究显示,采用S-1联合顺铂新辅助化疗方案,患者5年生存率超过50%,R0切除患者3年和5年无复发生存率均为50%。CY-PHOENIX研究显示,IP(PTX腹腔灌注联合S-1+PTX全身化疗)方案化疗后胃切除(+)患者的OS率显着高于胃切除(-)患者(图2),患者1年OS率为84.2%(95%CI,68.2%~92.6%)(图3),36例(94.7%)患者IP方案治疗后发生了腹水转阴。2017 ASCO年会报道的FLOT-4研究提示了围手术期化疗的重要作用。2017年美国医学会杂志(JAMA)报道的FLOT-3研究表明,在一定范围内的胃/胃食管结合部腺癌患者,新辅助化疗后手术切除,手术患者与未手术患者的OS分别为31.1个月和15.9个月,患者获得明显生存获益。越来越多的研究表明,药物转化治疗已在亚洲人群中取得初步进展。
术前新辅助腹腔与全身联合化疗(NIPS)策略最早由日本研究团队报道,系针对晚期胃癌腹膜转移的转化治疗方法。多项研究已证实,NIPS+手术是一种有效的治疗方式。在我国,上海交通大学医学院附属瑞金医院牵头开展的腹膜转移晚期胃癌患者的Ⅲ期多中心NIPS研究正在进展过程中,患者将以2︰1 的比例,随机进入NIPS组(PTX腹腔灌注联合S-1+PTX全身化疗)及PS组(S-1+PTX全身化疗)接受治疗,期待其提供进一步的有效证据。
目前,NIPS等转化治疗还在探索中,针对晚期胃癌的转化治疗还有很多问题有待进一步探索及验证,期待在未来,中国参与在内的FACO 国际多中心研究及FLOT-5研究能够为胃癌转化治疗提供更多更充分的循证依据。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#胃癌腹膜转移#
90
#转移治疗#
81
对课题有借鉴价值.马克下
81
#腹膜转移#
82
#腹膜#
70
不错.学习!
82
谢谢分享.学习了.谢谢
87