GUT:许正平/盛静浩团队发现血管生成素可维持肠道菌群稳态阻止肠炎发生
2020-09-03 BW Bio生物世界
肠道菌群是指定植于人体消化道内的所有细菌。虽然我们常常忽略肠道菌群的存在,但实际上它们对机体健康起到了非常重要的作用。肠道菌群是一个多元化和充满活力的细菌群落。
近日,浙江大学医学院、良渚实验室(系统医学与精准诊治浙江省实验室)许正平/盛静浩课题组在国际胃肠病领域顶尖学术期刊 GUT 杂志在线发表了题为:Angiogenin Maintains Gut Microbe Homeostasis by Balancing α-Proteobacteria and Lachnospiraceae 的研究论文。
该研究利用临床样本、血管生成素(angiogenin,ANG)基因缺失小鼠和多种肠炎模型证明肠道分泌的ANG通过差异调控α变形菌纲(α-Proteobacteria)和毛螺菌科(Lachnospiraceae)的生长而维持肠道微生态平衡;Ang1缺失导致肠道菌群紊乱,促进小鼠肠炎进展。
“绿色癌症”—炎症性肠病已成为我国消化道常见疾病
生活中每个人都有过肚子疼、拉肚子、没有食欲等类似经历,让人真切体会到肠道不适的感受,并希望拥有一个健康肠道。不幸的是,一种叫炎症性肠病(inflammatory bowel disease,IBD)的消化道疾病发病率在我国正逐年提高,它的特征是消化道慢性炎症,临床表现为反复发作的腹泻、腹痛、便血等,而且随着病情的逐步进展,IBD 患者会出现消化道的结构和功能障碍,严重损害患者及其家属的生活质量,被称为“绿色癌症”。
目前认为,遗传易感基因和多种环境因子共同导致了IBD的发生,但具体发病机制仍不明了。为深入了解IBD的发病机制,寻找IBD的预防、诊断和有效治疗途径,各国研究人员正从多个角度进行探索,已有许多研究证明肠道菌群在IBD发生发展中起到重要作用。
肠道菌群稳态是维持肠道健康的重要因素
肠道菌群是指定植于人体消化道内的所有细菌。虽然我们常常忽略肠道菌群的存在,但实际上它们对机体健康起到了非常重要的作用。肠道菌群是一个多元化和充满活力的细菌群落,研究显示一个健康成年肠道菌群有1000种以上,总数量多达约4×10E13个,与人体细胞数量相当。
种类繁多的肠道菌群组成一个庞大而复杂的微生态系统,具有帮助消化、促进肠道细胞分化、保护宿主免受病原体侵染、刺激和调节免疫系统等诸多功能,被认为是一个“隐藏的器官”。但是,在内外因素的影响下,肠道菌群可能出现结构和/或功能失调,紊乱的肠道菌群会诱发多种疾病。
抗菌肽在肠道菌群调节中发挥重要作用
肠道会分泌一类具有抗菌活性的小分子蛋白,即抗菌肽(antimicrobial peptides,AMPs),它们主要是由肠道潘氏细胞和肠上皮细胞分泌,种类繁多,具有广谱的抗细菌、真菌和病毒活性。目前发现的肠道抗菌肽包括防御素家族、组织蛋白酶抑制素、再生胰岛衍生蛋白家族、核糖核酸酶家族、溶菌酶家族等。
临床检测和实验室研究表明,抗菌肽表达异常与IBD的发生发展密切相关。然而,目前对抗菌肽“个性化”的体内抗菌作用缺乏研究,也尚未建立抗菌肽调节的特定菌群与IBD的关联。因此,深入而精细地探索抗菌肽-细菌-IBD的相互作用并阐明其调控机制,可能为IBD的诊治提供新的路径。
血管生成素通过调控肠道菌群稳态抑制IBD的发生
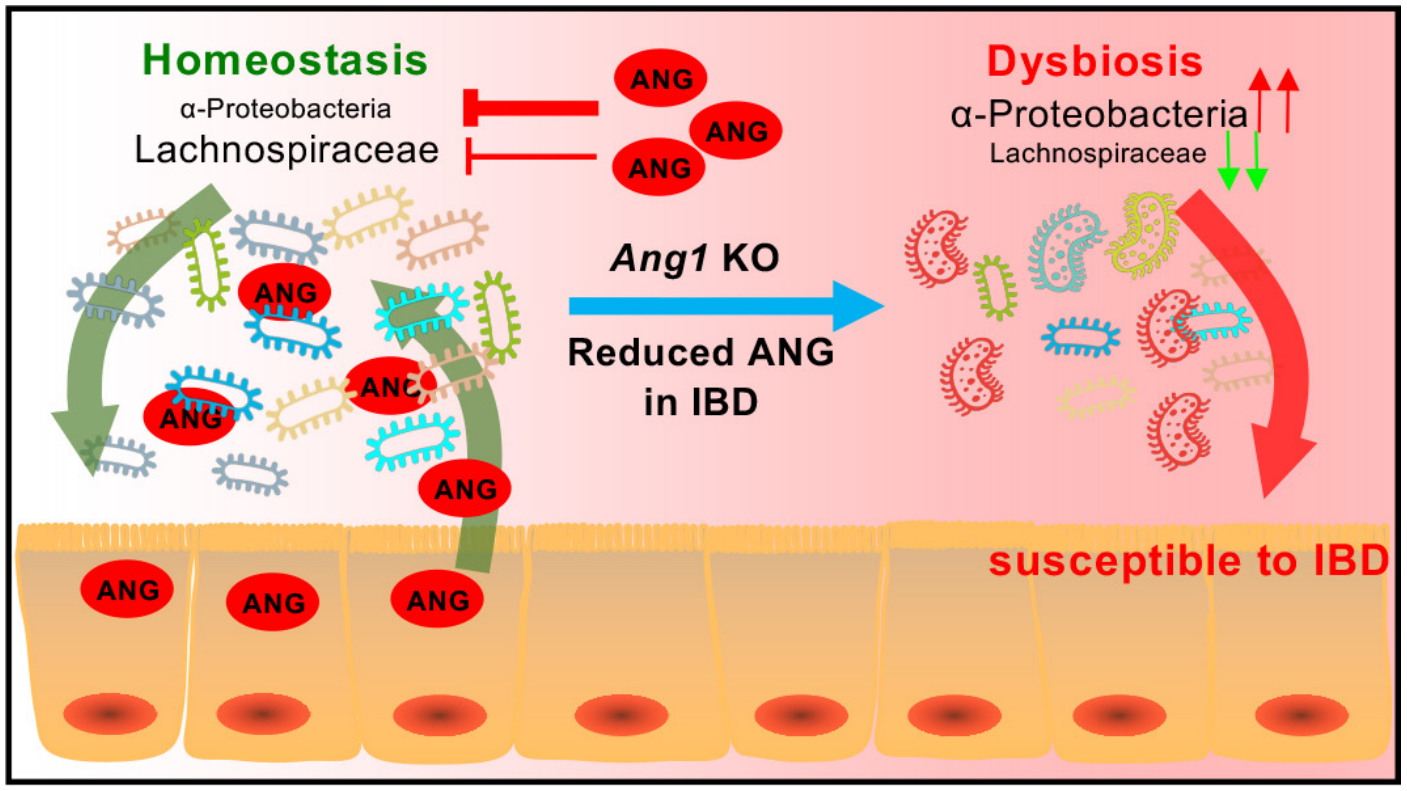
许正平/盛静浩课题组利用临床样本、血管生成素(angiogenin,ANG)基因缺失小鼠和多种肠炎模型证明肠道分泌的ANG通过差异调控α变形菌纲(α-Proteobacteria)和毛螺菌科(Lachnospiraceae)的生长而维持肠道微生态平衡;Ang1缺失导致肠道菌群紊乱,促进小鼠肠炎进展。
该研究团队发现,健康肠道可向肠腔中分泌适量的ANG蛋白,而IBD患者ANG的含量只有约正常人的一半。为了回答ANG分泌不足是否与IBD发生发展相关,他们对Ang1基因缺失小鼠和野生型小鼠进行肠炎诱导,发现Ang1缺失小鼠肠炎症状显着加重。
进一步,他们把Ang1基因缺失小鼠的粪便转移到野生型小鼠肠道中,发现后者的肠炎症状也明显加重,以上证据提示ANG可以通过调节肠道菌群而影响IBD进程。
然后,利用高通量测序技术,他们发现Ang1缺失小鼠肠道菌群变化显着,主要特征为α变形菌纲增多和毛螺菌科减少。更有意义的是,他们通过细菌培养与鉴定技术,筛选到了受ANG调控的菌种,分别为属于α变形菌纲的缺陷短波单胞菌(B. diminuta)和少动鞘氨醇单胞菌(S. paucimobilis),属于毛螺菌科的Anaerostipes sp.和Blautia sp.,并且在小鼠模型上证实前者具有促进肠炎的作用,而后者恰恰相反,可以抑制肠炎发生。
以上结果提示这些差异菌种可作为临床诊断IBD的指标,且两个毛螺菌科菌株具有预防或治疗IBD的潜能,将来可能开发为应用于临床的益生菌制剂。
接着,该团队揭示了ANG调控肠道菌群的机制。通过体外抗菌实验和扫描电镜等手段,他们发现ANG能选择性地结合并有效杀伤α变形菌纲;进一步体外细菌培养实验显示,α变形菌纲菌种与毛螺菌科菌种存在着相互抑制作用,解释了为什么ANG在能抑制α变形菌纲的同时可以促进毛螺菌科的生长。
最后,研究团都探索了ANG调节肠道菌群及减轻IBD的可行性。通过给Ang1缺失小鼠消化道补充重组ANG1蛋白,小鼠肠道菌群紊乱得到有效回复,肠炎症状也明显减轻。这为ANG的临床转化应用提供了实验证据的支持。
据悉,浙江大学医学院、良渚实验室(系统医学与精准诊治浙江省实验室)许正平教授和盛静浩讲师为该论文的共同通讯作者。浙江大学医学院博士研究生孙德森、博士后白荣盘和浙江大学医学院附属邵逸夫医院普外科主任医师周伟为该论文的共同一作。该研究成果得到国家自然科学基金和浙江省自然科学基金经费资助。
原始出处:
Desen Sun, Rongpan Bai, Wei Zhou, et al.Angiogenin maintains gut microbe homeostasis by balancing α-Proteobacteria and Lachnospiraceae.Gut. 2020 Aug 25;gutjnl-2019-320135. doi: 10.1136/gutjnl-2019-320135.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#稳态#
78
#血管生成素#
0
#肠道菌#
63