CAR-T新突破:治疗获益所需细胞量减少5倍,这一蛋白功劳大:Nature子刊
2022-08-17 上海细胞治疗工程技术研究中心 医药魔方Pro
NT-17与靶向CD33的CAR-T疗法联用,在急性髓系白血病模型小鼠体内的研究也获得类似的效果。
在过去的十年中,CAR-T细胞疗法治疗难治性血液系统恶性肿瘤已经变得越来越普遍。尽管取得了这些进展,但也有相当一部分患者经历过CAR-T毒性和持久性不理想的问题,这可能导致肿瘤细胞逃逸和疾病复发。
今年6月,EHA大会上公布的最新数据显示,Caribou Biosciences最初有望用于治疗非霍奇金淋巴瘤的同种异体CAR-T就遭遇了这种命运。由于半数患者复发,该产品持久性受到怀疑。持久性已成为同种异体CAR-T开发商面临的一个行业性问题, Allogene、CRISPR Therapeutics 和 Precision Biosciences均发现大量癌症患者在治疗后的6个月内复发。Caribou已从其抗CD19候选产品CB-010中去除PD-1受体,以减少CAR-T细胞耗竭,并在更长时间内保持高抗肿瘤活性。
6月13日,来自圣路易斯华盛顿大学的研究人员在Nature Communications上发表文章报道,NeoImmuneTech公司长效人类IL-7因子NT-17与CAR-T疗法联用,不仅促进CAR-T细胞增殖,还提高了细胞毒性,减少了耗竭并延长了疗法的持久性。在小鼠体内实验中,两者联用显著提高了CAR-T疗法对急性髓系白血病和B细胞淋巴瘤的疗效,带来长期无瘤生存。

NT-I7(又称efineptakin alfa, rhIL-7-hyFc)是一种与IgD和IgG4元件融合的工程化二聚体IL-7(hyFc:copyright:),可减少补体激活,同时延长体内血清半衰期,为寿命较短的天然重组人IL-7(rhIL-7)提供明显的药理优势。
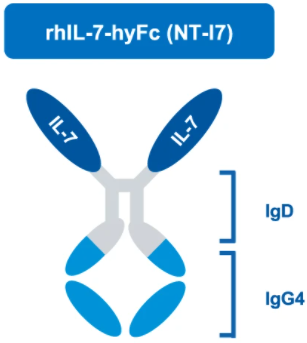
在首次健康志愿者的人体试验 (NCT02860715)中,单剂量肌肉注射NT-I7(60 mcg/kg)导致CD4+ 和CD8+ T细胞数量大幅增加,未报告重大不良事件或剂量限制性毒性。因此,研究人员决定探索这种试剂增强CAR-T细胞活性的潜力。
研究表明,NT-I7可以增强CD19靶向的CAR-T细胞活力,减少其在侵袭性B细胞淋巴瘤模型小鼠体内的耗竭,同时促进它们在CD19+肿瘤细胞存在情况下的扩增。NT-17与CD19靶向CAR-T细胞联用,与单独CAR-T细胞疗法相比,更为显著地缩小了小鼠体内的肿瘤,延长了小鼠的生存期(下图)。
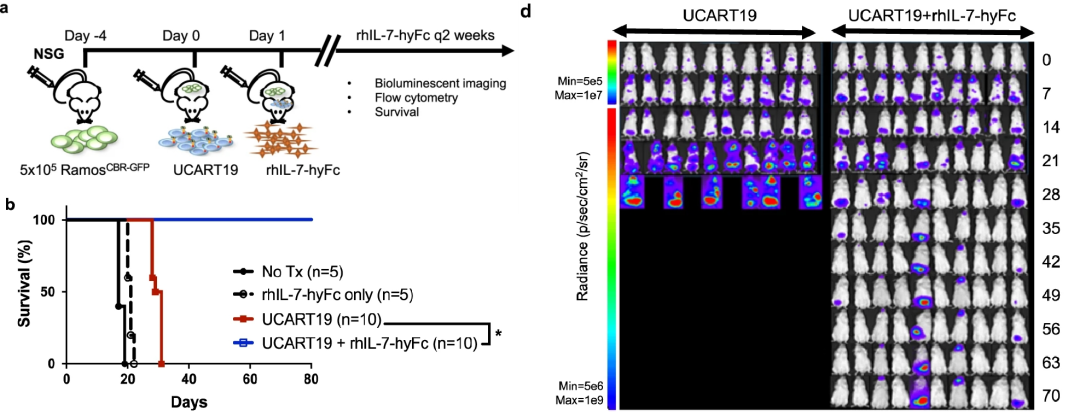
NT-17与靶向CD33的CAR-T疗法联用,在急性髓系白血病模型小鼠体内的研究也获得类似的效果。
此外,NT-17通过提高每个CAR-T细胞的肿瘤杀伤能力和促进其体内扩增,可以减少提供生存获益所需CAR-T细胞疗法的剂量。在小鼠模型中,与NT-17联用,可以将CAR-T疗法的有效剂量降低至少5倍(1.25X106个细胞减少到2.5X105个细胞),而仍能获得相同甚至更强的体内活性,并提高疗法的持久性。
NeoImmuneTech总裁兼首席执行官Se Hwan Yang博士表示:“这些结果表明NT-I7在细胞治疗中具有广泛的适用性,除了作为长效人类IL-7被熟知的益处外,NT-I7还具有扩大T细胞亚群、增强免疫系统和增强在血液瘤和实体瘤患者中抗癌应答的潜力。”
NeoImmuneTech的下一步计划是看NT-17是否能对人类产生类似的效果。
参考资料:
1# Immunity boosting treatment enhances CAR-T cell therapy for blood cancers (来源:Medical press)
2# Miriam Y. Kimet al. A long-acting interleukin-7, rhIL-7-hyFc, enhances CAR T cell expansion, persistence, and anti-tumor activity. Nature Communications. (2022)
3# CAR-T countdown: NeoImmuneTech drug could reduce number of cells needed for cancer therapy fivefold (来源:FIERCE Biotech)
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#新突破#
105
#Nat#
51
#CAR-#
66