JMV:姜世勃/陆路团队研发高效广谱抗冠状病毒疫苗的历程
2022-10-03 上海重大传染病和生物安全研究院 上海重大传染病和生物安全研究院
未来一些SARSr-CoV可能会跨物种传播,对人类健康产生巨大威胁,所以开发高效、广谱的冠状病毒疫苗以抵御目前流行以及将来可能出现的其他冠状病毒都具有重要意义。
2022年9月13日,上海市重大传染病和生物安全研究院双聘PI、复旦大学基础医学院姜世勃/陆路团队在《医学病毒学杂志》(J Med Virol, IF=20.693)( http://doi.org/10.1002/jmv.28143 )发文系统性地回顾了高效广谱抗冠状病毒(Pan-CoV)多肽药物的研发历程,详见报道JMV | 姜世勃/陆路团队研发高效广谱抗冠状病毒多肽药物的历程。
2022年9月25日,姜世勃团队再次在《医学病毒学杂志》(J Med Virol, IF=20.693)(https://doi.org/10.1002/jmv.28172)发文回顾了他们研发高效广谱抗冠状病毒疫苗的历程,并介绍了国际上研发小、中、大广谱抗冠状病毒疫苗的最新进展(周洁博士生和刘泽众青年研究员是本文的第一作者,王茜博士和姜世勃教授是本文的通信作者)。
 冠状病毒分为分为α、β、γ、δ四个属,β属冠状病毒又分为A、B、C、D四个谱系,B谱系病毒又称之为沙贝科病毒(sarbecovirus),包括SARS-CoV,新冠病毒(SARS-CoV-2)及其变异株,以及来源于蝙蝠等动物的SARS相关CoV(SARSr-CoV)。C谱系病毒又称之为玛贝科病毒(merbecovirus),包括MERS-CoV,以及来源于蝙蝠等动物的MERS相关CoV(MERSr-CoV)。冠状病毒的刺头(S)蛋白是介导病毒入侵细胞的重要蛋白(图1)。S蛋白由S1和S2亚单位组成,S1亚单位上的RBD负责病毒与细胞表面受体结合,而S2亚单位主要介导病毒膜与宿主细胞膜或内吞泡膜融合,使得病毒的基因进入细胞内进行复制。由此,S蛋白和RBD是目前冠状病毒疫苗设计的主要靶点。一般来说,开发一个抗病毒疫苗需时十年以上,所需经费超过十亿美元,而成功率不足10%。目前所用的七个抗病毒疫苗的平均开发时间为30年,而艾滋病疫苗的开发时间已经超过40年,但目前看来还是遥遥无期。然而,在一年多的时间内,全世界已经有14款抗新冠病毒的疫苗被多个国家批准紧急或有条件使用。为何新冠疫苗能在一年多时间内研发成功?这是因为冠状病毒有一个致命的疫苗靶点 – 受体结合域(RBD)。任何一个含有冠状病毒RBD的抗原(如病毒颗粒、S蛋白、S1亚单位、RBD片段)都可以在人和动物体内诱生一定程度的中和抗体反应和超过50%对疫苗毒株感染的保护率。
冠状病毒分为分为α、β、γ、δ四个属,β属冠状病毒又分为A、B、C、D四个谱系,B谱系病毒又称之为沙贝科病毒(sarbecovirus),包括SARS-CoV,新冠病毒(SARS-CoV-2)及其变异株,以及来源于蝙蝠等动物的SARS相关CoV(SARSr-CoV)。C谱系病毒又称之为玛贝科病毒(merbecovirus),包括MERS-CoV,以及来源于蝙蝠等动物的MERS相关CoV(MERSr-CoV)。冠状病毒的刺头(S)蛋白是介导病毒入侵细胞的重要蛋白(图1)。S蛋白由S1和S2亚单位组成,S1亚单位上的RBD负责病毒与细胞表面受体结合,而S2亚单位主要介导病毒膜与宿主细胞膜或内吞泡膜融合,使得病毒的基因进入细胞内进行复制。由此,S蛋白和RBD是目前冠状病毒疫苗设计的主要靶点。一般来说,开发一个抗病毒疫苗需时十年以上,所需经费超过十亿美元,而成功率不足10%。目前所用的七个抗病毒疫苗的平均开发时间为30年,而艾滋病疫苗的开发时间已经超过40年,但目前看来还是遥遥无期。然而,在一年多的时间内,全世界已经有14款抗新冠病毒的疫苗被多个国家批准紧急或有条件使用。为何新冠疫苗能在一年多时间内研发成功?这是因为冠状病毒有一个致命的疫苗靶点 – 受体结合域(RBD)。任何一个含有冠状病毒RBD的抗原(如病毒颗粒、S蛋白、S1亚单位、RBD片段)都可以在人和动物体内诱生一定程度的中和抗体反应和超过50%对疫苗毒株感染的保护率。

图 1
所以,针对新冠病毒原始毒株的疫苗研发的成功率很高。但后来发现第一代的新冠疫苗都是“早产儿”,长得“矮短矬”(即低效、短效、窄谱),其中和抗体水平普遍偏低,且在半年后降到更低的水平。随着新冠病毒的全球大流行,变异株不断出现,世界卫生组织(WHO)将一些感染力强,具有免疫逃逸性能的新冠病毒变异株命名为“需要关注的变异株(VOC)”,包括阿尔法(Alpha,B.1.1.7),贝塔(Beta,B.1.351),伽马(Gamma,P.1),德尔塔(Delta,B.1.617.2)和奥密克戎(Omicron,B.1.1.529)。奥密克戎又进一步分为BA.1、BA.2、BA.3、BA.4、BA.5五个亚谱系;BA.2、BA.4和BA.5又形成BA.2.75、BA.4.6、和BF.7等多个进化分支。其中,BA.4/5具有最强的免疫逃逸能力和最强的传播能力,现已成为全球流行的主要变异株亚谱系,而BA.2和BA.5的进化分支—BA.2.75和BF.7有可能成为未来的流行毒株(图2)。有研究表明第一代的新冠疫苗对抗奥密克戎感染的有效保护率均在48%以下,也就是说这些疫苗如果在奥密克戎流行区开展临床试验的话,恐怕没有一个疫苗能获批上市。所以,接种第一代的疫苗虽然能防重症,但不能防感染,也不能防病毒传播。这些变异株的不断出现,产生免疫逃逸现象,对现行的一些抗新冠的疫苗和抗体药物产生形成了严峻的挑战。未来一些SARSr-CoV可能会跨物种传播,对人类健康产生巨大威胁,所以开发高效、广谱的冠状病毒疫苗以抵御目前流行以及将来可能出现的其他冠状病毒都具有重要意义。
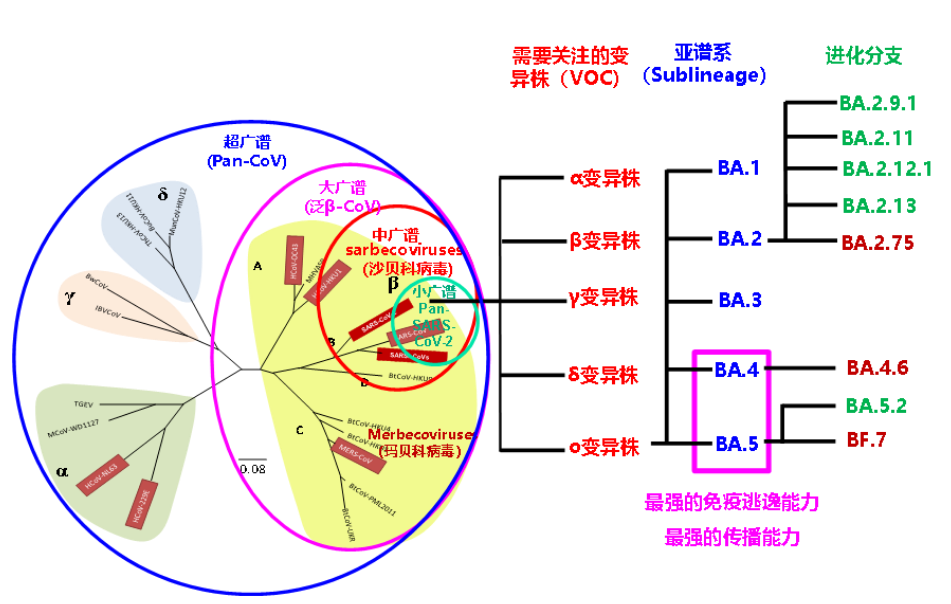
图 2
目前的广谱冠状病毒疫苗可分为小广谱、中广谱、和大广谱(图2)。小广谱疫苗,即新冠病毒通用(Pan-SARS-CoV-2)疫苗,是指广谱抗新冠病毒及其变异株的疫苗。现在很多疫苗开发商正在研发此类疫苗,多采用“以变应变”的策略,即将新变异株(如奥密克戎)的灭活病毒颗粒或刺头(S)蛋白加入到他们先前开发的疫苗中而形成的多价疫苗,还有通过纳米颗粒展示和环状RNA表达的形式开发对多种新冠变异株产生有效保护的新型新冠疫苗。中广谱疫苗,即沙贝科病毒通用疫苗(Pan-Sarbecoviruses,包括SARS-CoV、SARS-CoV-2及其变异株、蝙蝠SARSr-CoV),这是目前急需要开发的疫苗,可用于防控新冠病毒变异株及将来可能新发与再现的SARS样传染病。目前的疫苗平台设计此类中广谱疫苗主要有三种策略(图3/图5):1)通过将来源于不同冠状病毒的抗原展示在一个载体上(例如纳米颗粒)作为抗原,从而产生对多种冠状病毒的免疫保护;2)设计嵌合的S蛋白作为抗原,通过将来自不同冠状病毒的RBD,NTD及其他区域组成嵌合mRNA疫苗,也能对多种沙贝科疫苗产生保护效果;3)通过新型佐剂提高保守的抗原表位的免疫反应从而产生广谱的保护效果。大广谱疫苗,即β属冠状病毒通用疫苗(Pan-β-CoV vaccines),是指广谱抗β属冠状病毒(包括SARS-CoV、MERS-CoV、SARS-CoV-2及其变异株、蝙蝠的SARSr-CoV和MERSr-CoV)疫苗,也是未来需要开发的战略储备疫苗,可用于防控现在流行的β属冠状病毒(如SARS-CoV-2和MERS-CoV)及未来可能出现的β属冠状病毒新变种(如SARS-CoV-3或MERS-CoV-2)引起的SARS样或MERS样传染病。超广谱疫苗,是针对所有七种人冠状病毒的疫苗(Pan-HCoV vaccines)。由于这些病毒使用不同的受体,其S蛋白的RBD的氨基酸序列和结构也差异比较大,所以,超广谱疫苗的开发难度极高。

图 3
在2022年3月25日,世界卫生组织研发蓝图小组(WHO R&D Blueprint )召开紧急会议,向全世界呼吁要尽快地研发广谱抗沙贝科病毒疫苗(Pan-Sarbecovirus vaccine,即中广谱疫苗),防控现在和未来新冠病毒变异株的扩散。姜世勃受邀在本次会议上和2022年8月30日的另一场WHO会议上作了“以不变应万变策略研发冠状病毒通用疫苗和药物”的发言,介绍了他们刚刚发表的有关中广谱疫苗的研发成果(见WHO网站:https://cdn.who.int/media/docs/default-source/blue-print/session-6_shibo-jiang-_preparing-for-future_fudan-university_pathogenx-meeting_aug2022.pdf?sfvrsn=4162ede0_3)。2003年,当SARS-CoV向全世界蔓延之际,姜世勃的团队使用SARS-CoV的S1亚单位(含有RBD和NTD)或RBD加Fc构建了两个亚单位疫苗。他们使用这两个疫苗免疫小鼠和兔子,获得的结果令人吃惊!RBD-Fc疫苗在免疫动物体内诱导的特异性抗体比S1要高出5~25倍,而中和SARS-CoV假病毒和活病毒的抗体效价都在10,000以上,比灭活病毒疫苗和基于S蛋白疫苗的DNA疫苗、腺病毒疫苗及亚单位疫苗诱导的中和抗体效价高出十几到几十倍。他们进一步的研究证明RBD含有S蛋白中主要的中和位点,从感染者或免疫动物血清中分离出来的高效价中和抗体基本上都是针对RBD。他们在国际上发表了第一篇有关RBD疫苗和第一篇RBD靶向的中和抗体的文章,因此而开辟了基于RBD冠状病毒疫苗的新领域,其团队在该领域内一直保持着国际领先的地位(图4)。
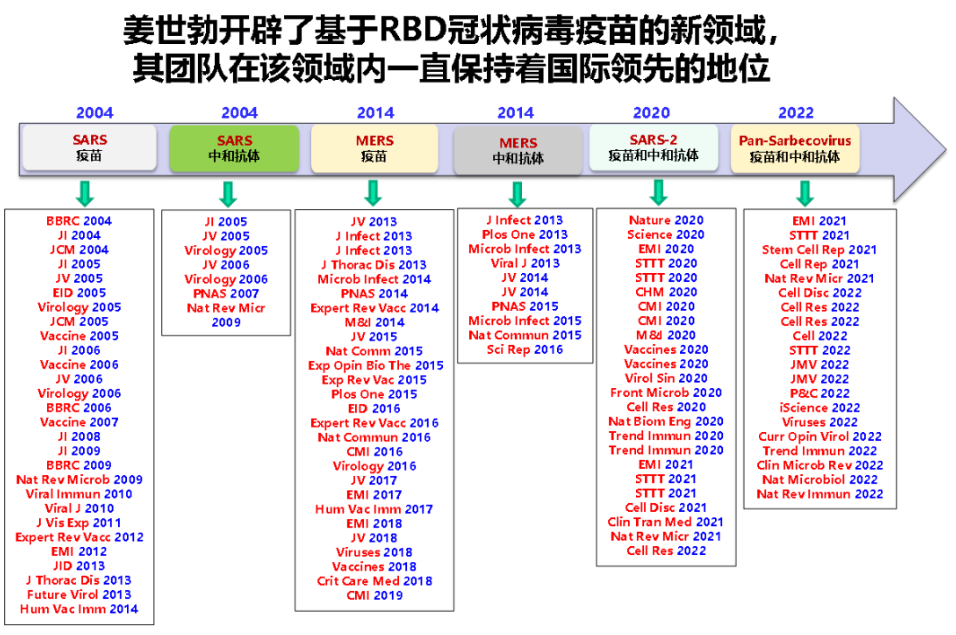
图 4
在2020年初当新冠疫情暴发伊始,姜世勃就在Nature和EMI发文,呼吁要尽快地研发安全、高效、广谱的抗冠状病毒疫苗,以应对未来可能出现的新冠病毒变异。他在2020年2月申请并获得一项国家自然科学基金,研发基于RBD的广谱抗沙贝科病毒疫苗。但从其他机构申请的基金项目均告失败,因为有专家认为:1)冠状病毒不易突变,MERS-CoV已经流行了8年,未见明显变异,且传播能力很差,至今全世界也只有2,000多人感染;2)研发广谱疫苗是一个漫长的过程,不能快速获批,无法立竿见影;3)新冠病毒也许在暑假后彻底消失;4)SARS-CoV也许永不再现。但姜世勃和团队成员们并未放弃,采用了“以不变应万变”的策略,即使用新冠病毒原始株的RBD加Fc构建了RBD-Fc疫苗。考虑到RBD中具有高保守序列的中和位点免疫力很低,他们就添加了一个全新的佐剂(即小分子STING激动剂),研发出第一个基于新型佐剂的高效广谱沙贝科病毒通用疫苗候选,其在免疫猴子体内诱生的抗体不但能中和SARS-CoV、蝙蝠SARSr-CoV、新冠病毒(SARS-CoV-2)及其变异株(包括Alpha,Beta,Gamma,Delta,Epsilon,Zeta,Eta,Iota,Kappa)的感染,也能有效地中和对大多数疫苗和抗体药物发生耐受的奥秘克戎变异株假病毒(交叉中和抗体滴度在35,000以上)和真病毒(交叉中和抗体滴度在9,000以上)(图5)。
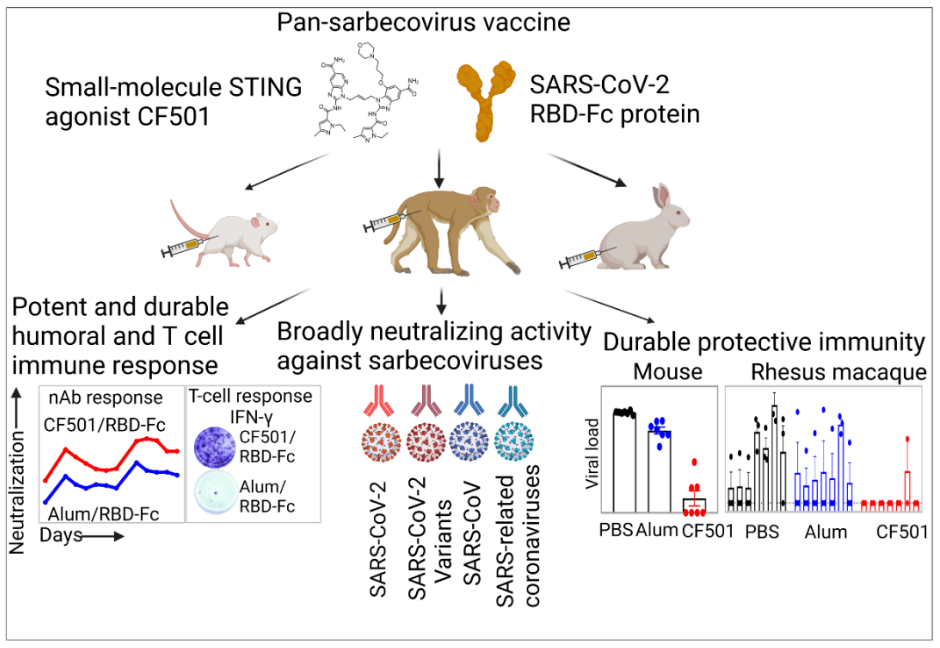 图 5
图 5
目前,他们正在与上海博沃生物科技有限公司和美国Fulgent Genetics Inc 合作,力图将这个高效广谱的沙贝科病毒通用疫苗尽快地推入临床,将可用来防控现在和未来的新冠病毒变异株及将来新发与再现的SARS样传染病。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







