Adv Mater:报道华东理工一氧化氮抗肿瘤纳米药物研究新进展
2018-06-23 华东理工材料学院 细胞
李永生教授团队在一氧化氮(NO)抗肿瘤纳米药物领域研究取得新进展,相关工作成果以“Dual intratumoral redox/enzyme-responsive NO-releasing nanomedicine for the specific, high-efficacy and low-toxic cancer therapy”为题,在线发表于Advanced Materials上。
李永生教授团队在一氧化氮(NO)抗肿瘤纳米药物领域研究取得新进展,相关工作成果以“Dual intratumoral redox/enzyme-responsive NO-releasing nanomedicine for the specific, high-efficacy and low-toxic cancer therapy”为题,在线发表于Advanced Materials上。
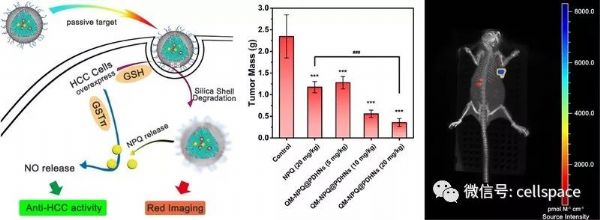
一氧化氮(NO)作为自然界中最小、最简单的生物活性分子之一,在高浓度时能够有效地抑制肿瘤细胞生长、引起细胞凋亡,从而表现出抗肿瘤活性。但目前NO前药的低水溶性、生理不稳定性、较短的半衰期以及较高的毒副作用严重阻碍了其在肿瘤治疗方面的应用。为了解决这些问题,该团队将具有较高抗肿瘤效率的NO前药NPQ负载于含二硫键的有机硅层保护的杂化纳米胶束中,制备了一种具有双重响应(氧化还原响应/酶响应)释放NO的纳米药物,同时利用染料分子QM-2聚集诱导发光(AIE)的成像性能,监控纳米药物在体内的分布。细胞实验表明,该纳米药物仅在肿瘤细胞中释放NO,而在正常细胞中则没有,对肝癌细胞的半抑制浓度IC50值远低于对正常肝细胞的IC50值,表现出对肝癌细胞的特异性杀伤效果。活体实验结果表明,纳米药物在低剂量(5 mg/kg)注射时,抑瘤率达到45.5%,与注射剂量为20 mg/kg的纯NPQ药物的抑瘤效果(49.9%)相当;当纳米药物注射剂量提高到20 mg/kg时,抑瘤率高达84.4%,这在目前负载单一药物的被动靶向纳米药物中处于最佳水平。荧光成像结果进一步显示,该纳米药物可以在肿瘤组织富集,具有较好的肿瘤靶向效果。另外,该纳米药物的杂化硅层能够有效防止NPQ在血液循环和正常组织中发生非酶催化分解释放NO,从而避免因NO引起的静脉舒张、血压降低等副作用。这为设计高效、低毒副作用治疗肿瘤用纳米药物提供了一条新的思路。
该工作主要由我校博士研究生贾晓博在李永生教授和中国药科大学黄张建教授的共同指导下完成。研究得到了国家自然科学基金、国家重点研究开发计划和上海市优秀学术带头人计划等项目的资助。
原始出处:
Jia X, Zhang Y, Zou Y, et al.Dual Intratumoral Redox/Enzyme-Responsive NO-Releasing Nanomedicine for the Specific, High-Efficacy, and Low-Toxic Cancer Therapy.Adv Mater. 2018 Jun 11:e1704490. doi: 10.1002/adma.201704490. [Epub ahead of print]
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#纳米药#
82
#一氧化氮#
79
#纳米药物#
85