ECCO 2024:Mirikizumab与乌司奴单抗对中重度克罗恩病患者的疗效比较
2024-02-24 MedSci原创 MedSci原创 发表于上海
Mirikizumab单抗的 CDAI 临床缓解效果不劣于乌司奴单抗。在生物治疗失败的患者中,与乌司奴单抗相比,Mirikizumab单抗在临床缓解和内窥镜终点方面更优。
近日,欧洲克罗恩病和结肠炎组织第19届大会(ECCO 2024)在瑞典- 斯德歌尔摩 隆重举行。作为世界上首屈一指的炎症性肠病(IBD)大会,每年都会吸引超过上千名与会者。本届大会汇集了全球的IBD领域的医生和专家,并汇报了该领域的最新研究进展。

克罗恩病(CD)是一种原因不明的肠道炎症性疾病,在胃肠道的任何部位均可发生,但多发于末端回肠和右半结肠,其病程多迁延,反复发作,不易根治。Mirikizumab是一款人源化IgG4单克隆抗体, 可与IL-23的p19亚基结合,进而阻断IL-23介导的炎症反应,其已于日本、欧盟、英国等地陆续获批上市,用于中至重度溃疡性结肠炎。
在本次大会上,研究人员报告了VIVID-1研究的次要终点之一,Mirikizumab与乌司奴单抗在中重度克罗恩病患者中的疗效和安全性对比。乌司奴单抗(Ustekinumab)是一种全人源IgG1k单克隆抗体,可结合IL-12/23Chemicalbook的p40亚单位,是全球唯一获批治疗CD的抗IL-12/23的生物制剂,免疫原性和抗抗体发生率低,安全性高。
在这项VIVID-1研究中,研究人员将成人受试者(N=1065)按 6:3:2 随机分配到Mirikizumab(N=579)(每 4 周静脉注射 (IV) 900 毫克至 第12周,然后皮下注射 (SC) 300 毫克至第52周)、乌司奴单抗(N=287)(静脉注射约 6 毫克/千克剂量,然后皮下注射 90 毫克至 第52周)或 PBO(N=199)(每 8 周注射一次)。
结果显示,三个治疗组的基线特征总体平衡。与 PBO 相比,接受Mirikizumab治疗的患者达到了所有关键的主要次要终点(p<.000001)。在治疗第52周时,Mirikizumab单抗组和乌司奴单抗组分别有54.1%和48.4%的患者取得CDAI临床缓解,Mirikizumab单抗不劣于乌司奴单抗(非劣效性界值为10%;P = 0.113117)。
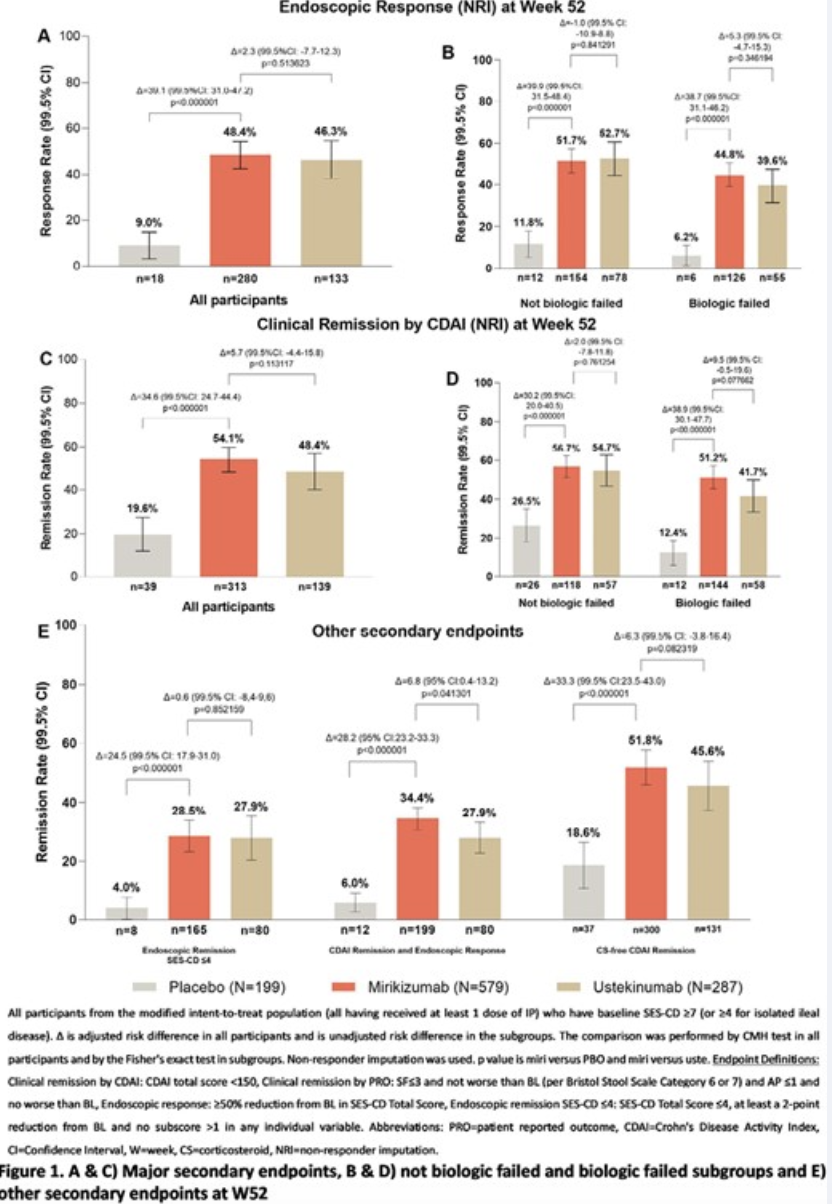
虽然在内镜反应方面没有达到优于乌司奴单抗的水平(p=0.51),但在生物治疗失败的病例中,与乌司奴单抗相比,Mirikizumab单抗在内镜反应和 CDAI 临床缓解方面显示出更高的反应率趋势。
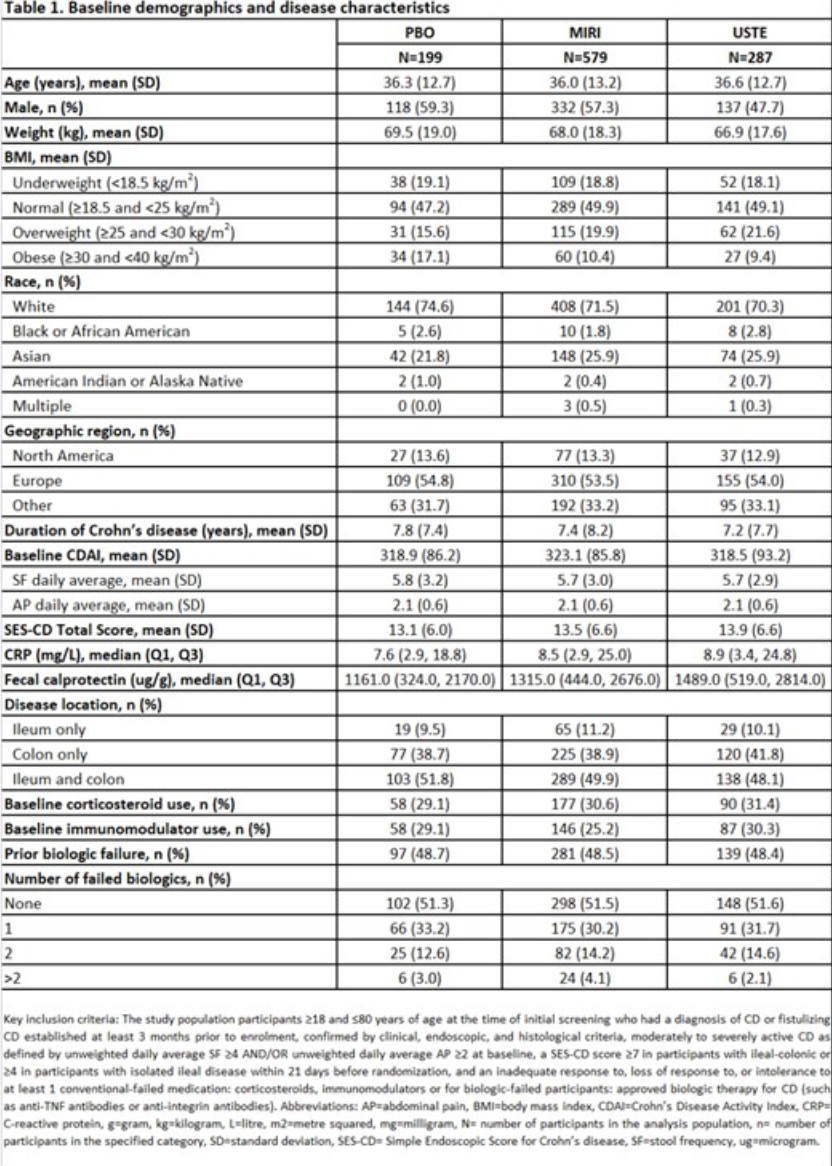
在安全性方面,Mirikizumab单抗(78.6%)和乌司奴单抗(77.3%)的治疗突发不良事件(TEAE)比例相似,最常见的TEAE是COVID-19、贫血、关节痛、头痛、上呼吸道感染、鼻咽炎和注射部位反应。Mirikizumab单抗(10.3%)和乌司奴单抗(10.7%)的严重不良事件发生率相当。
总之,Mirikizumab单抗的 CDAI 临床缓解效果不劣于乌司奴单抗。在生物治疗失败的患者中,与乌司奴单抗相比,Mirikizumab单抗在临床缓解和内窥镜终点方面更优。
参考资料
V Jairath, B E Sands, P Bossuyt, F Farraye, M Ferrante et al.Efficacy of mirikizumab in comparison to ustekinumab in patients with moderate to severe Crohn’s disease: Results from the phase 3 VIVID 1 study.Journal of Crohn's and Colitis, Volume 18, Issue Supplement_1, January 2024, Pages i62–i64, https://doi.org/10.1093/ecco-jcc/jjad212.0035
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#乌司奴单抗# #Mirikizumab# #ECCO 2024#
103