Dev Cell 徐延勇/李晶团队揭示肝细胞调控HDL代谢阻抑动脉粥样硬化进程的新机制
2023-10-22 论道心血管 论道心血管 发表于上海
该研究发现肝细胞源分泌蛋白Lcn2通过降低Nedd4-1介导SR-BI K500和K508位点的泛素化,阻抑SR-BI降解,改善HDL代谢,促进RCT,抑制高脂饮食诱导小鼠的AS进程。
动脉粥样硬化(Atherosclerosis, AS)所致心血管疾病是一种严重威胁人类生命健康并且具有高致残率和高致死率的常见慢性疾病。长期以来,高密度脂蛋白(HDL)被认为是AS和心血管疾病的独立保护因素,其可通过胆固醇逆向转运(RCT)、抗炎、抗氧化、保护血管内皮细胞、抗血栓形成等多种途径,阻抑AS的发生发展。SR-BI是HDL公认的细胞膜受体。肝脏SR-BI可促进HDL介导RCT,降低HDL-C水平,调节HDL代谢,阻抑AS进程。肝SR-BI作为调控HDL功能及代谢的重要靶标,如何靶向调控其表达始终是HDL代谢领域亟待解决的难题。
2023年10月19日,复旦大学徐延勇研究员团队与首都医科大学附属朝阳医院李晶副教授团队在Developmental Cell在线发表题为“Hepatocytic lipocalin-2 controls HDL metabolism and atherosclerosis via Nedd4-1-SR-BI axis in mice”的研究论文,该研究发现肝细胞源分泌蛋白Lcn2通过降低Nedd4-1介导SR-BI K500和K508位点的泛素化,阻抑SR-BI降解,改善HDL代谢,促进RCT,抑制高脂饮食诱导小鼠的AS进程。
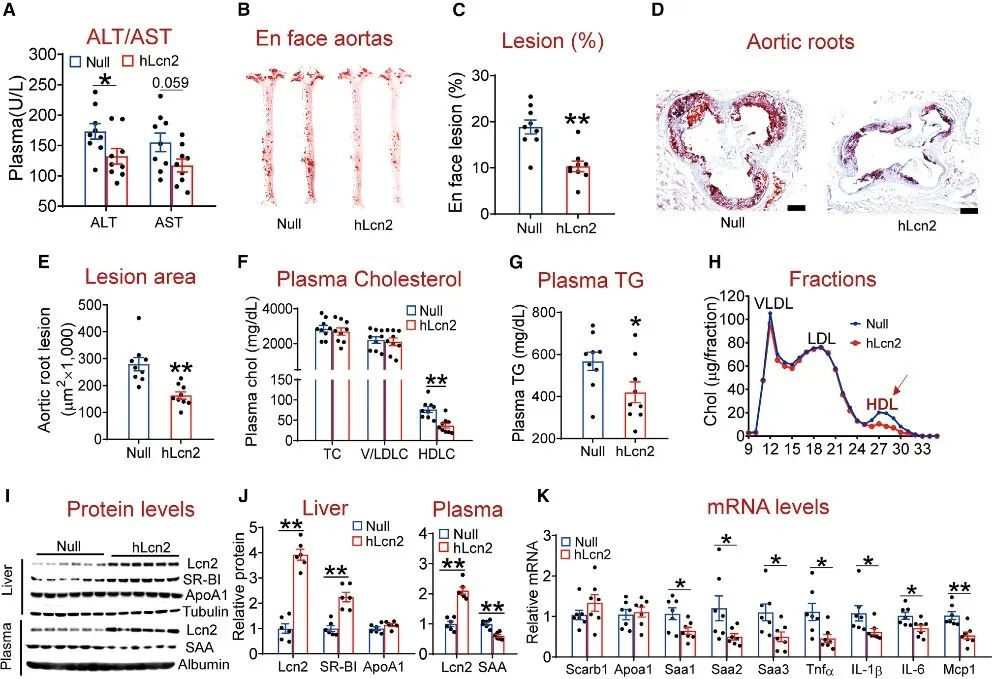
首先,研究团队在临床上发现肝脏Lcn2 mRNA水平与血浆HDL胆固醇水平呈显著的负相关,提示Lcn2可能是HDL代谢的关键调控分子。团队针对Lcn2在HDL代谢中的作用展开研究,发现肝细胞Lcn2高表达,改善SR-BI介导的HDL代谢,促进RCT,阻抑AS进程。而肝细胞Lcn2缺失有相反的实验效果。
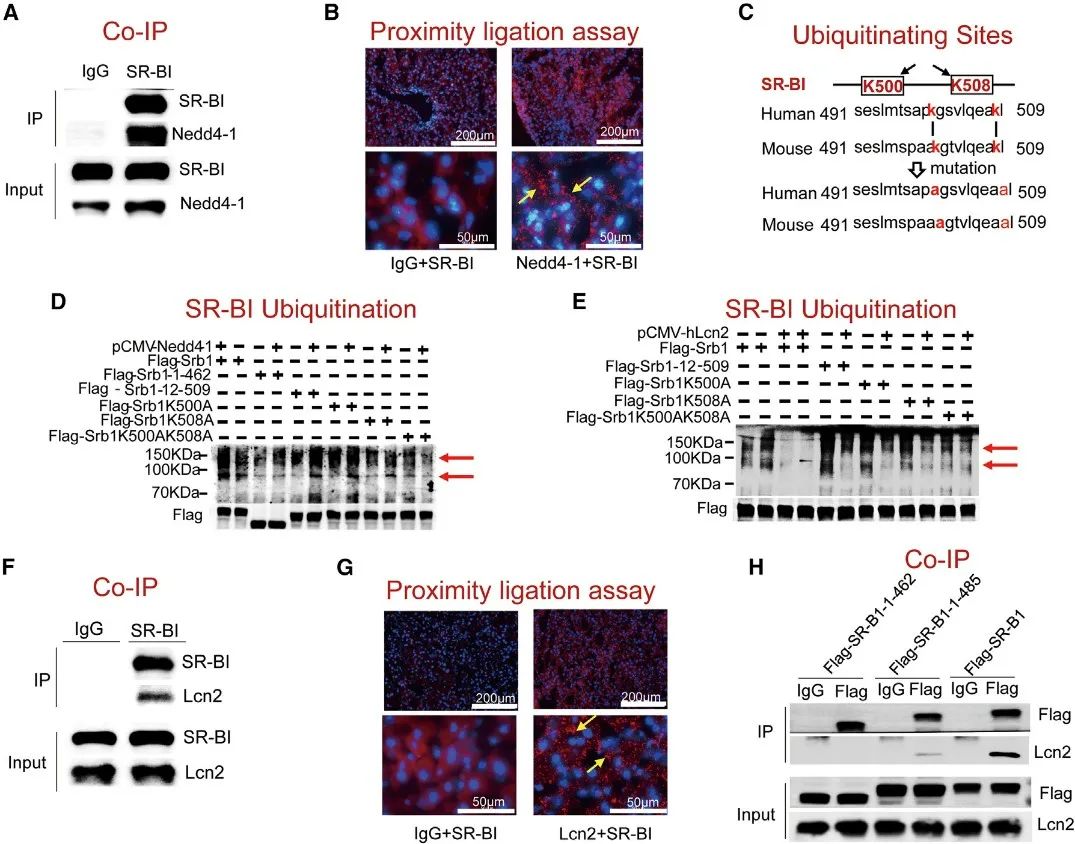
进一步机制研究发现,肝细胞Lcn2在翻译后修饰水平上降低Nedd4-1介导SR-BI K500和K508位点的泛素化,抑制SR-BI蛋白降解。
综上,该研究揭示了肝细胞SR-BI的调控新机制,为靶向调控肝脏SR-BI及HDL代谢防治AS提供新的靶点。

复旦大学基础医学院胡淑伟博士(现为东北俄亥俄医科大学博士后)、朱颖东博士(现为耶鲁大学博士后)、赵小杰博士(现为复旦大学博士后)为该论文的并列第一作者,徐延勇研究员、李晶副教授为该论文的通讯作者。特别感谢复旦大学基础医学院吴慧娟教授,在课题建立初期给予大量的人力支持与帮助。此外,本研究得到中国科学院邵孟乐研究员、吉林大学李心慰教授、南京师范大学胡志刚教授、上海交通大学刘军教授等的大力支持。
原文链接:
https://www.cell.com/developmental-cell/fulltext/S1534-5807(23)00494-X
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














签到学习
78