《Nature》重磅!衰老的骨骼干细胞会延缓骨折愈合,并促进炎症发展加速全身衰老!
2022-12-13 生物探索 生物探索 发表于安徽省
对衰老的骨骼干细胞进行单细胞遗传分析,研究人员发现了一种被称为聚落刺激因子的特殊因子。
骨骼干细胞(skeletal stem cell, SSC)的作用是分化产生骨细胞、软骨细胞,同时为造血干/祖细胞(haematopoietic stem and progenitor cell, HSPC)的发育提供了合适的微环境。但是随着人类不断衰老,干细胞也会衰老,主要表现在其分化能力和活性降低,随之而来的是在老年人身上发现的各种各样的疾病。
近日,美国斯坦福大学Charles K. F. Chan、Michael T. Longaker等研究人员发现,衰老的骨骼干细胞会产生一种炎症退化微环境,不仅会导致骨折愈合不良、骨质疏松症、各种血液疾病的发生,还会促进全身细胞和系统的普遍炎症,进而影响到人体健康。相关研究于2021年8月11日发表在Nature杂志上,论文标题为“Aged skeletal stem cells generate an inflammatory degenerative niche”。

骨折后愈合困难是导致老年人死亡率上升的一个主要原因,研究人员发现这与衰老的骨骼干细胞有关。前期的研究发现,年老小鼠的骨骼干细胞活性要远低于年轻小鼠。在愈合的过程中,骨折处形成骨痂,骨痂内充满骨骼干细胞,而在年老小鼠中,愈合部位的骨骼干细胞要少得多。此外,与年轻的骨骼干细胞相比,体外衰老的骨骼干细胞形成集落或骨骼的能力也较差。正常情况下,骨组织在旧骨吸收、新骨形成的动态平衡中不断地更新、修复,但在年老的骨骼中,衰老的骨骼干细胞所表达的基因与骨形成减少和骨吸收增加有关,这种不平衡最终导致骨质疏松症。
进一步研究发现,骨折愈合的部分问题可能存在于骨骼干细胞与HSPC之间的联系,衰老的骨骼干细胞会产生一种改变血细胞发育的微环境。在促炎性的衰老骨骼干细胞影响下,HSPC分化产生更多的髓系细胞,其中包括一种吸收骨骼的细胞类型,髓系细胞产生更多的炎症因子,导致纤维生长,干扰骨骼的愈合。
慢性炎症与多种组织和器官的衰老密切相关。衰老的骨骼干细包可以通过改变HSPC的正常发育推动更多炎症细胞的产生,同样,衰老的骨骼干细胞也可能加速全身各个部位的炎症和衰老的进程。因此,研究人员发现,如果可以逆转骨骼干细胞的老化,那么就可以阻止这种衰老的趋势。
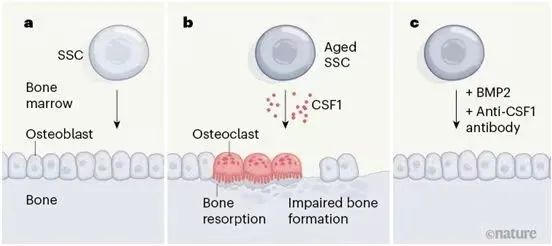
对衰老的骨骼干细胞进行单细胞遗传分析,研究人员发现了一种被称为聚落刺激因子1(Colony-stimulating factor 1, Csf1)的特殊因子。适量的Csf1对骨骼愈合是必需的,与年龄有关的Csf1数量的增加可能是干扰骨折愈合的重要原因。通过抑制这一基因的表达,可以促进老年小鼠骨折部位的愈合。这说明如果可以逆转骨骼干细胞的衰老,将有可能遏制炎症的发生和全身性的衰老。
此外,研究人员还发现一种叫做骨形态发生蛋白2(BMP2)的骨骼干细胞刺激信号分子的产生减少,使用含有BMP的凝胶对年老小鼠的骨折面进行处理,可以明显改善骨折的愈合情况。
通过对抗骨骼干细胞的老化,研究人员成功做到了使年老小鼠的骨折愈合贴近年轻小鼠的骨折愈合。随着人口老龄化,老年人骨折的医疗负担不断增加,这项研究在治疗老年人骨折上带给我们启发。此外,让衰老的骨骼干细胞返老还童很可能会潜在地扭转炎症免疫细胞的倾斜性产生以及生成的血细胞类型的不平衡,通过解决骨骼干细胞衰老时发生的变化,最终可能会减少整个身体与年龄有关的变化和疾病。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







