Cell Metab :减肥能增加骨质量,或成新的抗骨质疏松治疗策略
2020-10-21 张佳兴 生物探索
众所周知,脂肪组织可以影响骨骼的生长,通俗理解就是因为肥胖容易增加骨量。现已有证据表明脂肪组织和骨骼之间存在代谢关系。更有意义的是,了解脂肪细胞的产物控制骨细胞的机制可能会发现新的抗骨质疏松治疗策略。
众所周知,脂肪组织可以影响骨骼的生长,通俗理解就是因为肥胖容易增加骨量。现已有证据表明脂肪组织和骨骼之间存在代谢关系。更有意义的是,了解脂肪细胞的产物控制骨细胞的机制可能会发现新的抗骨质疏松治疗策略。
2020年10月6日,美国华盛顿大学医学院StevenL.Teitelbaum团队在国际学术期刊《细胞—代谢》上发表题为“AblationofFatCellsinAdultMiceInducesMassiveBoneGain”的文章,揭示了成年小鼠脂肪细胞的消除能够诱导大量的骨增加。
研究团队之前已经证明,通过在脂肪中表达白喉毒素受体(DTR),使白色(WAT)和棕色脂肪组织(BAT)的种系缺失,可观察到骨量显着提高。但此种系诱导脂肪消耗只发生在胚胎发育过程中。为了克服这一局限性,研究团队建立了一个更具治疗相关性的模型,在成年小鼠中诱导脂肪消融。为此,研究团队将表达灵长类白喉毒素受体(DTR)的小鼠与那些表达脂联素(ADQ)-Cre的小鼠交配。因此,DT给药可以完全消除这些DTRADQ小鼠中的WAT和BAT,并可消融骨髓脂肪细胞。
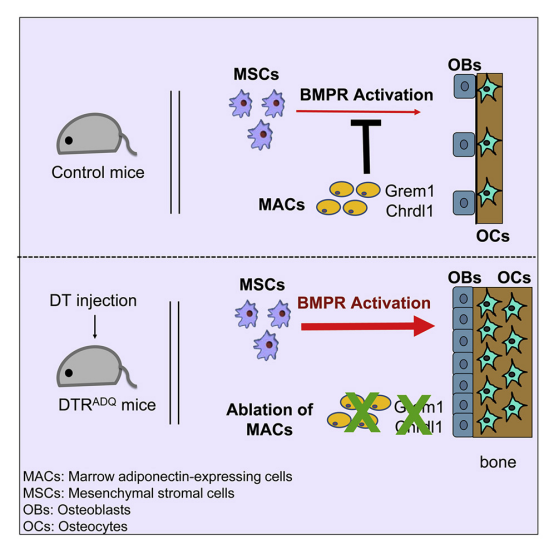
实验流程图
之后,研究团队假设脂肪组织消融术可以引起骨量增加,为了验证这一假设,将携带灵长类DTR的小鼠(DTR-STOPfl/fl)与表达ADQ-Cre(DTRADQ小鼠)的小鼠配对,给予2个月大的DTRADQ小鼠(DT/DTRADQ小鼠)的DT实际上消除了WAT-BAT,导致血清脂联素消失、血清乳酸脱氢酶(LDH)水平升高,这可代表外周脂肪库几乎完全消融。给药10天后,发现骨实质上占据了干骺端到骨干的整个皮质内间隙。而在DT给药后3-4天内就可观察到大量新骨基质,此时骨髓脂肪细胞不再明显,也没有骨髓坏死的迹象。
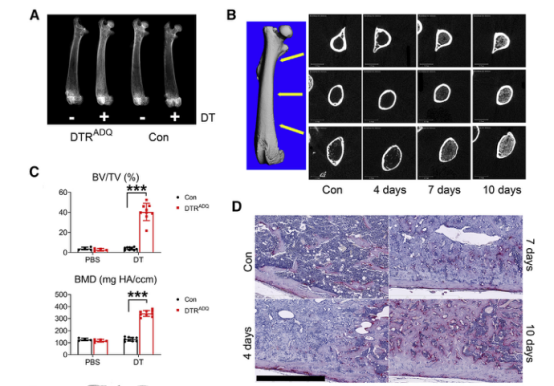
成年去脂小鼠骨硬化
随后,研究人员对其结果进行了机制研究,研究表明这种脂肪细胞敲除介导的骨骼质量增强现象反映出消除了其抑制剂后骨形态发生蛋白(BMP)受体的激活,这与同时的表皮生长因子(EGF)受体信号传导有关。DTRADQ诱导的骨硬化不是由于周围脂肪细胞的消除引起的,而是可能消除了表达ADQ的骨髓脂肪细胞。
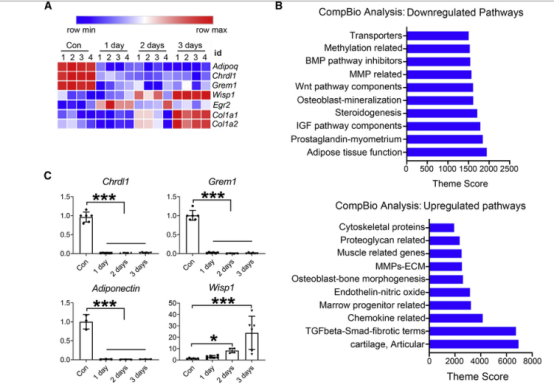
BMPR信号介导脂肪细胞消融诱导成骨
骨质疏松症表现为破骨细胞相对于成骨细胞活性的增强。治疗方法包括抗吸收或促成骨药物。但抗吸收剂诱导的骨质量可能导致非典型骨折,可能是因为这在药物性骨合成代谢的背景下并不发生成骨,因此需要刺激成骨细胞的制剂,而靶向BMP受体抑制剂(具有短期EGF受体活化作用)的合成代谢药物可能是大幅增加骨骼质量以预防或逆转病理性骨丢失的一种手段。
原始出处:
Wei Zou, Nidhi Rohatgi, Jonathan R Brestoff,et al.Ablation of Fat Cells in Adult Mice Induces Massive Bone Gain.Cell Metab. 2020 Oct 3;S1550-4131(20)30489-7. doi: 10.1016/j.cmet.2020.09.011.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#MET#
67
脂肪细胞导致骨质疏松
76
#Meta#
66
#CEL#
47
#Cell#
62
#抗骨质疏松#
55
#骨质#
51
什么时候有懒人用的减肥神药?
83
打卡
102