1例原发纵隔生殖细胞肿瘤诊治
2016-05-19 中山大学肿瘤防治中心 胡倩 王钊 黄河 林桐榆 中国医学论坛报
患者,19岁男性,于2011年11月出现持续性刀割样胸痛,活动时加重,体位改变可好转,伴有头面部、颈部浮肿,无发热、畏寒,无咯血,无咳嗽、咳痰,无心悸胸闷,无大汗淋漓,无其他部位放射性疼痛,当地医院行CT检查提示左上前纵隔恶性肿瘤,双侧肺纹理增多,左侧少量胸腔积液。
病史
现病史
患者,19岁男性,于2011年11月出现持续性刀割样胸痛,活动时加重,体位改变可好转,伴有头面部、颈部浮肿,无发热、畏寒,无咯血,无咳嗽、咳痰,无心悸胸闷,无大汗淋漓,无其他部位放射性疼痛,当地医院行CT检查提示左上前纵隔恶性肿瘤,双侧肺纹理增多,左侧少量胸腔积液。患者此后就诊于我院,12月16日在我院门诊查CT提示左前纵隔较大肿块,考虑恶性肿瘤,侵袭性胸腺瘤可能性大,肿块侵及左侧头臂静脉,其内及上腔静脉内栓子形成;左侧胸腔积液。等候检查期间,患者胸痛无明显缓解,出现头面部、颈部浮肿进行性加重,伴咳嗽、咳痰。患者为求进一步治疗,于2012年1月16日入院。患病以来,患者神志清,精神可,胃纳可,睡眠一般,大便通畅,小便清长,体重无明显下降。
既往史
既往体健,否认高血压、心脏病病史,否认肝炎、结核和伤寒等传染病病史,否认外伤史及输血史。
查体
体能状态(PS)评分1分;神清,精神可;头面部,颈部浮肿;左侧颈部及左侧前胸部可见静脉曲张。左臂肌力Ⅳ级,伴麻木,浅感觉减退。全身浅表淋巴结未及。双侧呼吸运动对称,呼吸音清,未及干湿音。全腹无压痛,无反跳痛,未扪及包块。肝脾肋下未及。脊柱四肢无畸形。
辅助检查
血常规、生化、凝血功能均未见明显异常;甲胎蛋白(AFP)为35221ng/ml,明显升高;神经元特异性烯醇化酶(NSE)为41.81ng/ml,轻度升高;乳酸脱氢酶为(LDH)331.7U/L,轻度升高;人绒毛膜促性腺激素(HCG)、癌胚抗原(CEA)和β2微球蛋白(β2MG)均正常。
全身CT检查发现左前纵隔肿块大小约70mm×91mm,肿块侵及左侧头臂静脉,其内及上腔静脉内栓子形成(图1a)。
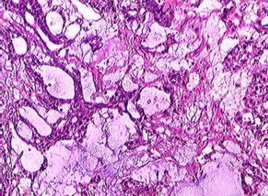
2011年12月,在我院行纵隔肿块穿刺术,穿刺组织病理检查见肿瘤细胞呈筛网状或巢状排列,细胞异型,核分裂易见,符合恶性肿瘤;免疫组化提示细胞角蛋白(CK)7(-)、ki-67为80%、CK(+)、CD5(-)、CD30(-)、CD117(+)、胎盘碱性磷酸酶(PLAP)(+)、HCG(+)、AFP(+);以上结果提示生殖细胞来源可能性大。
诊断
1.纵隔生殖细胞恶性肿瘤(卵黄囊瘤Ⅲc期高危)
2.上腔静脉压迫症
治疗经过
一线治疗
2012年1月16日至2012年6月,给予博来霉素(15mg,d1、d3、d5)+依托泊苷(VP-16)(总量500mg,d1~d3)+顺铂(总量100mg/m2,d1~d3)(BEP方案),6个疗程后疗效评价为部分缓解(PR)(图1b)。AFP值下降(图3)。

图1 初治时及BEP化疗后纵隔病灶(a 治疗前的病灶;b 6个疗程BEP化疗后的病灶)

图3 初治时AFP随化疗疗程的动态变化
手术
2012年7月,本院多学科讨论意见为,应行手术切除残留肿块明确是否有活性肿瘤成分。
2012年7月19日,在我院行胸骨正中劈开前纵隔肿块切除术;术中发现肿块大小5cm×5cm。
术后病理提示(前纵隔肿物)送检组织大部分坏死,可见纤维组织增生,炎症细胞浸润,局部见软骨、鳞状上皮、腺上皮、脂肪、神经、骨等组织,部分区域可见筛网状排列的星芒状细胞,结合病史及免疫组化结果,病变符合混合性生殖细胞肿瘤(成熟型畸胎瘤与卵黄囊瘤混合)。术后AFP为5.3ng/ml。此后患者一直在外科门诊随访,未予放化疗。
复发
2013年4月(术后8个月),患者再发胸痛;AFP升高至103.6ng/ml;正电子发射体层摄影(PET)/CT提示前纵隔出现高代谢病灶,并且侵犯前胸壁(图2a)。

图2 复发时及TIP化疗后纵隔病灶(a 复发时的病灶;b 4个疗程TIP化疗后的病灶)
挽救治疗
2013年5月22日,给予吉西他滨1.0g/m2、d1+多西他赛75mg/m2(GD方案),1个疗程后评价疗效为疾病进展(PD)。
2013年6月至2013年8月,多西他赛75mg/m2、d1+异环磷酰胺3g、d1~d3+顺铂40mg、d1~d3(TIP方案),4个疗程后评价疗效为PR(图2b)。
2013年9至2013年10月,异环磷酰胺(IFO)3g、d1~d3+脂质体多柔比星40mg、d1,2个疗程后评价疗效为完全缓解(CR)。AFP值下降(图4)。

图4 复发时AFP随化疗疗程的动态变化
放疗
2013年12月至2014年1月,行局部放疗(54Gy,23f)。
随访
此后,患者一直在门诊随访,末次随访时间为2016年3月22日,胸部增强CT扫描提示纵膈恶性肿瘤放疗手术治疗后,未见新发肿块征象。
讨论
生殖细胞肿瘤好发于儿童及青少年,可发生在性腺内,如卵巢和睾丸,也可发生在性腺发育过程中移行的中线区域,如松果体、骶尾椎、纵隔腔和后腹膜等。该疾病由原始多潜能生殖干细胞分化异常,停留在某一个阶段增生而形成。生殖细胞组织类型复杂,如原始生殖细胞未分化,可发生无性细胞瘤;生殖细胞未分化,可发生胚胎癌;如发生胚胎分化则可形成畸胎瘤;胚外组织分化可发生绒毛膜癌、卵黄囊瘤等。几种生殖细胞肿瘤可以单独存在,亦可以混合存在,形成肿块。
生殖细胞肿瘤的诊治可借鉴睾丸癌指南
目前在临床实践中,生殖细胞肿瘤的诊断和治疗还是借鉴睾丸癌的指南。睾丸癌绝大部分为生殖细胞肿瘤,而按肿瘤细胞的类型又可分为精原细胞瘤和非精原细胞瘤。非精原细胞瘤按病理类型又分为胚胎癌、绒毛膜上皮癌、卵黄囊瘤和畸胎瘤4种。睾丸肿瘤除TNM分期之外,还根据肿瘤标志物乳酸脱氢酶(LDH),人绒毛膜促性腺激素(HCG)和甲胎蛋白(AFP)进行S分期,包括S1、S2、S3期。此外,转移性睾丸癌根据其发生部位、有无肺外转移和肿瘤标志物,可以分为低危、中危和高危3种危险分度。
原发于纵隔的生殖细胞肿瘤被列为睾丸癌高危复发类型。在本病例中,患者AFP明显升高,病理免疫组化检查亦提示AFP(+),故考虑肿瘤中有卵黄囊瘤成分。卵黄囊瘤分泌AFP,AFP是胎儿期最早出现的血浆蛋白,由胚胎发育早期的卵黄囊分泌,之后可由肝细胞和消化道产生。因此,AFP对于卵黄囊瘤的诊断有重要的指导意义。
AFP的半衰期为4.2~5.8天。通常认为,对于卵黄囊瘤患者,AFP水平在治疗后呈指数水平下降是化疗敏感的一项重要指标(图3)。临床经验认为,卵黄囊瘤一线治疗可以在AFP恢复正常、再巩固2个疗程后停止,而患者获得疾病缓解之后,在随访监测过程中,AFP也是监测复发最敏感的一项指标(图4)。
生殖细胞肿瘤患者存在潜在治愈可能
在现代医学发展初期,针对生殖细胞肿瘤多采用简单的手术切除,但是单纯的手术切除后患者易出现局部肿块复发和远处转移,此时患者的5年生存率只有不到20%。随着生殖细胞肿瘤对化疗敏感的认识加深,以及博来霉素+依托泊苷+顺铂(BEP方案)、异环磷酰胺+顺铂+依托泊苷(VIP)等方案的普遍应用,近年来大大改善了这类疾病患者的预后。2015年欧洲泌尿学会(EAU)指南中指出,非精原细胞肿瘤Ⅲ期患者的5年生存率已经提高到约50%。
生殖细胞肿瘤对化疗高度敏感,通过化疗可以获得根治,然而一线治疗肿瘤指标正常后停止治疗,肿瘤容易复发。何时停止化疗进入观察随访监测阶段值得深入研究。2016年美国国立综合癌症网络(NCCN)睾丸癌临床指南指出,原发纵膈生殖细胞肿瘤(睾丸癌ⅢC期高危)的患者在BEP方案4个疗程化疗后如影像学疗效评价部分缓解(PR)(即使肿瘤指标正常),还必须补充局部手术切除术;术后病理如提示坏死或成熟畸胎瘤,患者可进入随访监测阶段;但如在已切除肿块中仍发现有非精原细胞其他活性成分(除外成熟畸胎瘤),则需要补充二线方案如VIP、顺铂+长春新碱+异环磷酸胺(VeIP)化疗2个疗程后清除残留肿瘤细胞以减少复发风险;如因患者个体原因无法接受局部残留肿块切除术,还可以采用局部放疗手段。通过手术、化疗和放疗等多学科综合手段,纵隔生殖细胞肿瘤(卵黄囊瘤)患者仍有潜在的治愈希望。
难治复发的纵隔生殖细胞肿瘤的处理
一般而言,原发纵隔生殖细胞肿瘤对化疗敏感,一线治疗过程中肿瘤指标呈指数级下降,但是也有一些患者对BEP方案化疗不敏感。
对于一线治疗不缓解的患者,建议根据预后因素来选择挽救治疗方案。不良因素包括:睾丸外病变、一线化疗未达到完全缓解(CR)、血清肿瘤学标志物水平高以及肿瘤负荷大等。
标准的二线治疗包括传统剂量和高剂量化疗。对于有预后不良因素的患者,化疗可采用临床试验方案传统剂量化疗、高剂量化疗以及高剂量化疗联合自体造血干细胞移植。二线化疗方案包括顺铂、异环磷酰胺、长春新碱或紫杉醇。
高危晚期的生殖细胞肿瘤复发可能性大。原发纵隔卵黄囊瘤患者极易因残留肿瘤细胞而出现疾病反复。
指南推荐,复发后的患者需要考虑姑息治疗。复发患者建议使用吉西他滨、奥沙利铂、紫杉醇或依托泊苷等组成姑息化疗方案。但我们认为,对于复发的患者,如对二线治疗敏感,治疗后肿瘤指标达正常,仍可以采用局部的手术及放疗清除肿瘤残留,患者仍有治愈的潜在可能。
目前,生殖细胞肿瘤的分子靶向治疗还是很有限,但是人们一直还在尝试通过多种分子靶向治疗药物治疗生殖细胞肿瘤。
2006年一项采用三氧化二砷治疗难治的生殖细胞肿瘤的Ⅱ期临床试验纳入的20例患者中,5例达到了PR,疾病进展时间为1个月。此外,还有几项采用贝伐珠单抗治疗生殖细胞肿瘤的研究,结果并没有突破性改善。随着新药的不断涌现,目前舒尼替尼、帕唑帕尼和γ分泌酶抑制剂――RO4929097等新药治疗复发生殖细胞肿瘤的临床试验正在进行中,我们仍在期待试验结果。
小结
纵隔卵黄囊瘤是一种罕见的高度恶性肿瘤。患者对化疗敏感,易复发,预后差。但是通过化疗、手术和放疗等多学科综合治疗手段,患者仍有潜在治愈希望。化疗达CR后合理处理活性残留是患者长期生存的关键。
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







拜读,好文
83
#生殖细胞#
63
#生殖细胞肿瘤#
82