JCO:IMPRESS研究解读:吉非替尼耐药后二线治疗该如何选择?
2018-01-07 慧语 肿瘤资讯
EGFR-TKI是EGFR突变阳性的晚期非小细胞肺癌一线治疗手段。一线吉非替尼耐药后是否需要继续服用吉非替尼尚不明确。一项III期、双盲、多中心的随机对照临床试验——IMPRESS应运而生。该研究评估一线吉非替尼治疗疾病进展后继续口服吉非替尼联合顺铂/培美曲塞化疗对比安慰剂联合顺铂/培美曲塞化疗的有效性和安全性。
一、IMPRESS研究简介
背景:
EGFR-TKI是EGFR突变阳性的晚期非小细胞肺癌一线治疗手段。一线吉非替尼耐药后是否需要继续服用吉非替尼尚不明确。一项III期、双盲、多中心的随机对照临床试验——IMPRESS应运而生。该研究评估一线吉非替尼治疗疾病进展后继续口服吉非替尼联合顺铂/培美曲塞化疗对比安慰剂联合顺铂/培美曲塞化疗的有效性和安全性。IMPRESS研究于2015年2公布了主要终点指标无进展生存时间(PFS),显示继续TKI无PFS获益。2017年10月本研究公布了成熟的总生存(OS)数据以及T790M特定生物标记物的探索性分析结果。
方法:
研究者在11个欧亚国家71家中心开展了这项随机对照III期试验IMPRESS研究。符合条件的受试者为:18岁以上,细胞学或者病理学确诊的未经化疗且EGFR突变阳性(EGFR突变状态由血浆提取的循环肿瘤DNA通过基于磁珠法乳浊液扩增和流式检测的数字化PCR检测)的局部晚期、转移性NSCLC;一线吉非替尼治疗取得4个月以上CR/PR或者6个月以上SD;随机前4周出现影像学进展(RECIST v11标准);预期生存超过12周,WHO评分0-1。随机入组后,试验组接受吉非替尼250 mg/d联合培美曲赛500 mg/㎡和顺铂75mg/㎡ ,对照组接受安慰剂联合培美曲赛500 mg/㎡和顺铂75 mg/㎡ 。主要研究终点PFS,次要研究终点OS、 ORR 、 DCR。
结果:
265例患者按1:1随机分到吉非替尼组(133名)和对照组(132名)。结果显示两组患者PFS无统计学差异(HR=0.86,95%CI 0.65-1.13,P=0.273);吉非替尼组的OS劣于对照组(风险比1.44, 95%CI 1.07-1.94, P=0.016,中位OS 13.4月vs19.5月)。亚组分析结果与总体结论一致。但在T790M突变阴性亚组中,观察到吉非替尼组患者的PFS有获益趋势但无统计学差异(风险比0.67,95%CI 0.43-1.03,P=0.0745)。不良反应主要为恶心和食欲下降,未观察到间质性肺部疾病。吉非替尼组1、2级胃肠道毒性更为多见,患者死亡2例,对照组死亡1例,均与治疗相关。总体两组安全性无差异。
结论:
IMPRESS研究结果表明EGFR突变阳性晚期NSCLC患者TKI一线治疗耐药后继续一代TKI治疗PFS无获益,OS受损。其中T790M突变阴性的患者继续TKI有获益趋势但无统计学差异。
二、研究解读
IPASS研究引领的一系列研究奠定了EGFR TKI作为一线治疗在EGFR阳性患者中的地位。随之而来的问题是耐药后该如何办?也相应有各种理论,其中一种是,基于临床观察发现,约25%的患者在进展后停用TKI会产生肿瘤爆发性生长现象,基于此推荐进展后继续使用TKI。那我们看下继续TKI治疗的3个研究:Impress研究、Aspiration研究及Lux-lung5研究。
令人困惑的是,三个研究的结论并不一致。Impress研究在进展后推荐使用化疗,而Aspiration研究显示进站后继续厄洛替尼治疗为患者带来3.1个月的PFS获益,Lux-lung5研究提示进展后在化疗基础上继续应用阿法替尼,中位PFS有2.8个月获益。那么接下来看下表面上结论相互矛盾的三个研究的异同之处。
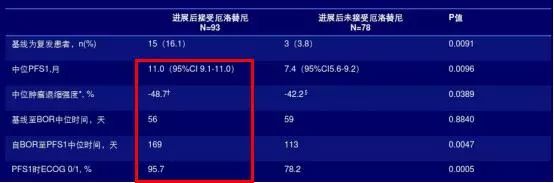
Aspiration 研究是一项II期单臂研究,无对照是它的天然缺陷,而Impress是个III期随机对照(RCT)研究,结论的可靠性更强。且Aspiration 研究的设计规定在第一次进展(PD)后,由患者或研究者自主选择是否继续接受TKI治疗,导致患者选择偏倚,从公开的数据可以看到那些在一线治疗中状态好的人更倾向选择继续治疗;比如更长的中位PFS1、更好的肿瘤退缩、更佳的ECOG状态等(见表1) ;而Impress研究是没有选择性的随机入组,并且数据显示在吉非替尼组的患者基线状态或许更差,比如有更多的脑转移和SD比例(或CR、PR比例低)。此外,Aspiration 研究PFS2的终点事件也是由研究者自行判断决定,研究者判定的PFS往往不够客观,操纵空间较大。ASPIRATION研究在发生PD时没有重复进行EGFRT790M的活检,以确认其获得性耐药的状态,是研究设计的一大缺陷;而Impress研究在设计上对T790M的状态进行了分析,并且T790m亚组分析提示对于T790M阴性的亚组继续吉非替尼治疗有获益趋势。但是两个研究均没有区分PD亚型(缓慢进展、局部进展或广泛进展/有症状的无症状的),由驱动基因导致的PD异质性大,不同的治疗选择在不同的PD亚型的预后差异巨大。ASPIRATION研究是自主选择是否继续治疗,临床经验提示那些缓慢进展或寡转移(1-3淋巴结)的患者更多的选择继续TKI治疗;而快速进展或全身系统性转移的患者更多的会终止TKI治疗。Impress研究虽然是随机分配,但同样在设计时没有考虑进展的亚型,也无法回答PD亚型对结局的影响。
表1 Aspiration 研究PD后是否继续TKI治疗的患者的基线情况
LUX-Lung 5的研究结论显示继续阿法替尼(二代)联用紫杉醇与自主选择的化疗(ICC)相比,对于一代二代EGFR-TKI治疗获得缓解之后又进展的NSCLC患者继续二代TKI治疗可以获得更久的PFS。但是,此研究的最大问题是没有对入组人群的EGFR状态进行检测,即入组人群既包括EGFR阳性人群也包括EGFR阴性人群,同时T790M的状态也未知,入组人群异质性大。并且此研究关于获得性耐药的定义,是用所谓的“临床获得性耐药”作为替代标准,即TKI临床获益、且阿法替尼疾病控制≥12周。此外,对照组是研究者自行选择的化疗方案ICC:化疗药物的中位PFS各不相同,紫杉是3.8个月,而培美和其他方案分别是2.9和2.1个月,而试验组中联合的化疗药物恰恰选择的是疗效好的紫杉。有研究提示对于T790M阴性的患者阿法替尼耐药机制与mTOR信号传导通路有关,而两项临床前研究3-4发现紫杉恰恰能够阻断mTOR信号通路,所以试验组阿法+紫杉的PFS优势究竟是来自于紫杉还是阿法延期或二者协同很难解释,对照组如果都规定为紫杉结果又会如何呢?
最后总结下三个继续TKI治疗的研究结果,Aspiration研究延用TKI治疗的获益人群是EGFR阳性、T790阴性且一线TKI效果更好的那部分人;Impress研究的结果是在EGFR阳性的人群中,PFS无差异,OS化疗更好,但在T790阴性的亚组人群中,我们发现继续TKI是有获益趋势的,这点其实是与Aspiration研究一致的。再看Lux-lung5研究在设计上,没有进行EGFR检测、T790M状态未知、耐药原因不明、获得性耐药用临床获益作为替代指标、对照组采用自主选择的化疗方案导致对于T790阴性亚组的获益是否是继续TKI带来的尚无法明确。Lux-lung5研究在设计上不分人群、不分耐药原因、不分进展类型,得到的结论似乎给临床的提示非常有限。但此研究的探索分析提示既往TKI治疗后获益时间更长的人群延用TKI治疗获益更多,此结果也与Aspiration研究不谋而合。
所以三个研究表面结果看似矛盾,其实内部有着千丝万缕的佐证关系,恰恰是不同的结论,给我们提示,关于继续TKI的问题不能一概而论,首先要考虑患者EGFR敏感性、明确耐药机制,明确进展类型,再去决定什么时间点去改变治疗可能更好。
原始出处:
1. Mok TSK, Kim SW, Wu YL, et al. Gefitinib Plus Chemotherapy Versus Chemotherapy in Epidermal Growth Factor Receptor Mutation-Positive Non-Small-Cell lung Cancer Resistant to First-Line Gefitinib(IMPRESSS): Overall Survival and Biomarker Analyses. J Clin Oncol. 2017 Oct 2. doi: 10.1200/JCO.2017.73.9250.
2. Soria JC1, Wu YL2, Nakagawa K, et al. Gefitinib plus chemotherapy versus placebo plus chemotherapy in EGFR-mutation-positive non-small-cell lung cancer after progression on first-line gefitinib (IMPRESS): a phase 3 randomised trial. Lancet Oncol. 2015 Aug;16(8):990-8. doi: 10.1016/S1470-2045(15)00121-7.
3. Rocha GZ1, Dias MM, Ropelle ER, et al. Metformin amplifies chemotherapy induced AMPK activation and antitumoral growth. Clin Cancer Res. 2011 Jun 15;17(12):3993-4005.
4. Le XF, Hittelman WN, Liu J, et al. Paclitaxel induces inactivation of p70 S6 kinase and phosphorylation of Thr421 and Ser424 via multiple signaling pathways in mitosis. Oncogene. 2003 Jan 30;22(4):484-97.
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#IMPRESS研究#
35
#JCO#
32
学习学习学习
55
学习了.涨知识
45
#二线治疗#
28
谢谢.学习了
46
学习了新知识
45
了解了解.继续关注
43
谢谢分享
27
吉非替你的奶要研究
21