第三个国产PD-1单抗正式获批
2019-05-31 佚名 医谷综合报道
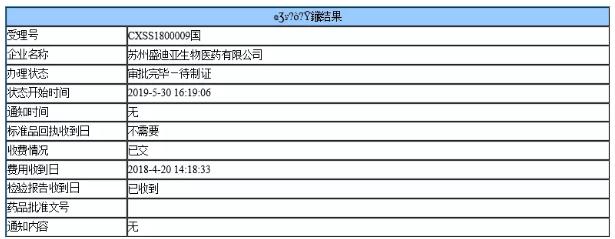
今日(5月31日),根据国家药监局行政事项综合查询网站的更新,恒瑞医药自主研发的PD-1单抗注射用卡瑞利珠单抗的审批状态已经更新为“审批完毕-待制证”,这意味着,卡瑞利珠单抗(SHR-1210,商品名为艾立妥)正式在国内获批,用于至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤患者的治疗,这也是第三个获批上市的国产PD-1单抗药物。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#PD-1单抗#
68