「病例报告」新型RET融合突变的奥希替尼耐药,双重EGFR加RET阻断耐药性
2023-05-30 找药宝典 网络 发表于上海
新型RET融合突变的奥希替尼耐药,双重EGFR加RET阻断耐药性
奥希替尼耐药机制大致可分为两类:EGFR依赖性和EGFR非依赖性。最常见的EGFR非依赖机制涉及以下基因的扩增:MET、HER2 和 PI3KC。致癌融合也是奥希替尼获得性耐药的驱动因素。ALK或ROS1 融合的奥希替尼耐药病例已显示出对成熟的 ALK/ROS1-TKIs 的客观反应 (OR),但RET融合多变且罕见,目前RET融合的奥希替尼耐药还没有最佳和最安全的治疗方法。下面分享两个病例Selpercatinib+奥希替尼、Pralsetinib+奥希替尼联合治疗奥希替尼耐药反应良好。
RET融合
RET融合是NSCLC的驱动基因之一,比例约2%,Selpercatinib和Pralsetinib已于2020年批准用于一线治疗晚期RET融合阳性非小细胞肺癌成人患者。同时,RET融合也是奥希替尼的耐药机制之一,比例约5%。
RET受体酪氨酸激酶可以激活许多下游信号通路,包括MAPK,PI3K和ERK,进而调节细胞生长和存活。迄今为止,至少已经鉴定出7个RET融合伴侣基因(KIF5B,CCDC6,CUX1,TRIM33,NCOA4,KIAA1468和KIAA1217)。形成的融合复合物导致 RET 酪氨酸激酶的组成性激活和未经检查的下游信号传导。
Case 1
患者信息:女性,73岁
主诉:因疲乏和咳嗽就诊
入院检查:胸部CT提示左上叶和下叶肺病变,分别约为5 cm。PET-CT显示转移性疾病,累及纵隔、双侧肺门、左腋窝、双侧锁骨下淋巴结和颈部淋巴结。行支气管镜检查和支气管内超声,对淋巴结进行活检,病理与非小细胞肺腺癌一致。基因检测示EGFR L858R点突变。
奥希替尼治疗:患者开始服用奥希替尼(80mg,qd),治疗仅两个月后,左上叶和下叶肺肿块的大小就减少了50%。由于3级肝酶升高,短暂中断治疗,当再次使用时,患者肝酶保持在正常范围内。
CGN-RET融合突变对奥希替尼产生耐药性:奥希替尼治疗近24个月后,患者再次检查发现有一个 7mm的环状增强病灶,涉及右侧矢状旁中央后回,被认为是颅内转移性病灶。此外,还注意到患者左下叶和中叶肺肿块的大小间隔增长。患者接受了4个周期的卡铂联合培美曲塞,随后接受2个周期的培美曲塞维持治疗。
尽管如此,患者仍经历进展性疾病,并发展出新的孤立性脑损伤。最终对扩大的左下叶肺肿块进行CT引导活检,并再次证明存在中分化肺腺癌。第二代测序揭示了一种新的CGN-RET融合突变的存在。
奥希替尼+selpercaptinib治疗反应良好:针对以上发现,患者开始服用RET抑制剂selpercaptinib(120mg)+奥希替尼(80mg)联合治疗。开始联合治疗后出现4级腹泻,selpercaptinib剂量减少至80mg。治疗6周后,患者对治疗有良好的反应,如图1所示。

图1. 胸部CT与selpercaptinib联合奥希替尼开始前(左)和(右)后66周的对比,左下肺结节大小消退。
不幸的是,患者出现消化道出血,需要长期住院治疗,随后在护理机构康复,艰难梭菌感染和明显的失调进一步复杂化。最终,她被过渡到临终关怀,病人在家中去世。
Case 2
患者信息:女性,62岁
入院检查:患者因疑似垂体腺瘤接受了颅内手术。对癌症相关基因分析显示:转移性肺腺癌(免疫组化 CK7+/TTF1+)与EGFRex19del p.E746_A750delELREA 和PD-L1表达。PET-CT扫描检测到左肺上叶有肿瘤,双肺、纵隔淋巴结和 L2 椎有多发转移,对应 T3N2M1c。
一线厄洛替尼,二线奥希替尼治疗:患者接受一线厄洛替尼治疗,15 个月后观察到原发肿瘤和纵隔淋巴结转移的进展。淋巴结活检和 DNA-NGS 分析揭示了原始EGFR ex19del 和新的EGFR突变 p.T790M。患者开始使用二线奥希替尼(80 mg,qd)。在该治疗的第4、7和13个月进行检测未显示 EGFR突变。
然而,在15个月后观察到两个肝转移。其中一个活检的 DNA-NGS 分析显示持续的EGFRex19del 和 p.T790M 突变,同时出现在血浆 cfDNA 中。此外,在该转移中发现了两种推定的耐药机制, MDM2扩增(19 个基因拷贝)和错义PTEN取代 p.C124S。没有进一步的可选靶向治疗方案,患者只接受了三个周期的卡铂-培美曲塞,同时继续使用奥希替尼,但由于骨髓毒性无法耐受更多化疗。
ANK3 - RET融合产生奥希替尼耐药性:对肝转移RNA进行的补充 NGS 分析显示ANK3-RET染色体10q上的融合。从奥希替尼前活检分离RNA的回顾性 NGS 未显示ANK3 - RET融合,这证实 ANK3 - RET融合是在奥希替尼治疗期间获得的。因其他RET融合已被报道为对 EGFR-TKI 获得性耐药的机制,所以可以解释为疾病进展原因。
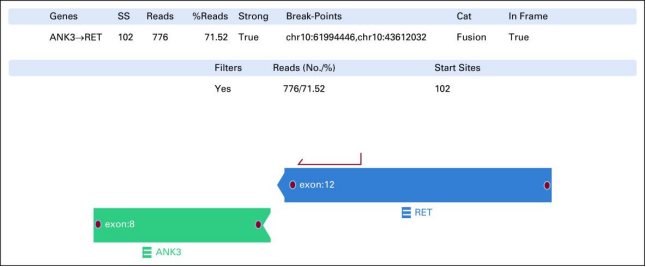
图2. 染色体 10q 上的基因间ANK3-RET融合
奥希替尼+ pralsetinib持续OR 超过12 个月:患者开始接受 pralsetinib (400 mg,qd)+奥希替尼(80 mg,qd)联合治疗。2 周后,联合方案因间质性肺炎而短暂中断,类固醇治疗后完全消退。此后减少联合方案剂量:奥希替尼减量至40 mg ,pralsetinib减量至200 mg,恢复联合TKI治疗,没有出现额外的不良事件。
1个月后进行的第一次评估显示混合反应,原发肿瘤消退,一个肝转移消失,另一个肝转移。在4周后的第二次评估中,发现原发肿瘤进一步缩小,两处肝转移灶均消退。治疗5个月后观察到胸部和腹部疾病稳定。
评估显示腹部完全反应和单个胸膜病变轻微进展,病变活检显示PTEN突变和MDM2扩增合。因此,为了控制胸膜病变,将奥希替尼剂量重新增加至 80 mg,同时维持pralsetinib 200 mg。到目前为止,在治疗12个月后进行的最后一次 PET-CT 显示持续的腹部完全反应和胸部SD。
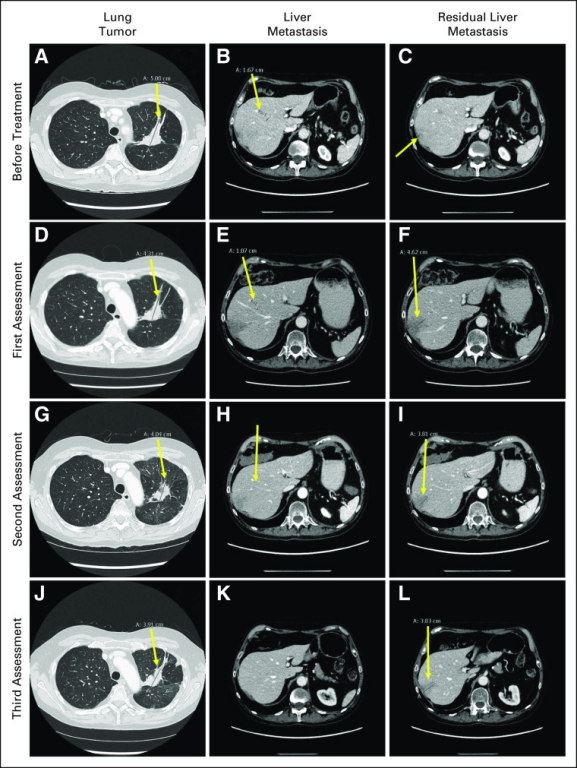
图3. 对奥希替尼和 pralsetinib 联合治疗的反应
治疗前:(A) 左上叶肺部肿瘤(5.1 cm),(B) 肝转移(1.7 cm)和 (C) 残余肝转移(不可测量)。第一次评估:(D) 左上叶肺部肿瘤(4.3 cm),(E) 肝转移(1.1 cm)和 (F) 残余肝转移(4.6 cm)。第二次评估:(G) 左上叶肺肿瘤(4.0 cm),(H) 肝转移(不可测量),和 (I) 残余肝转移(3.8 cm)。第三次评估:(J) 左上叶肺肿瘤(3.9 cm),(K) 肝转移(不可见)和 (L) 残留肝转移(3.8 cm)。
案例讨论
尽管奥希替尼有希望,但由于新的耐药机制的出现,治疗失败最终会发生。致癌融合在一小部分对奥希替尼产生耐药性的患者中充当驱动突变。案例1中患者发生的CGN-RET融合,迄今为止尚未在文献中报道过。
RET抑制剂selpercatinib与奥希替尼或阿法替尼联合治疗完全抑制了ERK和AKT磷酸化,证明可以通过双重EGFR加RET阻断来克服获得性耐药性。在临床环境中也观察到了针对EGFR和RET突变NSCLC的联合治疗的效用。在一组 12 名具有 RET 融合的晚期 EGFR 突变 NSCLC 患者中,使用selpercatinib和奥希替尼产生有利的治疗反应和持久益处,再次证明在临床环境中可以通过双重 EGFR 加 RET 阻断来克服获得性耐药性。
在一组 41 名使用二线奥希替尼取得进展的患者中,确定了两名具有获得性CCDC6-RET和一名具有NCOA4-RET融合的患者,使用奥希替尼+pralsetinib联合治疗,持续OR为4个月。Case 2中二线奥希替尼取得进展后,发生了ANK3-RET融合,将奥希替尼与pralsetinib 联合使用后,持续OR已超过12个月,据我们所知,这是迄今为止报告的奥希替尼联合RET-TKI 组合最长的OR。
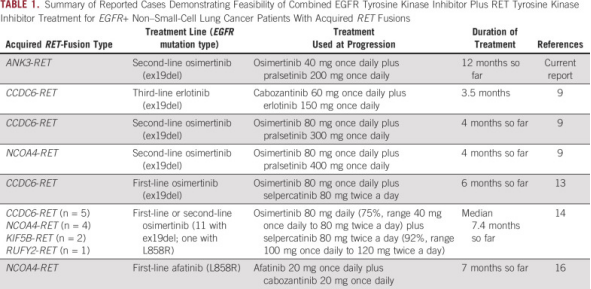
表1. 证明 EGFR 酪氨酸激酶抑制剂联合 RET 酪氨酸激酶抑制剂治疗具有获得性RET融合的EGFR + NSCLC的可行性的报告病例摘要
随着分子检测变得越来越普遍,它无疑将为促进NSCLC肿瘤发生的异质分子事件提供更广泛的见解。在各种获得性突变的情况下,联合TKI抑制剂治疗可能会在晚期NSCLC的治疗中变得更加普遍。有必要对最佳 TKI 抑制剂组合和安全性进行进一步研究。
参考文献:1.Mirshahidi H, Kwon S M S, Romagnolo A, et al. Advanced EGFR-mutant NCSLC resistant to osimertinib therapy as a result of a novel CGN-RET fusion mutation with favorable response to combined osimertinib and selpercaptinib, case report[J]. Current Problems in Cancer: Case Reports, 2023: 100246.
2.Urbanska EM, Sørensen JB, Melchior LC, Costa JC, Santoni-Rugiu E. Durable Response to Combined Osimertinib and Pralsetinib Treatment for Osimertinib Resistance Due to Novel Intergenic ANK3-RET Fusion in EGFR-Mutated Non-Small-Cell Lung Cancer. JCO Precis Oncol. 2022 Jul;6:e2200040. doi: 10.1200/PO.22.00040. PMID: 35797511; PMCID: PMC9489192.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








学习打卡
61
双重E G F R加r e t阻断耐药性
91