NEJM:血栓性微血管病全新诊疗进展
2014-08-28 sjtuwalker 丁香园
血栓性微血管病 (thrombotic microangiopathy,TMA) 是一组具有共同病理特征的急性临床病理综合征,分为遗传性和获得性,主要表现为内皮细胞肿胀脱落、内皮下绒毛状物质沉积和血管腔内血小板聚集形成微血栓、血管腔内栓塞及红细胞碎裂等微血管系统异常。 TMA临床上主要表现为血小板减少、溶血性贫血和微循环中血小板血栓造成的器官受累,其临床表现与TMA 的病变范围和累及不同器官
血栓性微血管病 (thrombotic microangiopathy,TMA) 是一组具有共同病理特征的急性临床病理综合征,分为遗传性和获得性,主要表现为内皮细胞肿胀脱落、内皮下绒毛状物质沉积和血管腔内血小板聚集形成微血栓、血管腔内栓塞及红细胞碎裂等微血管系统异常。
TMA临床上主要表现为血小板减少、溶血性贫血和微循环中血小板血栓造成的器官受累,其临床表现与TMA 的病变范围和累及不同器官造成的功能障碍有关。
该病涉及的临床科室非常广泛,患者往往可能在不同的科室,如肾脏内科、血液科、神经内科、妇产科、皮肤科、心血管内科和呼吸科等就诊,如接诊医生缺乏对该病的认识,往往会造成严重的误漏诊,故提高对该类疾病的认知度已成为目前国内外相关专业领域内的关注热点。
在这篇文章中作者认为TAMs包括远远不止溶血性尿毒症综合征 (hemolytic uremlc syndrome,HUS)和血栓性血小板减少性紫癜(thrombotic throm-bocytopenic purpura,TTP)两种疾病,共介绍了九种TMA:
1、四种遗传性TMA,包括ADAMTS13缺乏介导的TMA(TTP)和补体、代谢、凝血介导的TMA;
2、获得性TMA,包括ADAMTS13缺乏介导的TMA(TTP)、志贺毒素介导的TMA(ST-HUS)、药物介导的TMA(免疫反应)、药物介导的TMA(药物毒性反应)、补体介导的TMA,同时对各种TMA的病因、临床表现以及治疗作了介绍。

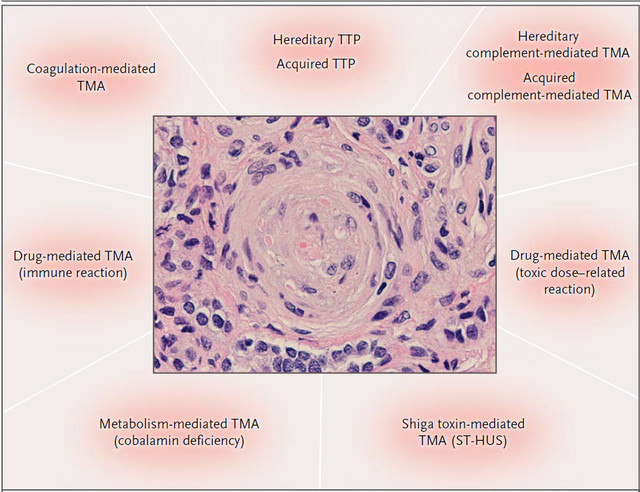
九种不同亚型TMA病理特点


TMA历史大事记
TTP
病因
1924年,Moschcowitz报道了首例TTP患者。患者女性,16岁,有乏力、面色苍白、紫癜和偏瘫等症状,14天后因心脏衰竭死亡。病理活检结果显示患者全身多处器官(包括肾脏)终末微动脉和毛细血管透明血栓形成。这是TMA的首次报道,同时也是TTP首例,主要由ADAMTS13缺乏介导引起。
在二价金属离子条件下一种金属蛋白酶切割vWF,其缺乏可导致超大vWF多聚体形成,这种金属蛋白酶即vWFCP,vWFCP基因定位于9q34 (C9ORF8),全长37kb ,有29个外显子,编码1427个氨基酸残基的蛋白。
研究表明该蛋白为具有凝血酶敏感蛋白1基序的裂解素和金属蛋白酶家族新成员(a disintegrin and metalloproteinase with thrombospodin type 1 motif,ADAMTS) 并被命名为ADAMTS13。ADAMTS13结构缺陷与遗传性TTP密切相关,而后天获得性ADAMTS13自身抗体则会造成获得性TTP。获得性TTP的发病率成人远高于儿童,危险因素包括年龄、种族和性别。
临床表现和诊断
TTP起病往往急骤,典型病例有发热、乏力、虚弱、少数起病较缓慢,有肌肉和关节痛等前驱症状。遗传性TTP的主要临床表现有溶血性贫血、血小板减少,往往伴有神经系统症状和其他器官受累。ADAMDTS13缺乏以及ADAMDTS13自身抗体抑制剂的缺失可以诊断遗传性TTP,确诊需要有ADAMDTS13基因的突变。
获得性TTP的临床特点不一,部分患者临床表现并不明显,部分患者则较危重。常见的临床表现包括乏力、胃肠道症状、过敏性紫癜和局灶性神经功能异常,但大约三分之一的患者无神经系统症状,多数患者肌酐可轻度升高。诊断标准为排除其他原因导致的溶血性贫血和血小板减少,因此,需要排除其他类型的TMA。ADAMDTS13水平低于正常的10%有助于诊断获得性TTP。
治疗
TTP的首选治疗方法为血浆置换ADAMDTS13,含ADAMDTS13的凝血因子VIII可有效治疗严重的过敏反应。虽然许多患者只在血小板减少或出现症状时才需要输血,其他一些患者仍然需要定期进行预防性血浆输注。血浆置换开始治疗前,获得性TTP的生存率大概在10%,一项临床随机研究结果表明,血浆置换治疗可使患者的生存率提高到78%。
糖皮质激素也是TTP的标准治疗方法,如果出现其他一些复杂的症状,也可适当运用利妥昔单抗和免疫抑制剂;很少有患者需要透析。长期的随访结果表明,获得性TTP患者复发和先天性缺损、重度抑郁症、系统性红斑狼疮、高血压的风险增加,重的甚至可以导致死亡。
补体介导的TMA
病因
补体旁路途径的激活可导致补体介导的TMA。与其他两条补体激活途径不同,C3自发水解为C3b,降解产物释放增加可导致旁路途径的持续激活。在调节失控的情况下,C3b在组织中的沉积显著增加,从而导致C5b-9末端补体复合物(也称为膜攻击复合物)的增加,损伤正常的细胞。
临床表现和诊断
补体介导的TMA患者会出现严重的急性肾损伤和高血压。目前的诊断标准包括:血清肌酐水平的升高、溶血性贫血、血小板减少、ADAMDTS13活性>5%、无志贺毒素感染。需要说明的是,该诊断标准并不特异,其他一些溶血性贫血、血小板减少的TMA患者也会出现类似的症状。
目前市面上的一些补体遗传学诊断可以提供更加准确的结果,给诊断带来了极大方便。需要注意的是,C3、C4以及补体因子H、B、I水平正常并不能排除补体介导的TMA。
治疗
抗补体治疗可用于补充血浆置换治疗。目前市场上唯一可用的抗补体剂是亚力兄制药公司的Eculizumab,Eculizumab是重组人抗补体C5单克隆抗体,它可能仅对C5有突变的患者有效。对于抗补体因子H抗体的患者,抗补体治疗作为初始治疗方案是一种合理的选择,但也应该考虑使用免疫抑制剂降低抗体的滴度。
Eculizumab的价格非常昂贵,一年需要614736美元,治疗时还需考虑患者的经济因素。同时,Eculizumab导致的脑膜炎双球菌感染也需注意。Eculizumab出现之前,终末期肾脏疾病发生率、肾脏移植后复发率以及死亡率很大程度上取决于患者是否有基因突变,抗补体治疗很大程度上将提高患者生存率。
志贺毒素介导的TMA(ST-HUS)
病因
产生志贺毒素的大肠杆菌是牛体内常见的肠道细菌,这与流行性ST-HUS主要发生在农村也相一致,爆发的主要原因是水源、牛肉制品、蔬菜以及其他食品的污染。志贺毒素与内皮细胞、肾系膜细胞以及上皮细胞上Gb3的结合可导致细胞损伤。
Gb3的结合、内吞作用、逆向运输、细胞内志贺毒素易位以及核糖体的失活可导致细胞凋亡。志贺毒素同样可以促进细胞活化、炎症、血栓形成,且可以通过诱导内皮细胞释放vWF因子促进血栓形成。
临床表现和诊断
进食被志贺毒素污染的食物数天后可出现剧烈腹痛、腹泻,腹泻常为血性。胃肠道症状缓解后患者可出现血小板减少和肾功能衰竭。急性结肠炎期可通过大便培养诊断志贺毒素感染,但当出现ST-HUS时,大便培养可阴性。
治疗
ST-HUS的治疗目前仍然是对症支持治疗,早期积极的水化治疗可起到保护肾脏的作用,多数ST-HUS患者通常需要透析。血浆置换和抗补体治疗在本病治疗中的作用还不明确。急性期过后患者仍会出现高血压和神经系统症状,极少数患者会出现终末期肾脏病。
药物介导的TMA(免疫反应)
病因
某些药物的特殊结构可促进多种细胞表面药物依赖性抗体与抗原的结合,例如,奎宁依赖性抗体可部分通过激活内皮细胞来介导TMA。
临床表现和诊断
服药后数小时内突然出现无尿性急性肾损伤,伴有其他器官的全身症状高度考虑药物介导的TMA,之前可能也会有相关的病史。奎宁介导的TMA可能会被忽视,因为其一般数年后才发病,这类患者一般之前服用过奎宁片或含有奎宁的饮料。药物依赖性抗体检查阳性可支持该病诊断,但结果阴性也不能排除该诊断。
治疗
支持治疗和避免服用此类药物可能是唯一有效的治疗方案。由于患者症状可能是TTP或药物介导的原因不确定,这时可用血浆置换治疗。这类患者常出现慢性肾脏疾病伴高血压,但晚期肾脏疾病少见。
药物介导的TMA(药物毒性反应)
病因
药物介导的肾脏毒性损伤机制有很多,其中,钙调神经磷酸酶抑制剂(如环孢霉素和他克莫司)可导致内皮功能障碍、增加血小板聚集,可能通过抑制前列腺素的分泌来损伤肾脏。抑制肾脏内皮细胞和足细胞VEGF的功能可逐渐导致肾小球TMA的发生。
临床表现和诊断
典型的临床表现是肾脏功能的逐渐丧失以及高血压,静脉使用大剂量的吗啡可导致严重的TMA发生。
治疗
支持治疗和避免服用此类药物可能是唯一有效的治疗方案。对于某些药物,例如钙调神经磷酸酶抑制剂,减少剂量即可,不必停药。此类患者溶血性贫血和血小板减少通常可治疗,但肾功能衰竭可持续存在。
代谢介导的TMA
病因
编码甲基丙二酸尿症和高胱氨酸尿症的C类蛋白(MMACHC)基因出现纯合子或复合杂合子突变可导致钴胺素代谢的异常。甲基维生素B12的缺乏可导致同型半胱氨酸血症、血浆蛋氨酸水平的下降以及甲基丙二酸尿症。钴胺C的代谢异常可导致血小板活化、活性氧的产生、内皮功能障碍、组织因子表达以及凝血系统的激活。
临床表现和诊断
钴胺C病的婴儿可出现各种发育异常疾病。成年患者可出现溶血性贫血、血小板减少、急性肾损伤以及高血压等临床表现。
治疗
肠胃羟钴胺是治疗婴儿钴胺C病的主要药物。具有上述临床表现的成年患者,如果抗补体治疗无效,应怀疑患者细胞内代谢维生素B12存在缺陷,可完善一些常规检查,如果患者有同型半胱氨酸血症、血浆蛋氨酸水平的下降、甲基丙二酸尿症、维生素B12水平正常应考虑钴胺C病,治疗上可予羟钴胺、甜菜碱和亚叶酸治疗。
钴胺C病的婴儿常可出现神经系统后遗症,大约40%的患者会出现慢性肾脏病、高血压、蛋白尿。替代治疗可预防终末期肾脏疾病和TMA的复发。
凝血介导的TMA
病因
血栓调节素在凝血介导的TMA中的作用还不清楚。DKGE在凝血介导的TMA中的作用已被部分研究证实,几乎所有的患者都有DKGE基因纯合子或杂合子的突变,DKGE基因杂合突变的患者无明显的临床表现。
编码DKGE的基因出现纯合突变可出现功能的丧失,导致PKC的激活,PKC的激活可促进血栓因子的上调以及VEGF受体的下调。DKGE基因突变同样也可导致VEGF功能的下降以及肾足细胞损伤。以上这些过程促进了血血栓形成。凝血系统和补体系统在TMA的发病机制中可能存在一定作用。
临床表现和诊断
伴有DKGE基因突变的急性肾损伤患者高度考虑此病,大部分患者的发病年龄在1岁。
治疗
血浆输注和血浆置换以及免疫抑制剂治疗效果在本病中看法不一,在接受抗补体治疗的过程中患者可能复发。终末期肾脏疾病在此疾病中很常见,4例凝血介导的TMA患者接受了肾移植,1例有复发性肾损伤。
原始出处
George JN1, Nester CM.Syndromes of thrombotic microangiopathy.N Engl J Med. 2014 Aug 14
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







这在大医院容易见到
195
#血栓性#
93
非常好的内容!
116
#血管病#
94
:-)
174
#血栓性微血管病#
138
#微血管#
65