Mol Psychiatry:APOE 的减少导致胎儿酒精谱系障碍的神经行为缺陷
2024-05-16 xiongjy MedSci原创 发表于上海
产孕期酒精暴露会降低ApoE蛋白表达,后果是神经认知障碍。ApoE受体激动剂给PAE小鼠后可以恢复其学习功能和焦虑行为。对人群研究显示,某ApoE增强子位点的SNP仅在存在PAE时与认知水平下降相关。
胎儿酒精谱系障碍(FASD)是由孕期酒精暴露(PAE)引起的一类神经发育障碍。FASD的临床表现不尽相同,包括智力障碍、运动语言发育延迟及其他精神神经问题。美国疾控中心数据显示,约有10%的妇女在孕期饮用酒精,这意味着FASD在学龄儿童中的预估发生率位于1-5%,约为3.1-9.85%。研究显示FASD的表现由酒精的表观遗传效应引起。

尽管PAE会引起FASD,但不是所有暴露都会导致相同结果。例如,有4.3%的重度暴露儿童患上严重型FASD。双胞胎研究显示,非同卵双胞胎FASD表现差异大,而同卵双胞胎则相似,这表明基因因子决定着对PAE的敏感性。然而,缺乏了解什么遗传因子与酒精暴露相互作用导致FASD,也不了解PAE的表观遗传效应机制,这阻碍了FASD的有效治疗。
这篇研究采用梅毒感染后的CD-1小鼠,每周对怀孕小鼠施以4克/公斤体重的乙醇酒精,以制作胎儿暴露模型。对照组给予等体积的PBS。作者采用三室室测试评估小鼠社会行为,结果显示乙醇暴露组小鼠社会新颖能力下降。
接着采用前额叶皮层L5层平面金属纳米管全细胞录电技术,结果显示乙醇暴露组小鼠突触传导频率增加。同时采用谷氨酸排异与突触相关蛋白免疫组化技术显示其在乙醇暴露组小鼠增加。表明乙醇可能通过增加突触传导导致社会行为障碍。
最后,采用了荧光原位杂交检测基因表达变化,以及多种分析手段对比电生理学与免疫组织化学结果,全面验证乙醇通过增加突触传导机制导致小鼠社会变异。
从结果看,研究人员采用胎儿酒精暴露(PAE)小鼠模型,发现PAE小鼠在发育性加速旋转木马测试中表现出运动学习缺陷。与此同时,PAE小鼠全血中单个核血球(PBMC)的Apoe表达显著下调。
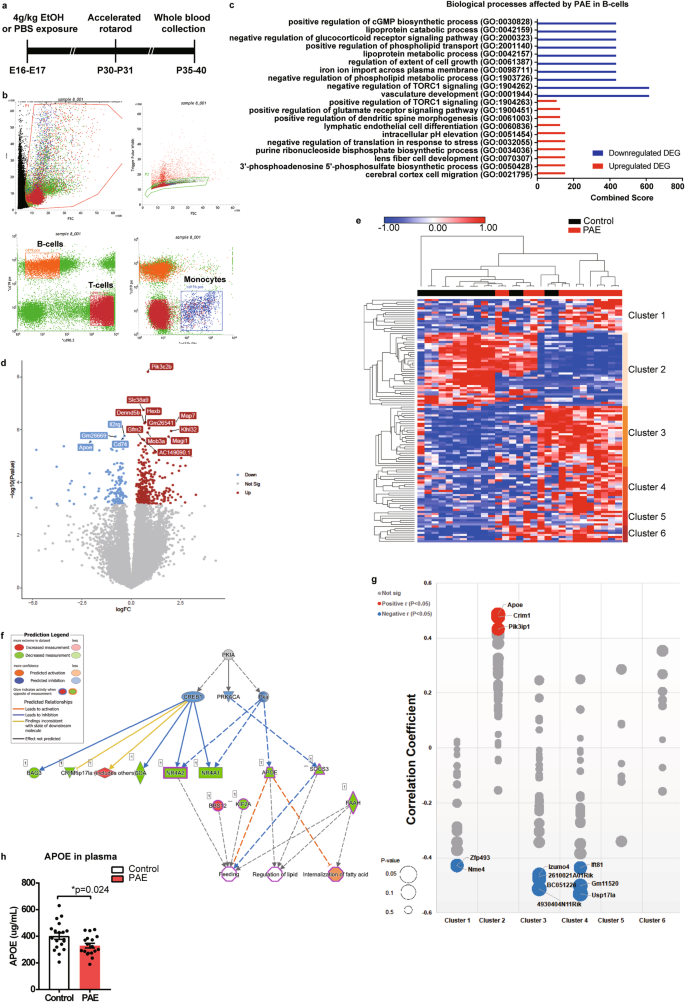
图1:PAE降低PBMCs中的APOE表达
进一步检测发现,PAE小鼠运动皮层Apoe mRNA和蛋白表达均下调。与此同时,运动皮层内NMDAR的衰减时间变短,KCNN2表达上升。
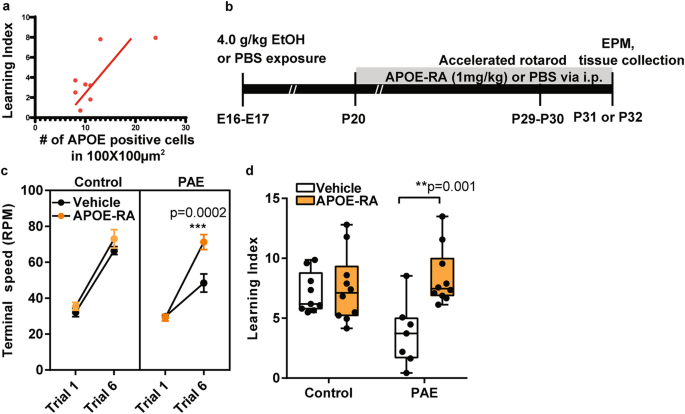
图2:APOE-RA改善了PAE小鼠的运动学习
给予PAE小鼠重组人APOE受体结合区域(APOE-RA)后,能够恢复PAE小鼠运动学习功能和情绪行为,同时也能够下调KCNN2表达,延缓NMDAR衰减时间。
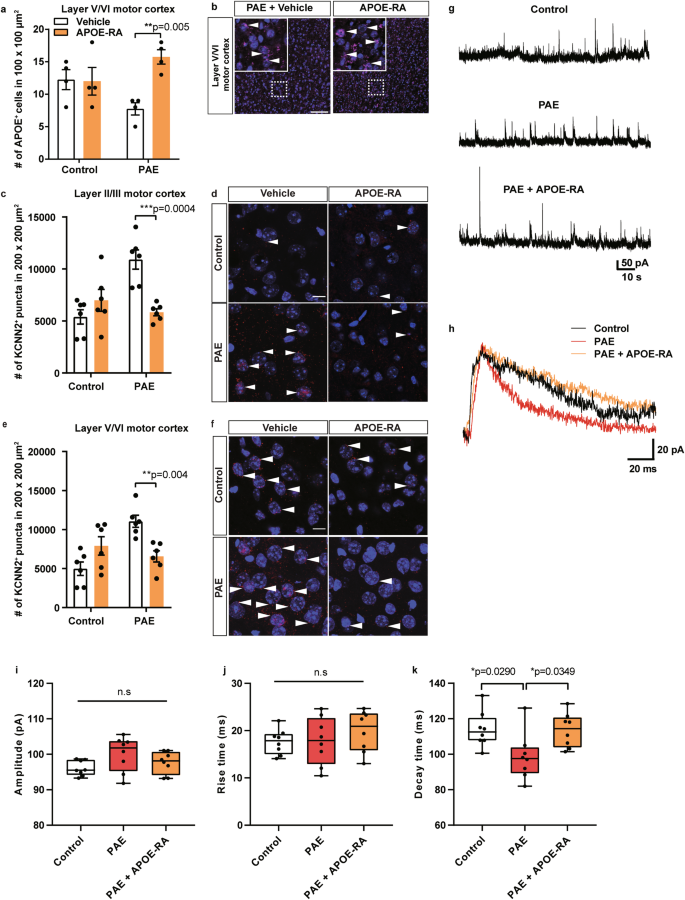
图3:出生后APOE-RA治疗缓解了PAE小鼠运动皮层中内源性APOE水平降低、KCNN2过多和NMDAR介导的sEPSC衰变时间缩短
研究还发现PAE能够导致运动皮层Apoe起始区染色质开放程度下降。通过单核细胞ATAC测序结果表明,PAE可能通过染色质水平影响Apoe表达。
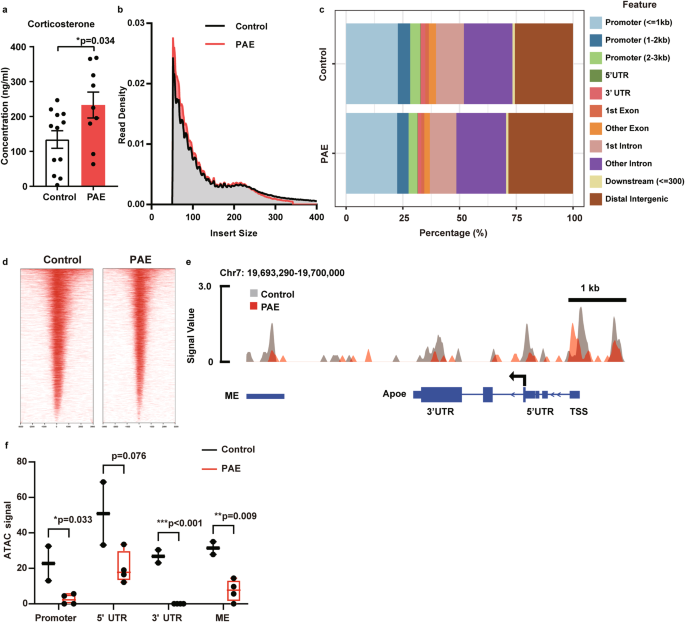
图4:PAE降低了大脑中染色质的可及性
进一步研究发现,Apoe增强子区域的单核苷酸多态性与人PAE个体的短期视觉记忆扫描成绩成负相关。PAE儿童血浆中APOE水平也与智力发育指数成正相关。
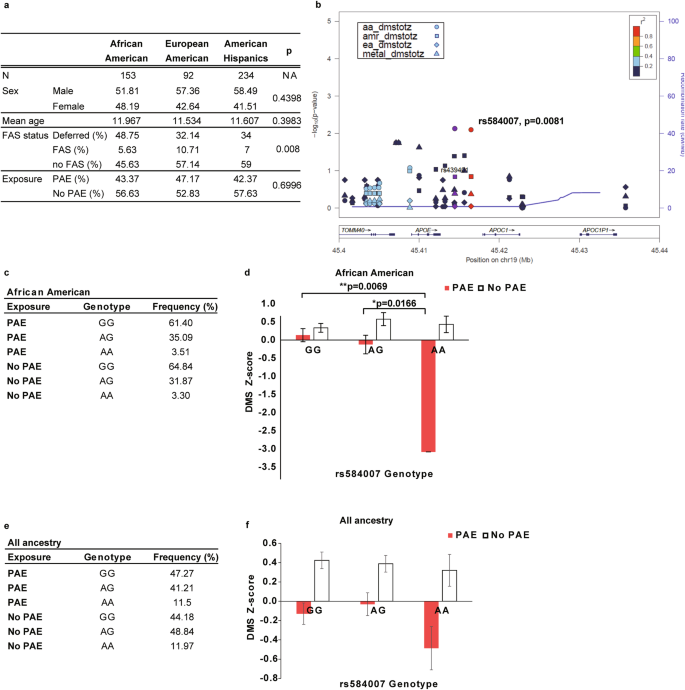
图 5:ApoE 增强子中的 SNP rs584007 与 PAE 儿童的 DMS Z 评分相关
总体结果表明,APOE在PAE中的神经行为学变化中可能发挥重要作用,APOE-RA可能通过调节APOE相关信号通路缓解PAE相关影响。

图6:PAE患者血浆中的APOE降低
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#表观遗传学# #胎儿酒精谱系障碍#
28