骨肉瘤新辅助化疗下的保肢手术
2013-07-27 中国医学科学院肿瘤医院 王佳玉 徐兵河 张鑫鑫 于胜吉 中国医学论坛报
骨肉瘤的外科技术在20世纪70年代得到快速发展,使部分患者可接受人工假体置换而避免截肢。研究者为避免患者在等待人工假体制作期间无治疗,设计了一个术前化疗方案T5(甲氨蝶呤+长春新碱+多柔比星),即最早的新辅助化疗方案。后续美国儿童肿瘤协作组(POG)的随机对照研究及德奥肉瘤协作组(COSS)、美国纪念斯隆-凯特林癌症中心的回顾性分析均提示新辅助化疗并不影响生存,且可诱导肿瘤细胞死亡
骨肉瘤的外科技术在20世纪70年代得到快速发展,使部分患者可接受人工假体置换而避免截肢。研究者为避免患者在等待人工假体制作期间无治疗,设计了一个术前化疗方案T5(甲氨蝶呤+长春新碱+多柔比星),即最早的新辅助化疗方案。后续美国儿童肿瘤协作组(POG)的随机对照研究及德奥肉瘤协作组(COSS)、美国纪念斯隆-凯特林癌症中心的回顾性分析均提示新辅助化疗并不影响生存,且可诱导肿瘤细胞死亡,促使肿瘤边界清晰化,从而增加手术保肢率。
新辅助化疗方案的发展
早期的骨肉瘤辅助治疗研究使用包含多柔比星(ADM)、顺铂(DDP)、博来霉素、环磷酰胺、异环磷酰胺(IFO)及大剂量甲氨蝶呤(HD-MTX)在内的至少3种以上化疗药物方案。此后陆续有研究证实含ADM、DDP±HD-MTX短疗程强化治疗即可达到多药联合化疗的长期生存结果。骨肉瘤的新辅助化疗方案多参考辅助化疗方案。
一项Ⅱ期骨肉瘤新辅助化疗研究中位随访64个月的结果显示,EPI方案(DDP+IFO+表柔比星)的5年无病生存(DFS)率和总生存(OS)率分别达41.9%和48.2%。在另一项多中心新辅助化疗研究中,IFO联合依托泊苷(VP16)的病理学完全缓解(PCR)率高于HD-MTX+ADM(56%对39%),但两组患者的5年OS率及DFS率相似。
另外,研究发现,不管用何种方案化疗,对新辅助化疗有较佳病理反应是影响预后的重要因素。一项入组881例患者的骨肉瘤新辅助化疗研究显示,DFS和OS与病理反应密切相关,病理反应较佳与较差组的5年DFS率分别为67.9%和51.3% (P<0.0001), 5年OS率分别为78.4%和63.7%(P<0.0001)。一项来自儿童肿瘤协作组的研究也证实了这一点:病理反应较佳者的8年术后无事件生存(EFS)率和OS率分别为81%和87%,远高于反应较差者(分别为46%和52%)。
新辅助化疗方案的具体选择
骨肉瘤新辅助化疗推荐药物为HD-MTX、IFO、ADM、DDP,可序贯或联合用药,每例患者要选用两种以上药物,动脉或静脉给药(MTX、IFO不适合动脉给药)。我国学者推荐剂量范围为:MTX 8~10 g/(m2·2w),IFO 15 g/(m2·3w),ADM 90 mg/(m2·3w),DDP 120~140 mg /(m2·2w),用药时间为4~6个周期。目前对新辅助化疗是否可改善患者长期生存尚无统一认识。但可以肯定的是:化疗期间有足够时间进行保肢手术设计;新辅助化疗可诱导肿瘤细胞死亡,促使肿瘤边界清晰化,增加手术保肢率,使外科手术更易于进行;有效的新辅助化疗可降低术后局部复发率,而局部复发也对预后存在不利影响。对于术前化疗后仍不能切除的肿瘤,可行放疗。广泛切除术后经病理证实术前化疗反应佳者(术后病理提示,大于90%的肿瘤细胞坏死),术后应继续使用术前化疗方案。而对病理证实术前化疗反应不佳者,术后应改变化疗方案或增加剂量强度。
新辅助化疗后的保肢手术
新辅助化疗后的保肢手术是目前较规范的治疗。因骨肉瘤外科边界经化疗得到一定程度的缩小,可找出最佳边界实施广泛切除,从而达到局部根治的目的,并保留肢体功能。保肢手术在出现至今的30余年中得到快速发展。目前达成共识的保肢手术适应证为:①埃奈克(Enneking)分期ⅠA、ⅠB、ⅡA期和部分化疗敏感的ⅡB期患者,且主要血管神经未受累;②局部软组织条件允许,可达广泛切除;③无转移病灶或转移病灶可治愈;④全身情况良好,且保肢愿望强烈。
最初,当人工假体还未兴起时,常采用瘤段骨切除加关节融合术,但这种术式会造成关节功能完全丧失,渐被弃用。当各种骨填充物和人工假体出现后,骨肉瘤保肢手术获得快速发展。
在瘤段骨切除后,急需解决的是大范围骨缺损的修复问题。自体骨移植一直是骨移植修复的金标准,对范围较小的骨缺损,可采用带或不带血管蒂的腓骨、髂骨、锁骨移植等。但对于更大范围骨缺损,自体骨远不能满足需要,可采用同种异体骨移植。因同种异体骨来源广泛、生物活性强、便于保存、生物相容性佳,并可根据骨缺损形状行自行匹配而获广泛应用。
更多学者倾向于将同种异体骨与自体骨结合,在断端用自体骨移植,可加强移植骨的传导性和诱导性,加速骨融合,促进骨修复。也可对瘤段骨行灭活处理,再将其植回原处。瘤段骨灭活再植有费用低、操作简便、骨缺损匹配等优点,但有移植骨骨折、感染、骨坏死、灭活不全等风险。在实际应用中,骨肉瘤多发生于长骨干骺端近关节处,术中扩大切除可能波及关节的功能,此时单纯的植骨已不能满足需要。
人工假体对保肢技术的促进
人工假体置换术后可保留关节大部分功能,早期稳定性强、可承重,且避免了移植骨骨折、坏死等并发症。定制型假体有标准化组件系统,术前根据患者参数定制尺寸合适组件,不受假体大小限制,术后稳定性好。目前,采用骨水泥固定的肿瘤型旋转铰链式关节假体应用范围较广,术后可大部分保留关节功能,且患者满意度较高。对于儿童骨肉瘤,可延长型假体近年来得到更广泛的应用。无创可延长型假体在术后可采用物理方法在体外行假体延长,无须再次手术。假体置换术主要的并发症是假体松动和下沉,这是置换术失败而再次手术的主要原因,发生率约为52%。一旦假体松动,须进行翻修术,因而首次手术时即需要考虑到这一点。
近年来,将骨移植与假体置换结合,即同种异体骨-假体复合内植物成为骨肿瘤术中重建的重要发展方向。有研究表明,假体置换结合同种异体骨移植术的术后假体无菌性松动率低于单纯假体置换。二者结合的优势在于更多保留骨量,利于后续翻修,且软组织附着较好,肌肉功能恢复较快,便于术后早期活动和关节功能的恢复。随着保肢技术的不断进步,骨肉瘤的保肢治疗已进入良性发展轨道。相信随着更多化疗药物、辅助抗肿瘤药物及人工假体、骨填充材料的出现,骨肉瘤患者不仅能获得长久生存,且生存质量也能得到更大幅度的提高。
■典型病例
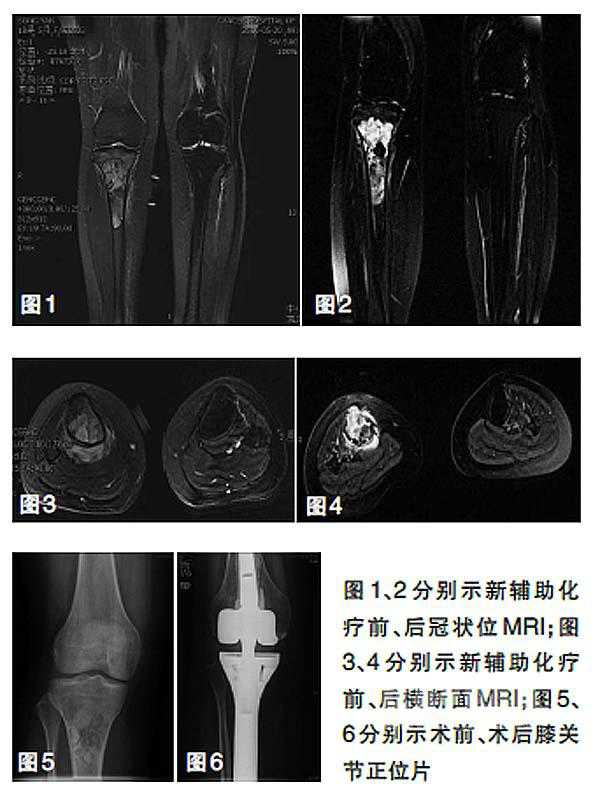
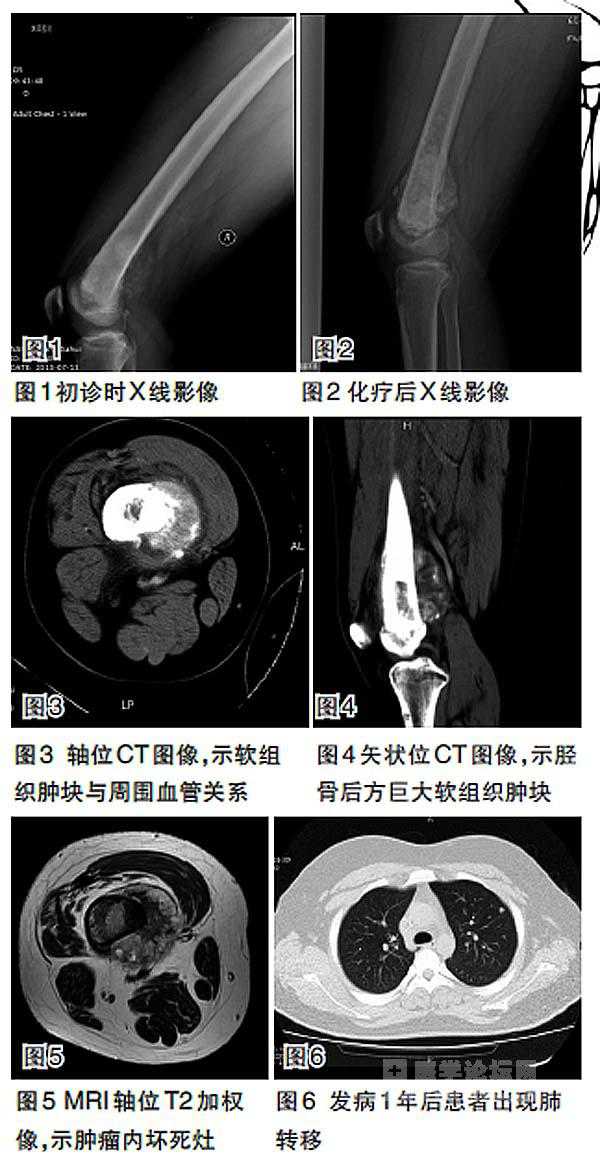
患者女性,19岁,以“右小腿疼痛半个月”入院。完善相关检查后,“右胫骨上段病变切开活检”结果为右胫骨骨肉瘤(T2N0M0)。行新辅助化疗1个周期(14天),方案为表柔比星150 mg、44h、d1,顺铂 150 mg、44h、d3+甲氨蝶呤 15g、d15。从横断面磁共振成像(MRI)可见,肿瘤在新辅助化疗后有所缩小,肿瘤周围软组织反应带范围也相应缩小。后行“右胫骨上段肿瘤瘤段截除、新轴心式膝关节置换术”,术后辅助化疗4周期(21天),方案为表柔比星 100 mg、24h、d1,异环磷酰胺 10 g、96h、d2~5。术后随访3年,患者下肢功能良好,无局部复发和远处转移。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#新辅助#
52