Nature:炎症性肠病的神秘面纱正在被揭开!
2024-09-04 Hanson临床科研 Hanson临床科研 发表于上海
本文通过遗传学、免疫细胞和微生物组的研究,科学家们正在逐步揭开IBD的发病机制,并为开发个性化治疗方案提供了新的希望。
炎症性肠病(IBD)是一种导致消化道长期炎症的疾病,包括溃疡性结肠炎(UC)和克罗恩病(CD)两种常见形式,它们都可能引起腹泻、贫血和腹部绞痛。这些疾病影响全球数百万人,给患者带来极大的生理和心理负担。IBD的发病原因复杂,涉及遗传和环境因素,且全球多个地区的发病率正在上升【1】。
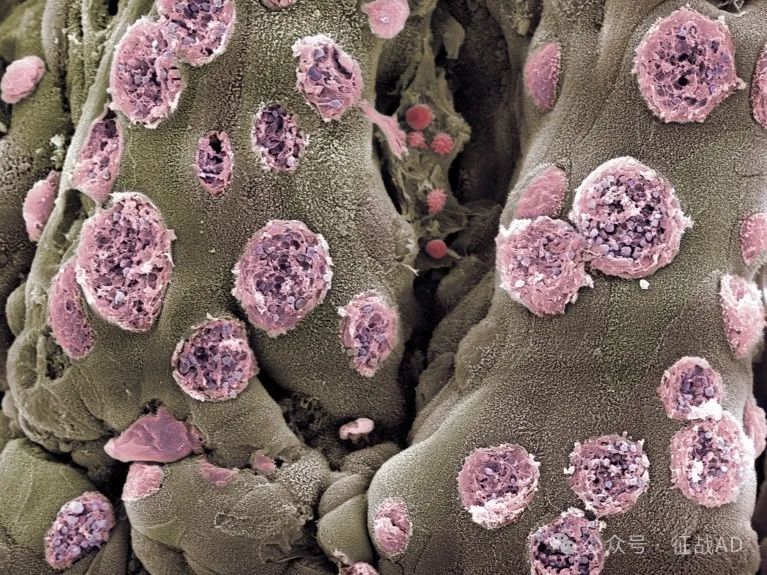
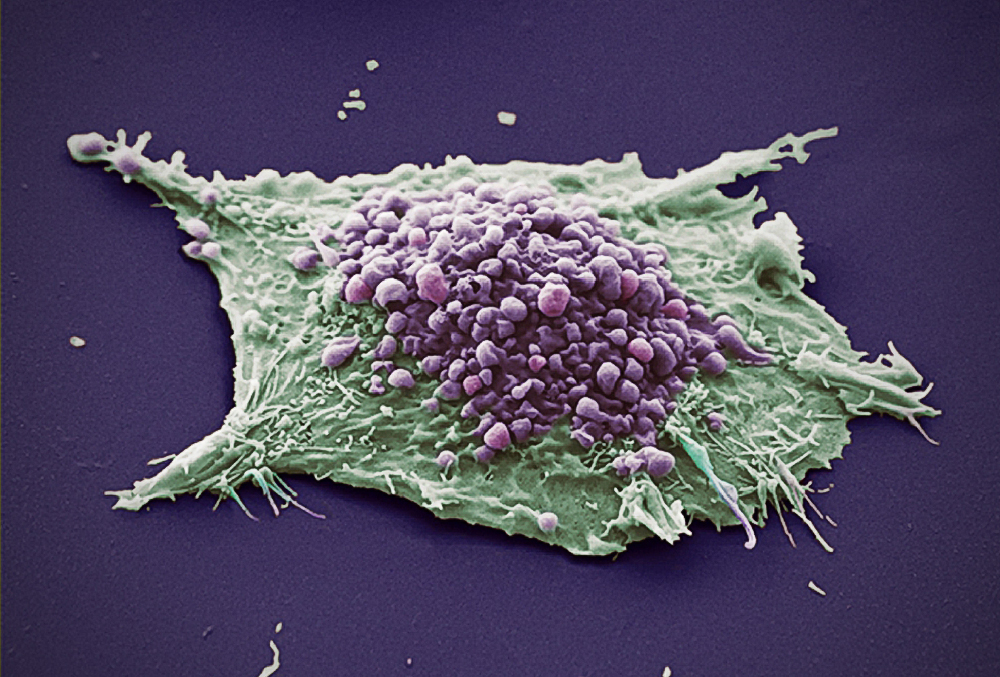
图1. 溃疡性结肠炎(UC)患者的肠道中生长着产生粘液的细胞(粉色)
图2. 克罗恩病(CD)是炎症性肠病的一种,通常会影响肠道
近年来,随着基因组学、免疫学和微生物组学等领域的快速发展,科学家们开始从分子层面深入探索IBD的病理机制。这些研究不仅有助于我们更好地理解IBD的复杂性,也为开发新的治疗策略提供了可能。此外,肠道微生物组与IBD之间的关系也是当前研究的热点。肠道微生物组是指居住在人体肠道中的微生物群落,它们与宿主的健康和疾病状态密切相关。研究表明,IBD患者的肠道微生物组成与健康人群存在显著差异,这些差异可能影响肠道的免疫反应和炎症状态。
2024年8月16日,Heidi Ledford 在 Nature 杂志新闻专栏发表了题为 The mysteries of inflammatory bowel disease are being cracked — offering hope for new therapies 的报道【2】。本文通过遗传学、免疫细胞和微生物组的研究,科学家们正在逐步揭开IBD的发病机制,并为开发个性化治疗方案提供了新的希望。

主要研究内容和结果
🔷 遗传学研究
研究者们对一个被称为“基因荒漠”的基因组区域进行了研究,发现了调控ETS2基因活性的DNA序列,该基因与免疫细胞的炎症反应有关。
-
遗传学研究的新发现:过去十年 IBD 的遗传学研究揭示了该疾病的复杂遗传背景,James Lee 等研究学者在 Nature 杂志上发表题为 A disease-associated gene desert directs macrophage inflammation through ETS2 的研究【3】,特别关注了一个通常被忽视的基因组区域——“基因荒漠”,他们在这个区域发现了一个调控炎症反应的“主调节器”,这是一段控制ETS2基因活性的DNA序列,ETS2基因活性的高水平会增强免疫细胞(巨噬细胞)促进炎症的能力。
-
MEK抑制剂的潜在应用:此外,研究还表明,MEK抑制剂这类药物可能通过抑制ETS2蛋白的激活来减轻炎症,尽管需要进一步研究以确保这些药物的安全性和有效性。这些发现不仅增进了我们对IBD遗传基础的理解,也为开发新的治疗策略提供了重要的线索。
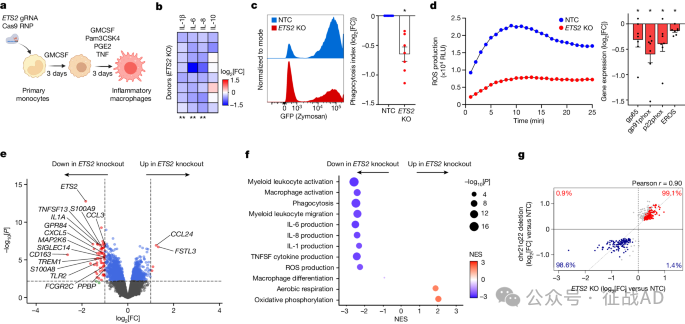
图3. ETS2 对巨噬细胞炎症反应至关重要
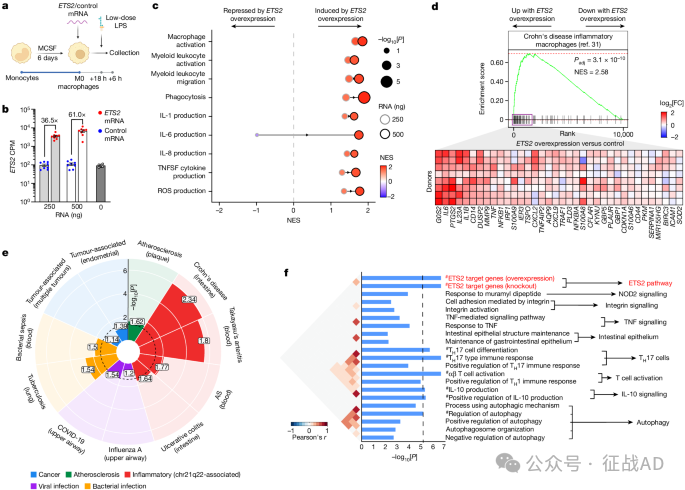
图4. ETS2 调控巨噬细胞炎症反应
🔷 免疫学研究:IBD患者体内的“流氓抗体”
英国纽卡斯尔大学的儿科免疫学家 Sophie Hambleton 及其团队在研究中发现,某些IBD患者体内产生了能够阻断肠道内抗炎蛋白IL-10活性的抗体,这种抗体的存在导致IL-10无法正常抑制炎症,从而引发IBD。在 NEJM 上发表的题为 Neutralizing Autoantibodies against Interleukin-10 in Inflammatory Bowel Disease 的报告中【4】,研究团队分析了两名IBD儿童的样本,发现这些儿童体内产生了能够阻断IL-10蛋白活性的抗体。在识别了IL-10与这些儿童疾病之间的联系后,对其中一名儿童进行了抗体消耗治疗,成功缓解了其症状。尽管目前尚不明确具体有多少IBD患者会产生这种自身抗体,但研究团队在成年IBD患者样本中也发现了这种抗体的产生。
这项研究揭示了IBD患者中存在一个特殊群体,他们的疾病可能与自身产生的抗体有关,这些抗体干扰了正常的抗炎机制。这一发现为开发新的治疗策略提供了重要的线索,特别是对于那些产生这些抗体的IBD患者。
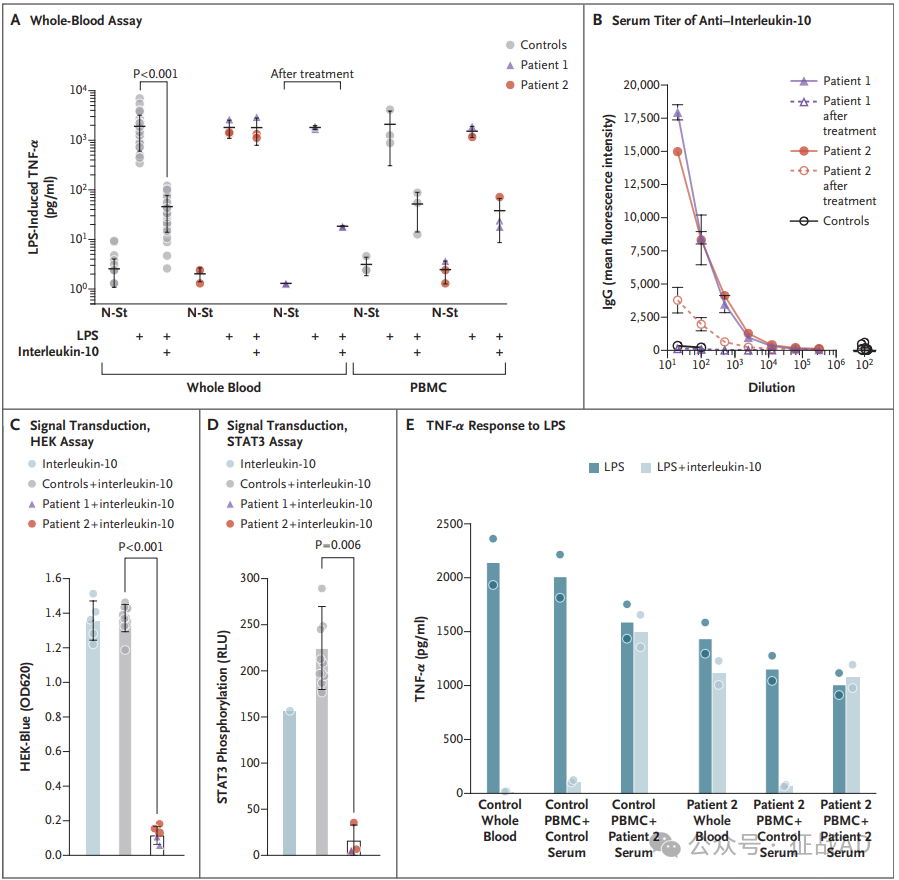
图5. 2名IBD患儿IL-10自身抗体的鉴定和功能表征
🔷 肠道微生物组研究
在一项由哈佛大学的 Christopher Smillie 教授领导的研究中,科学家们分析了 IBD 患者与健康人群的粪便样本,识别出与IBD相关的140,000种细菌菌株。研究中发现数百种与IBD相关的细菌菌株,许多菌株似乎已经适应了在炎症组织中生存。此外,某些菌株的存在可以用来预测疾病的严重程度,例如,Eggerthella lenta 菌株的丰度随着与炎症相关的蛋白质水平的升高而降低【5】。Smillie 希望这些微生物的特征描述能够用于监测疾病进展,并根据患者对潜在疗法的反应可能性将IBD患者进行分组。
这项研究揭示了IBD与肠道微生物组之间的复杂关系,并为未来通过微生物组特征来监测疾病进展和指导治疗提供了新的视角。尽管研究仍处于早期阶段,但这些发现为IBD的个性化治疗和患者管理提供了希望。
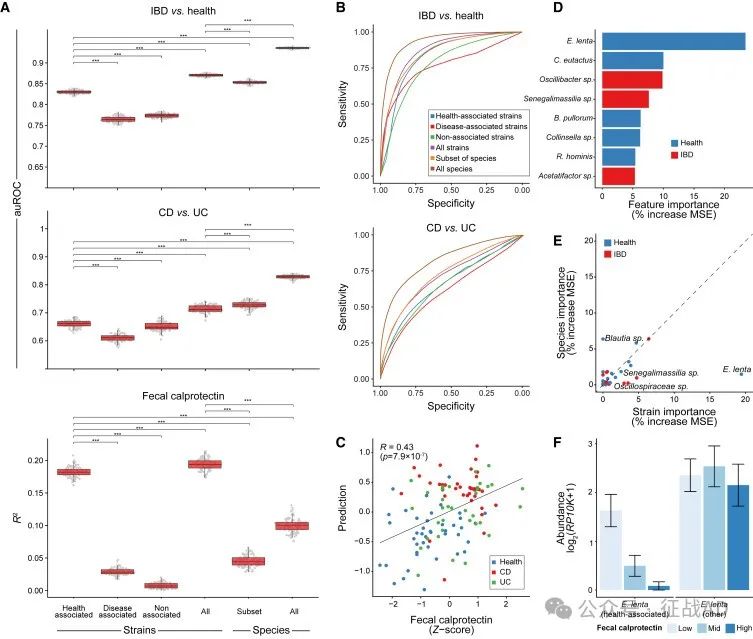
图6. 健康和IBD相关菌株准确预测炎症的生物标志物
编者按:
本研究为IBD的个性化治疗提供了新的视角,尤其是在遗传、免疫和微生物组学方面。
未来,通过进一步的研究,有望开发出针对特定遗传背景和免疫反应的治疗方案,以及利用微生物组特征来监测疾病进展和预测治疗反应。
原文链接:
【1】https://doi.org/10.1016/S2468-1253(19)30333-4
【2】https://doi.org/10.1038/d41586-024-02556-6
【3】https://doi.org/10.1038/s41586-024-07501-1
【4】https://doi.org/10.1056/NEJMoa2312302
【5】https://doi.org/10.1016/j.chom.2024.05.022
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#IBD# #炎症性肠病#
64