西工大李鹏教授/冯涛副教授ACS Nano:响应性纳米涂层包覆益生菌协同药物治疗肠道疾病
2023-07-28 BioMed科技 BioMed科技 发表于上海
研究团队提出了一种简单且安全的益生菌联合药物涂层包覆策略,即通过可对胃肠道微环境响应的海藻酸钙纳米涂层包覆益生菌和负载抗炎药物,达到协同治疗炎症性肠道疾病的目的。
肠道菌群在维持肠道环境稳态和调节人体健康方面起着重要作用,菌群失调与炎症性肠病、肥胖、糖尿病、抑郁症和癌症等多种疾病相关。益生菌能够在肠道中不断产生关键的生物分子来重新编程肠道菌群,是一种有效治疗肠道菌群失调的方法。口服益生菌具有无创性和患者依从性高的优势,但是由于益生菌难以抵抗恶劣的胃肠道环境(如低pH值、消化酶和胆汁酸等),使得其生物利用度和治疗效率有待进一步提高。
此外,在临床治疗肠道疾病时,口服益生菌通常需要与其他治疗药物共同给药,然而不同口服制剂在体内的独立递送可能会降低联合治疗的效率。因此,如何实现口服益生菌和治疗药物的同时有效递送,从而达到协同治疗肠道疾病的效果,亟待深入研究。
基于上述问题,西北工业大学柔性电子研究院李鹏教授/冯涛副教授团队提出了一种简单且安全的益生菌联合药物涂层包覆策略,即通过可对胃肠道微环境响应的海藻酸钙纳米涂层包覆益生菌和负载抗炎药物,达到协同治疗炎症性肠道疾病的目的(图1)。通过考察涂层包覆的益生菌在不同pH培养基、模拟胃液和模拟肠液中的生长增殖和药物释放情况,以及小鼠胃肠道活体荧光成像,证明海藻酸钙涂层可以保护益生菌免受恶劣胃部环境的破坏,在到达肠道后分解并释放益生菌和抗炎药物。
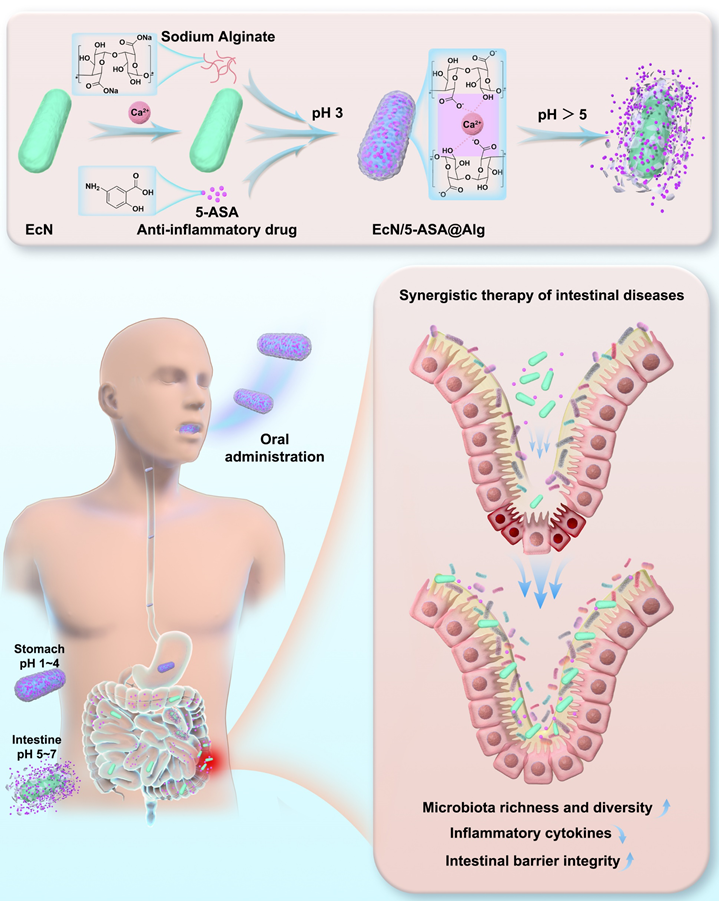
图1. 海藻酸钙纳米涂层包覆益生菌、负载抗炎药物的制备过程,及口服后协同治疗肠道疾病的示意图
在小鼠急性和慢性结肠炎模型中,涂层包覆的益生菌能够在肠道恢复生物活性,并与抗炎药物共同作用,显著改善了小鼠体重下降、疾病活动指数上升以及结肠长度变短等结肠炎症状(图2)。肠道菌群基因测序和免疫组化/荧光染色等结果显示,益生菌和抗炎药物协同上调菌群多样性和益生菌丰度、下调有害菌丰度和促炎细胞因子水平,提高紧密连接蛋白表达量,从而修复肠道屏障治疗结肠炎。本研究证明了海藻酸钙纳米涂层包覆益生菌并负载药物实现协同治疗肠道疾病的可行性,为提高口服益生菌的治疗效果提供了新思路。
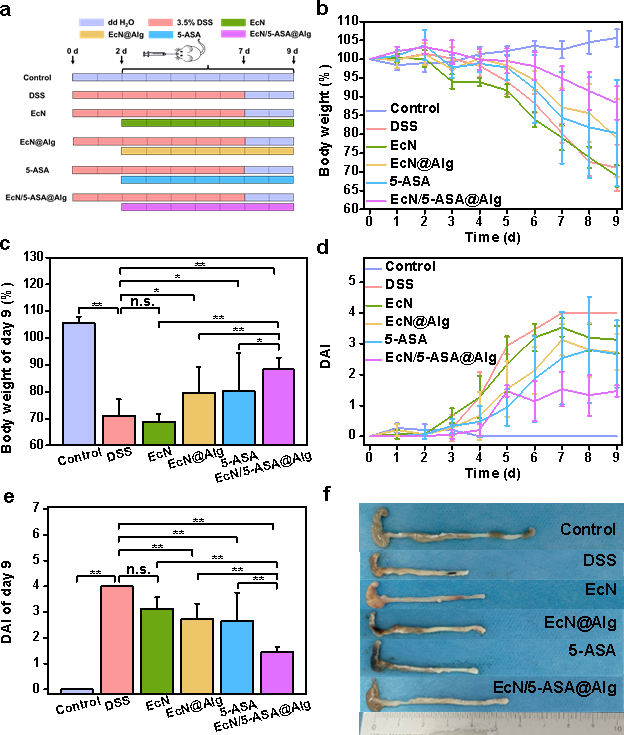
图2. EcN/5-ASA@Alg缓解葡聚糖硫酸钠诱导的小鼠急性结肠炎。(a)实验设计示意图;(b,c)小鼠在治疗期间和第9天的体重;(d,e)小鼠在治疗期间和第9天的疾病活动指数;(f)不同治疗组的结肠组织图像(n=5,**P < 0.01,*P < 0.05,n.s. 无显著性差异)
相关工作以“Gastrointestinal Microenvironment Responsive Nanoencapsulation of Probiotics and Drugs for Synergistic Therapy of Intestinal Diseases”为题发表于ACS Nano。西北工业大学柔性电子研究院李鹏教授、冯涛副教授为本文的共同通讯作者,博士生彭盼娣为第一作者。该工作得到国家自然科学基金、宁波市自然科学基金、重庆市自然科学基金以及陕西省杰出青年科学基金等项目的支持。
参考文献
Pandi Peng, Tao Feng*, Xue Yang, Chaofan Nie, Luofeng Yu, Rui Ding, Qian Zhou, Xueqing Jiang, Peng Li*. Gastrointestinal Microenvironment Responsive Nanoencapsulation of Probiotics and Drugs for Synergistic Therapy of Intestinal Diseases. ACS Nano, 2023, 17, XXX - XXX.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言