甲状腺功能报告单解读及相关指标检测的影响因素(全)
2022-11-11 检验之声 检验之声
随着甲状腺指标异常人群的逐年增多,近些年人们对甲状腺功能的关注越来越多,但甲状腺作为一个复杂的人体器官, 其功能的正常发挥受诸多因素的影响。
随着甲状腺指标异常人群的逐年增多,近些年人们对甲状腺功能的关注越来越多,但甲状腺作为一个复杂的人体器官, 其功能的正常发挥受诸多因素的影响。正常人群中,下丘脑分泌促甲状腺激素释放激素(TRH), 调节垂体分泌促甲状腺激素(TSH),TSH作用于甲状腺促进甲状腺分泌甲状腺激素T3,T4,而在甲状腺激素合成的过程中还需要甲状腺过氧化物酶(TPO)、甲状腺球蛋白(Tg)以及TSH受体(TSHR)等的参与,当甲状腺激素达到一定浓度后,这个信息又会进一步通过反馈调节传递给下丘脑和垂体,从而使整个甲状腺系统维持在一个相对稳定的水平。
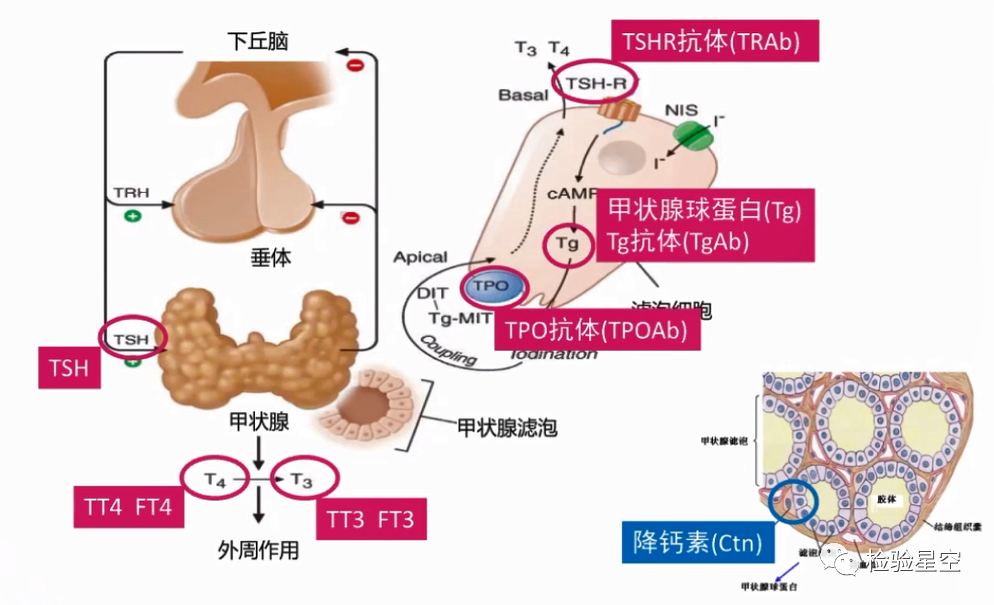
虽然在临床上检测甲状腺功能目前主要看TSH, T3, T4, TPOAb, TgAb, TRAb等相关指标,但实际上甲状腺正常功能的实现更为复杂,TSH与TSHR能否正常结合,甲状腺组织能否正常分泌T3,T4,T3,T4能否正常向细胞内转运并与外周结合蛋白(TBG,ABL等)结合,无活性的T4能否向有活性的T3正常转化, T3能否与靶组织的受体正常结合,下丘脑-垂体-靶腺反馈机制是否正常均能影响甲状腺功能的正常发挥,因此,甲状腺功能远比检测指标数字所反映的问题复杂得多。
在没有检验因素干扰的前提下,正常人体中,游离T4(FT4)与TSH之间存在一定的线性关系,通常FT4的水平越高,TSH的水平就越低,若T4与TSH水平的关系脱离正常对应范围,出现某些高高低低的变化,通常会有一些基本规律可以把患者归因于某种特定的疾病,具体见下图。 甲状腺功能报告单解读思路
甲状腺功能报告单解读思路

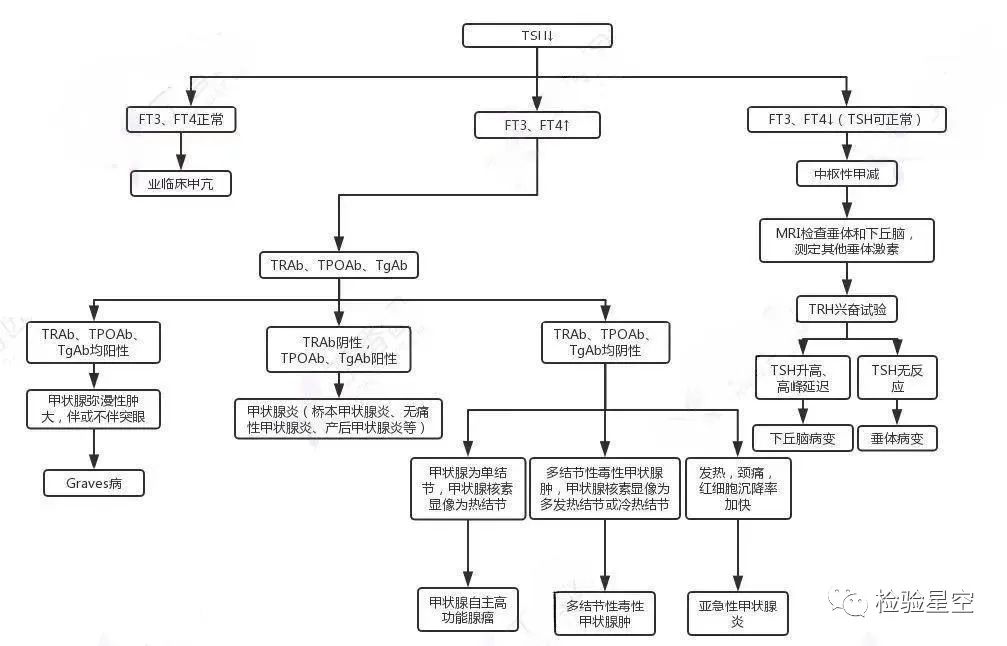 甲状腺分泌指标
甲状腺分泌指标
1.甲状腺素
包括总三碘甲状腺原氨酸(TT3)、总甲状腺激素(TT4) 、游离三碘甲状腺原氨酸(FT3)、游离甲状腺素(FT4)。是甲状腺分泌的重要激素,具有促进营养代谢、体格生长、大脑发育、完善神经和心血管功能等诸多作用。血清甲状腺素指标的高低直接反应甲状腺的功能状态。
临床意义
➤增高:表示甲亢,见于Gravse病、亚甲炎早期甲状腺毒血症、桥本甲亢及功能性甲状腺结节、药物性甲亢(服含碘制剂、避孕药、雌激素及服用甲状腺素药物治疗过量等等)。
➤降低:见于原发性甲减及继发性甲减(甲亢碘131治疗后、甲状腺手术后,垂体性甲减、药物性甲减等)。
其中 FT3、FT4比较稳定,不易受其他因素影响,是目前诊断甲亢、甲减的常用化验指标。FT3在甲亢早期或复发初期最先升高,对甲亢诊断意义大,而FT4甲亢时也增高,但甲减时最先降低,对甲减诊断优于FT3。
TT4测定可用于甲亢、原发性和继发性甲减的诊断以及TSH抑制治疗的监测;血清中TT3的绝大多数(99.5%)与血浆中特异蛋白结合,仅极少数处于游离状态(0.5%)。TT3浓度的改变,表示甲状腺功能的异常,TT3、TT4在甲亢时常同步升高。但也有例外。
特殊情况
➤仅TT3增高:包括TT3型甲亢(在缺碘地区多见)、TT3优势甲亢(即甲亢经药物治疗后,TT4已正常,而TT3持续不降甚或增高,此型复发率高,宜手术治疗)、甲亢早期或甲亢复发初期;
➤仅TT4增高:包括TT4型甲亢(与吃含碘食物过多有关)、少数仅TT4高的老年甲亢;
➤TT4减低:见于甲减。
因此,临床上常同时测定TT3和TT4值。
2.降钙素(CT)
是由甲状腺滤泡旁细胞(又称C细胞)分泌的一种含有32个氨基酸的直线型多肽类激素,降钙素的主要生理功能是调节血液中钙离子的浓度,与甲状旁腺素(PTH)及维生素D等因子一起维持内环境中钙离子的平衡。
降钙素的作用
➤对骨骼的作用:可使破骨细胞活动减弱,成骨细胞活动增强,从而减弱溶骨过程,增强成骨过程,使骨组织释放的钙盐减少,而钙盐沉积增加,因而血钙下降。降钙素还可抑制骨盐的溶解与转移,抑制骨基质分解,提高骨的更新率。
➤对肾脏的作用:降钙素可抑制肾小管对钙、磷、钠的重吸收,从而增加它们在尿中的排泄,降低血液中的浓度,引起低钙血症或低磷血症,但对钾和氯则影响不大。
➤对胃肠道的作用:可抑制肠道转运钙以及胃酸、胃泌素和胰岛素等的分泌。
甲状腺髓样癌(MTC)起源于甲状腺滤泡旁细胞,可大量分泌CT,因此CT是MTC最敏感的血清学标记物之一,测定CT对于MTC的诊断、术前和术后的评估和管理均有重要意义。
临床意义
➤对甲状腺结节病人进行CT筛查可早期诊断MTC,在未经刺激的情况下,血清降钙素>100 pg/ml,则提示可能存在MTC;
➤术前CT水平与肿瘤恶性程度有关,可辅助决定手术范围;
➤术后随访中监测CT可用于预测复发风险,早期发现并处理转移病灶。
TSH和TRH分泌指标
1.TSH
TSH在脑垂体产生,有促进甲状腺滤泡细胞产生TT3、TT4、FT3、FT4的作用。临床上甲状腺素分泌指标和促甲状腺激素分泌指标常常放在一起检查和综合考虑,用来反映甲状腺的分泌情况,指导甲状腺疾病的诊断和治疗。
临床意义
➤TSH高低受甲状腺素负反馈控制。甲状腺素高时,TSH低;甲状腺素低时,TSH高。故甲亢时TT3、TT4、FT3、FT4增高,而TSH是降低的,甲减时相反。
➤临床上如果仅有TSH的增高和降低,TT3、TT4、FT3、FT4均正常,往往诊断为亚临床甲减或甲亢。
➤但当出现血清游离甲状腺激素(FT4、FT3)高于正常范围,但血清TSH不被抑制,则提示有TSH腺瘤存在的可能。
2.TRH
TRH由下丘脑室旁核内的一些神经细胞合成、分泌。经垂体门脉系统输送至腺垂体,具有促使腺垂体分泌促TSH的作用,进而影响甲状腺素的分泌。
临床意义
➤升高:多见于原发性甲状腺功能减退、席汉氏综合征、垂体前叶功能低下、应用去甲肾上腺素、多巴胺、抗甲状腺药物、寒冷反应等;
➤降低:见于甲状腺功能亢进、下丘脑性甲状腺功能减退等。
甲状腺生化免疫指标
1.甲状腺球蛋白(TG)
正常值参考值5~40μg/L。
临床意义
➤甲状腺疾病(如甲状腺功能亢进症、毒性结节性甲状腺肿、亚急性甲状腺炎和慢性淋巴细胞性甲状腺炎)可出现TG升高;
➤TG对甲状腺癌(DTC)预后判断和监测治疗效果有重要意义:临床对DTC患者的随访发现,测定TG含量诊断DTC复发或转移的灵敏度为88%~97%,特异性为100%;甲状腺癌术前TG水平高提示肿瘤能产生TG,术后TG可作为灵敏的随访肿瘤标志物。
2.甲状腺自身抗体
甲状腺自身抗体内分泌科高频检查的3个指标分别是甲状腺过氧化物酶抗体(TPO-Ab)、甲状腺球蛋白抗体(TG-Ab)、促甲状腺素受体抗体(TR-Ab)。
(1)TPO-Ab和TG-Ab
这两个抗体是针对甲状腺细胞内容物的抗体,均属于自身免疫性甲状腺炎的标志性抗体,可能使甲状腺细胞损伤,其水平升高表明甲状腺组织处于免疫性炎症活跃状态。
TPO-Ab与TG-Ab的临床意义基本相同,但 TPO-Ab 无论是敏感性还是特异性都要优于TG-Ab,是诊断甲状腺自身免疫性疾病(尤其是桥本氏甲状腺炎)的首选指标。相比之下,TG-Ab的特异性较差,仅有TG-Ab升高对诊断意义不大。为了提高阳性检出率,临床通常采取两种抗体联合检测。
临床意义
➤病因诊断:TPO-Ab和TG-Ab显著升高是诊断桥本氏甲状腺炎的主要依据。此外,还可用于自身免疫性甲状腺疾病(AITD)与非 AITD 的鉴别诊断,例如,原发性甲减与继发性甲减的鉴别,前者TPO-Ab、TG-Ab均阳性,后者则呈阴性。Graves病甲亢患者也可有TPO-Ab、TG-Ab升高,但程度轻度或者TPO-Ab升高而TG-Ab正常。
➤预后判断:通常认为TP-OAb、TG-Ab升高提示患者将来发生甲状腺功能减退的风险增加。如孕妇 TPO-Ab 、TG-Ab 持续阳性,预示发生“产后甲状腺炎”及“婴幼儿甲减”的风险较高,但不是绝对的。
➤TG-Ab还可作为分化型甲状腺癌(TDC)的监测指标:正常情况下,分化型甲状腺癌患者TG-Ab水平会在根治术后逐渐降低,并在1~4年内转阴,如果TG-Ab水平再次升高,往往提示肿瘤复发。临床上TG-Ab往往综合TSH和TG对甲状腺癌术前术后进行风险和预后评估及治疗反应监测。
(2)TR-Ab
属于针对甲状腺细胞表面 TSH 受体的抗体,包括甲状腺刺激性抗体(TS-Ab)和甲状腺抑制性抗体(TB-Ab)两种亚型。前者与自身免疫性甲状腺机能亢进(即 Graves 病)的发病有关,而后者与自身免疫性甲状腺机能减退(如桥本氏甲状腺炎)的发病有关。
目前多数医院只是检测TR-Ab,不能分别检测两种亚型。临床上测的TR-Ab可以当做是TS-Ab。
临床意义
➤鉴别甲亢病因:Graves 病患者TR-Ab阳性率可达95% 以上,而其他原因引起甲亢(如亚急性甲状腺炎)一般为阴性,因此,TR-Ab常用于Graves病与其他甲状腺疾病的鉴别。
➤指导用药及判断预后:TR-Ab是决定Graves病患者能否停药的重要参考指标。TR-Ab阳性表明机体处于免疫活跃状态,阴性表明机体处于免疫缓解状态。Graves病患者经过治疗甲功恢复正常后,如果 TR-Ab也转为阴性,则停药后复发的可能性小;若药物治疗后TR-Ab仍持续阳性,则停药后复发的可能性较大。
➤有助于预测新生儿甲亢:TR-Ab能够通过胎盘,刺激胎儿甲状腺,引起新生儿一过性甲亢(发生率1~2%)。因此,对患有Graves病的孕妇检测TR-Ab,有助于预测新生儿甲亢,指导新生儿是否有必要采取积极筛查或治疗措施。
➤有助于甲功正常的 Graves 眼病的诊断:临床上有些突眼病人,虽然甲状腺功能正常,但TR-Ab呈强阳性,这种情况同样可以确诊为Graves眼病。
 TSH降低,FT4/FT3升高
TSH降低,FT4/FT3升高
 TSH降低,FT4/FT3正常
TSH降低,FT4/FT3正常
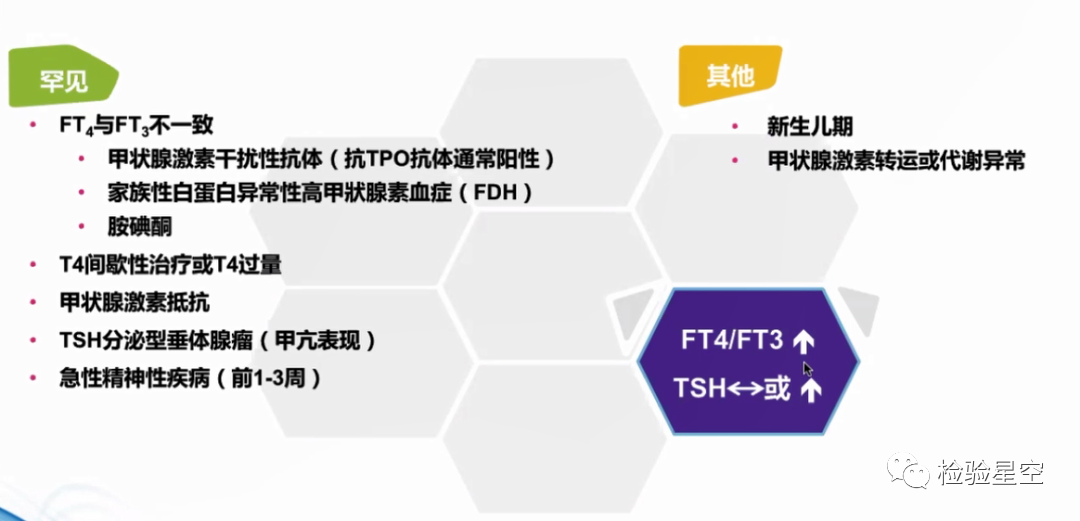
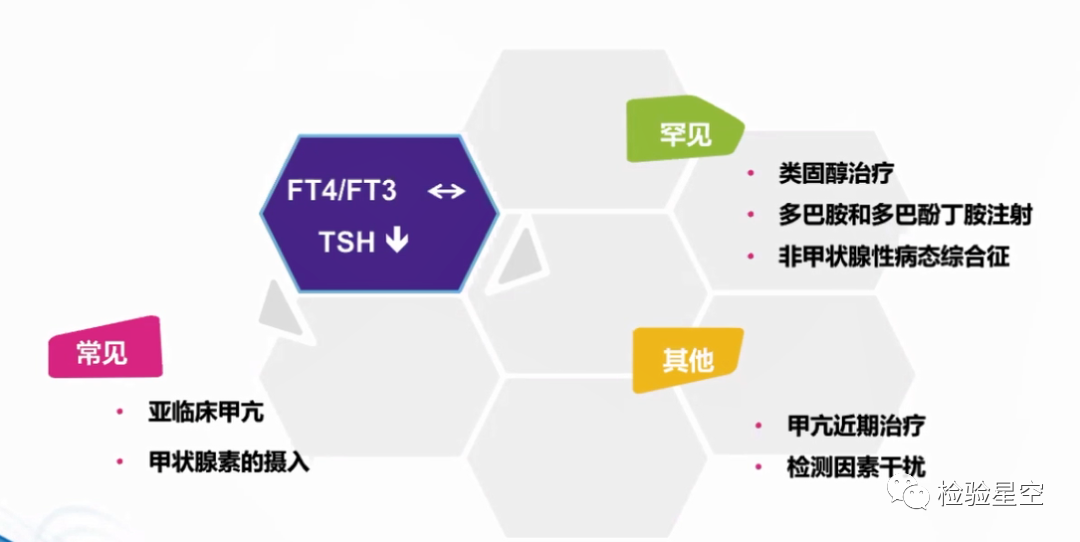 TSH正常或降低,FT4/FT3降低
TSH正常或降低,FT4/FT3降低
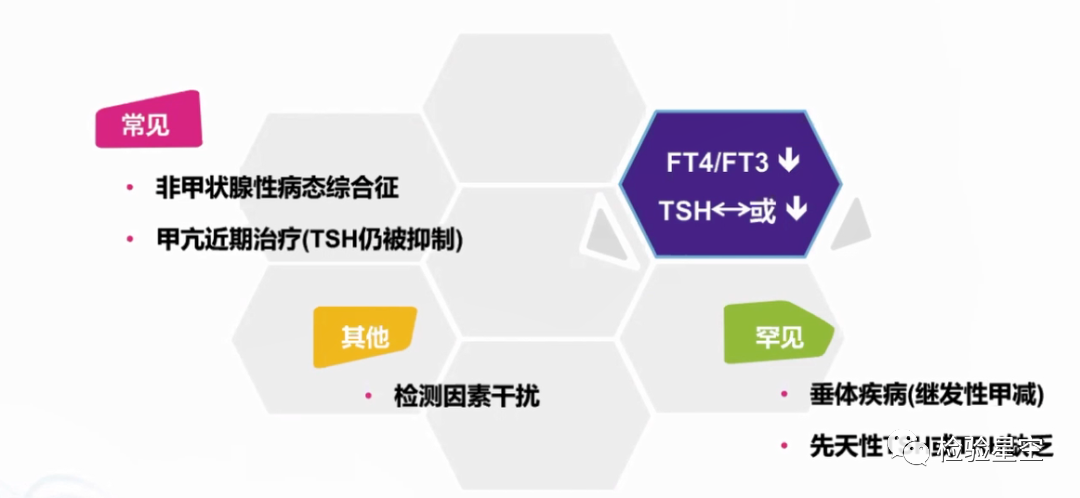 TSH升高,FT4/FT3降低
TSH升高,FT4/FT3降低
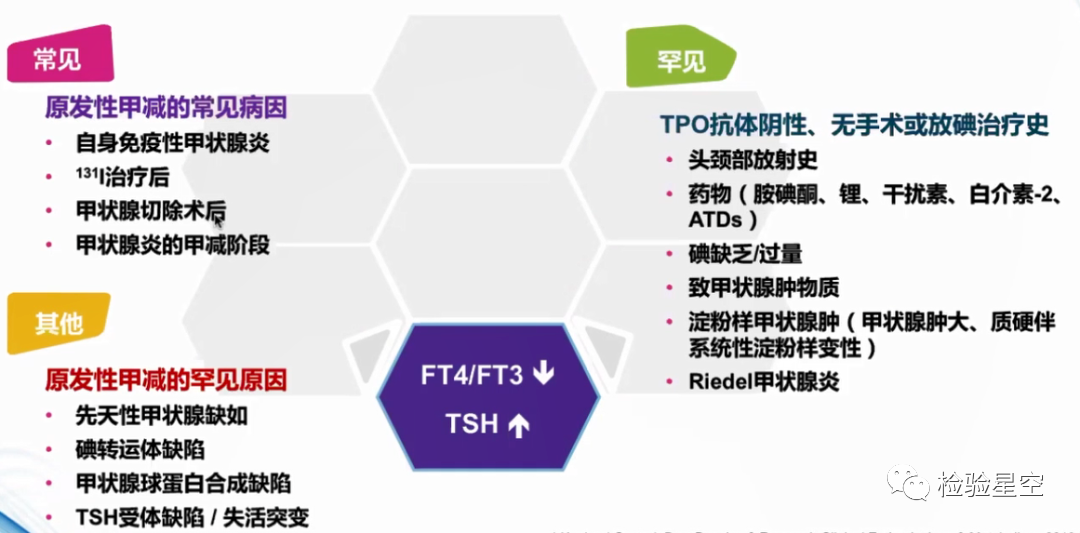 TSH正常或升高,FT4/FT3升高
TSH正常或升高,FT4/FT3升高
 TSH正常,TT4/TT3异常而FT4/FT3正常
TSH正常,TT4/TT3异常而FT4/FT3正常
 但值得注意的是,结合患者的临床表现,不同的甲状腺检测结果的组合模式通常可能对应多种疾病,每一种甲状腺检测结果的组合模式如何解读?这些检测指标的异常可能与哪些疾病相关?
但值得注意的是,结合患者的临床表现,不同的甲状腺检测结果的组合模式通常可能对应多种疾病,每一种甲状腺检测结果的组合模式如何解读?这些检测指标的异常可能与哪些疾病相关?
常见的甲状腺功能检查结果误读
 甲状腺功能报告解读注意事项
甲状腺功能报告解读注意事项
1.每一种甲状腺功能结果可由多种不同的疾病或临床状态所引起,同一疾病在其发生发展不同阶段可以呈现不同的甲功形式,有时候仅通过数字的结果而不结合临床背景可能会做出错误的判断。临床上,早孕反应呕吐严重的孕妇化验甲功时常常会发现FT4轻度升高、TSH轻度降低,临床遇到这种情况,不要轻率地诊断为“Graves病”,还要想到“妊娠期hCG相关性甲亢(又叫‘妊娠甲亢综合征’)”,其发生与hCG产生增多有关。hCG与TSH结构相似,可以促进甲状腺激素的分泌,使FT4轻度升高、TSH轻度下降。
如果孕妇之前无甲亢病史,甲功检查有轻度的FT4升高及TSH降低,TRAb、TPOAb等甲状腺自身抗体阴性,同时hCG水平显著升高,则基本可以确定是“妊娠期hCG相关性甲亢”。与Graves甲亢不同,本病病程呈一过性,不需要抗甲状腺药物治疗。
2.妊娠与非妊娠甲功正常值不同,妊娠期体内发生的一些生理和激素水平变化会影响甲状腺功能,由此导致妊娠期的甲功与非妊娠期有所不同。妊娠期对甲状腺功能影响最重要的两种激素是人绒毛膜促性腺激素(hCG)和雌激素。在妊娠早期,hCG增高可刺激甲状腺分泌,导致促甲状腺激素(TSH)轻微下降(称为“亚临床甲亢”),到妊娠中后期TSH逐渐恢复正常。
雌激素可使血清中甲状腺激素结合蛋白(TBG)的含量增加,因血液中99%的甲状腺激素(TH)都是和甲状腺结合蛋白结合在一起的,实验室测定的总甲状腺激素(TT3、TT4)水平可能会轻微升高,而游离甲状腺激素(FT3、FT4)通常保持正常。因此,在妊娠早期化验甲功发现TSH轻微下降,TT3、TT4轻度升高,孕妈不用担心,因为这不是甲亢,而属于孕期正常的生理变化。
2011年美国甲状腺协会(ATA)指南首次提出妊娠期特异的TSH参考值:孕早期(T1期)0.1~2.5mlU/L;孕中期(T2期)0.2~3.0mlU/L;孕晚期(T3期)0.3~3.0mlU/L。
我国滕伟平教授的研究显示,中国人群血清TSH水平普遍升高,ATA提出的妊娠期TSH正常范围并不适合中国孕妇,建议采用本地区的妊娠特异性TSH参考值;无条件获得妊娠特异性参考值的医院,可以采用我国《妊娠和产后甲状腺疾病诊治指南》提出的参考值。
3.甲状腺自身抗体特异性不强,甲状腺自身抗体(如TPOAb、TGAb等)主要见于各种自身免疫性甲状腺疾病(AITD),而Graves甲亢、桥本氏甲状腺炎等均属于AITD范畴,因此这些患者均可检出甲状腺自身抗体,两者区别在于:桥本氏甲状腺炎患者的抗体滴度较高,而Graves甲亢患者尽管也能查出TPOAb、TGAb,但抗体滴度相对较低。
由于甲状腺自身抗体的诊断特异性不强,且上述两种疾病的抗体滴度也没有一个截然的界限,因此,在临床诊断时,往往还要结合甲功、TRAb或甲状腺细针穿刺细胞学检查进行综合判断。
4.HT与TSH变化不总是同步,TSH是反映甲状腺功能活动的敏感指标,当发生亚临床甲状腺疾病时,TSH往往先于TH发生变化,因此,测定TSH对诊断“亚临床甲亢”或“亚临床甲减”具有重要价值。
TH与TSH之间通过反馈调节最终实现下丘脑-垂体-甲状腺轴的动态平衡,但这需要一个长达数周的时间过程,在此期间, TSH和T3、T4之间的变化并不完全同步。
一般来说,甲减用TH制剂替代治疗后,需要4~6周才能使血TSH恢复正常;而甲亢用抗甲状腺药物(ATD)治疗后,需要2~6个月才能使血TSH恢复到正常范围。在此之前,血T3、T4与TSH的浓度会出现矛盾现象,T3、T4已正常,而TSH仍升高(甲减)或降低(甲亢),这段时间为TSH与TH之间的“非平衡期”。
这种看上去似乎矛盾的结果,并非实验室检查结果不准确,而是因为两者之间达成平衡存在一个时间差的缘故,这对评价“非平衡期”的用药效果及指导临床用药具有重要意义。
在甲亢没干预时,表现为FT3、FT4升高,TSH降低,经一段时间治疗后,FT3、FT4已经呈下降趋势,但是TSH仍低,这个阶段调整药物,不能只看TSH,需要根据FT3、FT4及临床经验等综合判断。
5.TH降低,未必就是“甲减”,一般说来,甲减时,往往都有甲状腺激素(如FT3、 FT4)水平减低,但反过来,甲状腺激素水平降低,一定就是甲减吗?答案是:未必。
这是因为,老年人、严重营养不良及晚期恶液质的患者在化验甲功时,也常常会有T3(或T3、T4)轻度下降,而TSH正常或轻度降低,但反T3(rT3)升高。这种情况是机体为降低代谢消耗的一种保护性反应,临床称之为“低T3综合征”,也称 “正常甲状腺性病态综合征”(ESS),并不是真正的甲减。
6.“甲功五项”可协助定位诊断,“下丘脑-垂体-甲状腺”是人体最重要的三大内分泌轴之一。甲状腺分泌TH受下丘脑分泌的促甲状腺激素释放激素(TRH)和垂体分泌的TSH控制;同时,TH分泌增加又可反馈性抑制垂体TSH的合成和分泌。
通常情况下,TH对TSH的反馈抑制作用占优势。一般说来,若TH与TSH变化方向相反,即可推知原发病变部位在甲状腺(如Graves病、高功能甲状腺腺瘤);而当TH与TSH的变化方向一致,则原发病变部位有可能(不是全部)在垂体或下丘脑。
7.TSH、TH升高≠垂体性甲亢,“垂体性甲亢”是由于TSH分泌过多引起的甲亢,患者的TSH与TH往往同步升高;但反过来,TSH与TH同时升高,却未必一定就是“垂体性甲亢”,也可能是 “甲状腺激素抵抗综合征(resistance to thyroid hormone,RTH)”。
RTH患者往往有家族史,“垂体TSH瘤”通常无家族史,但少部分多发内分泌腺瘤(MEN-1型)中的TSH瘤存在家族性发病;
RTH患者影像学检查垂体无异常发现,“垂体TSH瘤”常常发现腺瘤;
RTH患者血清糖蛋白激素α亚单位(α-GSU)水平降低,垂体TSH瘤α-GSU和/或α-GSU/TSH比值显著增高;
RTH患者血清TSH对TRH(促甲状腺激素释放激素)反应正常或者增强,绝大多数垂体TSH瘤患者TSH对TRH无反应;
基因检测发现编码甲状腺激素受体β(TRβ)的基因发生突变对诊断RTH最具价值。
8.TSH在评估甲功方面存在局限性,TSH是反映甲状腺功能最敏感的指标,特别是在诊断亚临床甲亢或甲减时具有重要作用。此外,也常常用于中枢性(包括垂体性和下丘脑性)甲减的诊断:原发性甲减时,血清TSH应大于10mIU/L,若此时TSH正常或只是轻度升高,则疑似“中枢性甲减”。
但TSH在反映甲状现功能方面也存在一定的局限性,对继发于垂体或下丘脑的甲功异常(即中枢性甲亢或甲减)及甲状腺激素不敏感综合征(RTH),不宜将血清TSH作为评价甲状腺功能的指标。
9.新生儿TSH轻度升高≠先天性甲减,正常足月新生儿出生后30分钟TSH迅速上升至60~80mIU/L,24小时后下降至20mIU/L,出生后1周左右缓慢下降至6~10mIU/L。新生儿先天性甲减筛查大多在出生后2~7天进行,足跟血TSH只要不超过10mIU/L就可以认为是正常的,不能机械套用成年人甲减(TSH>5mIU/L)的诊断标准。
二、甲状腺功能相关实验室指标的影响因素
甲状腺检测结果的不同组合对于患者疾病状态的诊断非常重要,除了患者本身的疾病状态会对甲状腺检测指标产生直接的影响外,检测过程中出现的检测干扰以及患者本身的疾病史,饮食水平,服药状况等都有可能对检测指标造成干扰,因此,在临床对检测结果存在怀疑时,能够识别和确认这些干扰因素以辅助临床医生对患者的疾病状态做出准确的判断就显得尤为重要。
 常见的干扰甲状腺试验室检测指标的因素有哪些?这些干扰因素可能会引发甲状腺相关实验室指标发生何种变化?通过哪些方法能够进一步排除或确认这些影响因素的存在?
常见的干扰甲状腺试验室检测指标的因素有哪些?这些干扰因素可能会引发甲状腺相关实验室指标发生何种变化?通过哪些方法能够进一步排除或确认这些影响因素的存在?
一、常见的生理因素干扰
生物学变异
FT4的个体内变异相对较小,大约在5%~7%,而TSH在个体内变异比较大,可以达到29%,其生物学意义在于保持FT4水平的稳定。
昼夜节律
有研究显示:受试者间隔10分钟采样一次,绘制24小时TSH的分泌曲线,在统一控制进食和睡眠时间的情况下,所有受试者TSH都有显著的昼夜节律:在夜间处于高浓度水平,而在白天处于低浓度水平,且夜间男性TSH水平高于女性。因此建议对甲功测定的采血时间加以限制,不能太过宽泛,尤其是对甲癌术后患者、孕妇、亚临床甲减等患者,应尽量在清晨空腹采血。但进食和采血时间对FT4水平几乎是没有影响的。
季节
有日本学者的研究显示:夏季TSH水平偏低,冬季TSH水平偏高,但不同的文献报道存在不一致。
妊娠
妊娠导致的绒毛膜促性腺激素(HCG)具有刺激甲状腺的作用,从而抑制TSH分泌,使血清TSH水平降低20%~30%,HCG一般在妊娠8-10周达到高峰,通常HCG每增高10000 IU/L,TSH降低0.1 mIU/L,因此妊娠妇女较非妊娠妇女TSH平均降低0.4 mIU/L,TSH水平降低发生在妊娠8-14周,妊娠10-12周是下降的最低点,且有20%的孕妇可降至0.1 mIU/L以下。
治疗监测
一项横断面研究显示,左旋甲状腺素(L-T4)治疗不足和过量的发生率高达30%~50%,这与L-T4制剂的质量,患者的依从性,服药时间,胃肠吸收,患者个人体质等都有很大的关系。通常来讲,虽然TSH是衡量甲状腺功能相对敏感的指标,但也需要在服药数天或数周后才能达到相对稳定的水平,因此此时FT4的水平可能更加可靠;此外,一般空腹口服L-T4,前90分钟T4浓度上升最快,并在2小时达到峰值,因此常规监测应最好在服药之前进行样本采集和指标检测。
药物
多种药物包括多用于心内科和影像科的含碘药物与制剂,一些抗肿瘤药物如酪氨酸激酶抑制剂索拉菲尼,伊马替尼等,以及干扰素α等药物的免疫治疗均可能造成甲状腺功能的改变,因此对患者的疾病状态做出诊断时,还应充分考虑这些因素的影响。二、常见的测定因素干扰
巨TSH
巨TSH是TSH自身抗体与TSH形成的抗原抗体复合物,其分子量较大,在体内清除减慢,其免疫学活性与单体TSH相似,但生物学活性较低,在测定过程中可以与试剂中的抗体结合,造成测定结果增高,巨TSH在人群中的发生率为0.6%~1.6%。巨TSH仅对TSH的测定造成干扰,因此可能造成T3/T4正常,但TSH轻度或显著升高,对此类人群的鉴别可使用PET沉淀和凝胶色谱方法。
甲状腺自身抗体(THAAbs)
THAAbs是人体自身产生的T3/T4抗体,可在体内存在数月至数年,在普通人群中THAAbs阳性率约为1.8%,自身免疫性疾病患者中THAAbs阳性率可达40%,THAAbs阳性的个体中,TgAb/TPOAb的阳性率高达80%~100%,机体中存在的THAAbs可与试剂中的甲状腺激素类似物结合,造成FT3/FT4结果假性升高,当怀疑THAAbs干扰时,需要进一步识别和确认干扰,稀释和PEG沉淀的方法建议在检测TT3/TT4时使用,需要同时检测FT3/FT4/TT3/TT4时,建议更换检测方法进行复测或者使用金标准平衡透析-质谱的方法。
异嗜性抗体(HA)
HA是指已知或未知抗原刺激人体产生的能和多个物种的免疫球蛋白结合的免疫球蛋白,HA在体内的存在可持续4-12个月,并且可以通过胎盘影响新生儿甲状腺激素的测定。采用双抗体夹心法检测时,HA存在导致的TSH受干扰概率更大,T3/T4受干扰概率较小,其干扰TSH测定的发生率约为0.4%,干扰后主要导致检测指标假性升高,可考虑更换检测方法,进行稀释验证,或使用异嗜性抗体阻断剂(HBT)来排除HA的存在。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言