Science:MSKCC再发文!迄今很大临床研究发现,一些癌症患者天生就携带响应免疫治疗的基因
2017-12-08 BioTalker 奇点网
昨天(12月7日),纪念斯隆-凯特林癌症中心(MSKCC)的临床医学科学家Timothy A. Chan团队又在顶级期刊《科学》撰文称(1),他们发现癌症患者从免疫检查点抑制剂治疗中的获益程度,与他们从父母那里遗传获得的先天性基因特征有关。更重要的是,他们找到了那些影响患者对免疫检查点抑制剂治疗响应程度的相关基因。
昨天(12月7日),纪念斯隆-凯特林癌症中心(MSKCC)的临床医学科学家Timothy A. Chan团队又在顶级期刊《科学》撰文称,他们发现癌症患者从免疫检查点抑制剂治疗中的获益程度,与他们从父母那里遗传获得的先天性基因特征有关。更重要的是,他们找到了那些影响患者对免疫检查点抑制剂治疗响应程度的相关基因。
这一发现意义重大,不仅可以帮助医生判断哪些患者更适合免疫治疗,同时也有助于那些很难从免疫检查点抑制剂治疗中获益的患者及时找到更合适的治疗方案。
临床医学科学家Timothy A. Chan
MSKCC不愧是世界顶级的癌症研究中心。
2011年第一个免疫检查点抑制剂Yervoy(ipilimumab)获FDA批准,MSKCC的Jedd D. Wolchok博士等人居功至伟。
然而,广大的医务人员很快又面临另一个问题,究竟哪些患者可以从免疫检查点抑制剂治疗中获益?无人能解。
没成想三年之后的2014年,Timothy A. Chan团队就在《新英格兰医学期刊》发表重要研究论文,他们发现黑色素瘤患者携带的基因突变量与免疫治疗响应有关。次年,他们在非小细胞肺癌中也发现了这种现象。随后大量的研究证实了他们的发现。有研究认为,这可能是癌细胞携带的基因突变,导致癌细胞表面出现了新抗原,增加了杀伤性T细胞识别癌细胞的可能性。
Jedd Wolchok, Alexandra Snyder Charen和Timothy Chan
用一句话慨括Chan博士的这两个发现就是,「患者肿瘤基因突变越多,响应免疫治疗的可能性就越大。」这一度甚至成为基因检测领域创业的热门话题。
不过这显然不是全部,早就有研究表明,仅有一小部分肿瘤里的基因突变有免疫原性,能刺激机体的免疫活性细胞产生免疫应答。
近几年研究人员还发现,肿瘤免疫表型和肠道微生物也会影响患者对免疫检查点抑制剂治疗的响应程度。
但,患者从父母那里遗传获得的先天性基因特征如何影响免疫检查点抑制剂治疗反应,尚不清楚。尤其是人类白细胞抗原(human leukocyte antigen, HLA)。对,我们熟知的「移植配型」,要配的就是它。如果对不上,患者对移植物产生排异反应的风险就大大增加。
HLA基因位于人体第6号染色体上,是一大群基因的统称。HLA对人类来说至关重要,它分布在人体细胞表面,负责将各种抗原呈递给T细胞,以帮助T细胞判断是否要攻击目标物体。简单来说,HLA决定了T细胞能看到什么。
为了适应环境中各种各样的病原物,HLA基因在进化过程中已经变成人体内多样性程度最高的基因,用以帮助人体免疫系统识别更多的病原物等异己,维持自身的稳定性。早就有研究表明,人体HLA的情况与艾滋病、乙肝和疟疾患者的预后有关。
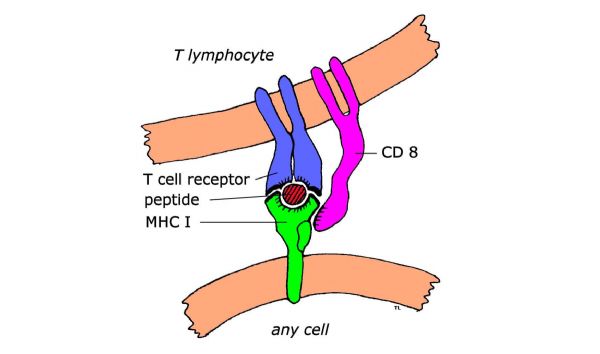
作为人体内异常细胞,癌细胞被杀伤性T细胞(CD8+)识别是通过HLA I实现的(16-18)。可以说,HLA在杀伤性T细胞识别癌细胞中起到了至关重要的作用,然而,HLA与免疫治疗响应程度之间的关系还不明确。
杀伤性T细胞识别HLA(MHC1)呈递的抗原
Chan团队决定一探究竟。
他们先找到了两个接受免疫检查点抑制剂治疗的患者队列,分别命名为队列1和队列2。队列1有369名患者,其中269名为晚期黑色素瘤,100名为晚期非小细胞肺癌,他们分别接受了CTLA-4抗体和PD-1抗体治疗,还做了外显子测序,临床数据保存完好。队列2有1166名患者,涉及包括黑色素瘤和非小细胞肺癌在内的多个癌种,所有患者都做了MSKCC已获FDA批准的MSK-IMPACT测序,治疗方式有CTLA-4坑体、PD-1抗体和PD-L1抗体。
研究人员首先分析了这些患者的HLA I基因分型信息,然后将其余患者治疗后的临床信息结合。
一分析,Chan发现,在肿瘤内基因突变携带量没有差异的人群中,HLA I更多样的患者,从免疫检查点抑制剂治疗中获益更多,这两个队列中均是如此。把肿瘤的分期和药物类型等因素也考虑进来时,上述的相关性仍显着存在。
当他们把HLA I的多样性与肿瘤基因突变的负担量结合起来考虑的时候,发现HLA I更多样、基因突变多与患者从免疫检查点抑制剂治疗中获益关系更强。与单独分析基因突变携带量相比,基因突变多、HLA I更多样的患者,从治疗中获益更大。
队列1和队列2数据分析:
A和B为HLA多样性高和多样性低患者的总体存活率
D和E为多样性高且突变多与多样性低且突变少患者的总体存活率
这就有意思了,在免疫检查点抑制剂治疗领域一直没人关注的HLA确实与免疫治疗的效果有相关性。接下来Chan团队想要探究单个HLA I等位基因与免疫检查点抑制剂治疗的临床相关性。
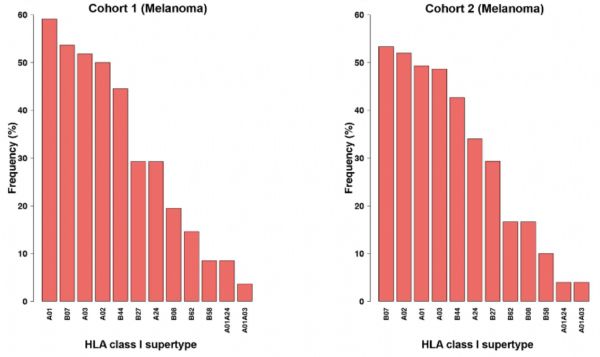
由于HLA I等位基因众多,研究人员已经根据它们各自的特点,将他们分成12个超型,其中A超型6个,B超型6个。基本上是涵盖了在不同人群中发现的大多数HLA I的等位基因。
12种超型,以及它们在两个队列中所占的比例,其中B44超型占45%左右,B62超型占15%左右
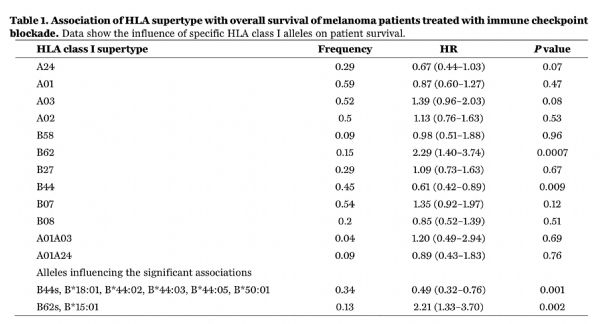
在分析各种超型对黑色素瘤患者生存率的影响时,研究人员发现,如果患者有B44超型里的等位基因,那么患者的生存率会显着提高,这种提高是与另外6个等位基因的存在有关;如果患者有B62超型里面的HLA I等位基因,那么患者的生存率会显着降低,而这种降低也与另外一个等位基因的存在有关。
总的来看,Chan团队的研究HLA I基因的多样性影响了免疫检查点抑制剂治疗的效果。B44超型可以提高患者的存活率,而B62超型会降低患者的存活率。Chan建议,在以后的临床试验中,可以考虑使用这些位点评估患者是否可以从治疗中获益。另外,对于B44超型,既然可以提高患者的存活率,那么久可以据此设计新的治疗方法。
12个超型在接受免疫检查点抑制剂治疗的黑色素瘤患者中的比例,以及没有这12种超型和有12种超型的风险比
MSKCC的MSK-IMPACT测序就包含血液样本中的HLA基因型分析,且已获FDA批准。他们即将展开下一步的研究。
原始出处:
1、Diego Chowell et al., Patient HLA class I genotype influences cancer response to checkpoint blockade immunotherapy. Science. 07 Dec 2017.
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#研究发现#
72
#癌症患者#
74
#SCIE#
73
基因在很大程度决定了肿瘤特性
96
学习了.涨知识
95
基因的奥秘不断展开
103
谢谢分享.学习了
85
学习了.谢谢分享
95
学习了很有用不错
58
昨天(12月7日).纪念斯隆-凯特林癌症中心(MSKCC)的临床医学科学家TimothyA.Chan团队又在顶级期刊<科学>撰文称.他们发现癌症患者从免疫检查点抑制剂治疗中的获益程度.与他们从父母那里遗传获得的先天性基因特征有关.更重要的是.他们找到了那些影响患者对免疫检查点抑制剂治疗响应程度的相关基因.
61