垂体功能性促性腺激素腺瘤临床病例分析
2020-03-24 王含必 姚勇 邓成艳 生殖医学杂志
垂体功能性促性腺激素腺瘤是一种罕见的良性垂体肿瘤,它分泌一种或两种具有生物学活性的促性腺激素:FSH和/或LH[1],至今全球仅报道34例功能性促性腺激素腺瘤[2]。
垂体功能性促性腺激素腺瘤是一种罕见的良性垂体肿瘤,它分泌一种或两种具有生物学活性的促性腺激素:FSH和/或LH[1],至今全球仅报道34例功能性促性腺激素腺瘤[2]。通常垂体的功能性腺瘤常伴随特异性的临床表现,易于临床鉴别诊断,而垂体功能性促性腺激素腺瘤与其他腺瘤不同,缺乏特异性临床症状及体征,常与其他疾病相混淆,导致误诊及漏诊。垂体功能性促性腺激素腺瘤有多种不同的临床表现,在女性患者中主要表现为月经不规律、异常子宫出血、不孕不育、卵巢过度刺激综合征(OHSS)[3-4];在男性患者中主要表现为睾丸肥大和性功能障碍[5-6]。由于这些症状与其他妇科疾病的表现相同,所以垂体功能性促性腺激素腺瘤经常被误诊及漏诊,直到发展到大腺瘤,引起头痛、视野缺损及垂体功能低下,伴随着性腺机能减退时才被发现并诊断[7]。本文收集迄今为止在北京协和医院收治的5例垂体功能性促性腺激素腺瘤女性患者,总结分析其临床表现、发病特征及治疗,以期提高临床医生对该病的认知,降低误诊及漏诊率。
资料与方法
一、研究对象
回顾性分析了我院收治的5例垂体功能性促性腺激素腺瘤女性患者的临床资料,垂体瘤切除术后经病理切片和免疫组化获得确切诊断。分析内容主要包括临床症状及体征、实验室检测及影像学检查、诊治经过(药物治疗及手术治疗)、病理诊断及免疫组化检测。二、病理检测
每位患者在手术前都接受了全面的激素及影像学评估,手术切除的组织标本都进行了病理学诊断,均由两名病理学医生实施;同时进行免疫组化检测,检测内容主要包括促肾上腺皮质激素(Adrenocor-ticotropic Hormone,ACTH)、生长激素(growthhormone,GH)、兔抗人增殖细胞核核抗原单克隆抗体Ki-67(index 2%)、FSH、LH、P53、PRL、促甲状腺激素(TSH)。术后随诊血清性激素水平、盆腔超声和垂体MRI。
结 果
一般资料
患者年龄34~47岁,平均年龄38.8岁。5例患者均已婚,各育有1孩。2例患者有2次妊娠史,3例患者仅有1次妊娠史。5例患者均有月经紊乱症状。以月经紊乱为首发症状的患者3例,其中1例患者在月经紊乱的同时出现溢乳;还有1例患者产后1年仍有触发溢乳,但未就医,2年后出现月经紊乱,仍是因月经紊乱为主诉就诊。这些患者既往月经规律,后无明显诱因出现月经紊乱,主要表现为月经期延长,出血时间最短15d,最长淋漓不净达30余日;同时出现月经周期紊乱,表现为周期不规律,周期最短仅15d,最长可达60d。二、诊疗过程5例患者各有不同的临床表现,初诊均未能诊断出垂体促性腺激素腺瘤,各自经历不同的诊治过程。下文总结这些患者所经历的诊疗过程。
1.药物治疗:5例患者中2例曾按月经紊乱进行药物治疗,其中1例患者地屈孕酮治疗后仍无法控制异常出血,1例患者口服避孕药治疗后可达到控制月经的效果,但停药后再次发生月经紊乱。因有溢乳症状,发现PRL升高的2例患者使用溴隐亭治疗,最大剂量5mg bid时,溢乳症状消失,但月经紊乱的症状无改善。
2.腹腔镜卵巢囊肿剔除术:4例以月经紊乱为主诉的患者就诊时超声检查均发现双侧卵巢增大,内见无回声多房囊肿,其中1例尝试地屈孕酮治疗无效后,发现囊肿长大,行双卵巢多房囊肿剔除术;其余3例均未接受任何药物治疗,以双侧卵巢多房囊肿而进行了腹腔镜双侧卵巢囊肿剔除手术,手术后病理检查均为单纯囊肿。1例因同时出现腹痛症状,怀疑为“卵巢囊肿蒂扭转”而在当地医院进行了急诊双卵巢囊肿剔除术。这些患者经卵巢囊肿剔除术后均未能恢复正常月经。2例于术后一个月再次出现双侧卵巢囊肿,使用复方口服避孕药妈富隆治疗无效。另2例患者未定期随访,分别于术后4年和6年再次发现双卵巢多房囊肿,其中1例甚至二次实施了腹腔镜囊肿剔除术,术后病理仍为卵巢单纯囊肿。5例患者中有1例未行卵巢囊肿剔除术者,因发病时月经紊乱及溢乳同时出现,初诊时行垂体MRI检查,发现垂体腺瘤,但因是微腺瘤,故未考虑外科手术切除,而是服用复方口服避孕药调整月经,同时溴隐亭治疗高PRL血症,两种药物共同治疗一段时间后,妈富隆治疗未能有效控制异常子宫出血,于当地医院分段诊刮后诊断为子宫内膜单纯增生。患者转诊于我院,根据病史判断为垂体功能性促性腺激素腺瘤,经垂体瘤切除术后卵巢囊肿自行消失,使患者免于不必要的卵巢囊肿剔除术。
3.溢乳及垂体腺瘤:垂体腺瘤的发现都是以溢乳或PRL升高作为线索,经垂体MRI检查确诊。5例患者中,1例开始有触发溢乳,但未予重视,后发展到出现头痛、双眼视物模糊、左眼颞侧视野缺损等症状,经垂体MRI检查证实垂体大腺瘤;1例因首发症状即有溢乳,且伴有PRL升高,经垂体MRI检查证实有垂体腺瘤;1例在腹腔镜卵巢囊肿剔除术后2年出现溢乳,经垂体MRI检查发现腺瘤;另外2例均无溢乳症状,但因月经紊乱进行女性性激素检查时发现PRL升高,进一步垂体MRI检查时发现垂体腺瘤。
4.垂体瘤手术治疗:1例因出现头痛,视神经压迫症状,双眼视物模糊和左眼颞侧视野缺损,伴小便次数增多,经垂体MRI检查发现垂体大腺瘤,而在当地医院接受“经鼻蝶入路垂体腺瘤近全切除术”。术后病理示垂体腺瘤,免疫组化检查FSH、LH、PRL、ACTH、TSH、GH均阴性。术后垂体瘤引发的症状缓解,而月经紊乱未得到改善。首次垂体术后4年再次发现垂体大腺瘤。于我院行二次垂体腺瘤切除术,手术后病理诊断为FSH瘤。其余4例患者均在发现大腺瘤时进行了神经内镜下经鼻蝶入路垂体腺瘤切除+鞍底重建术。
5.分段诊刮术:2例患者曾因月经紊乱而在当地医院就诊,行分段诊刮术,术后病理1例提示单纯增生,1例未发现异常。
三、辅助检查
1.性激素检查:5例患者垂体腺瘤手术前性激素水平见表1。2例患者手术后连续抽血随诊观察性激素变化情况,分别于术后3d及术后4d雌激素水平降至早卵泡期水平,FSH、LH水平下降至<1U/L,但很快恢复至正常水平。
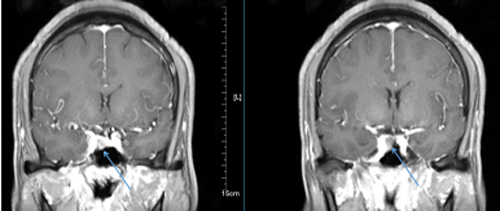
2.影像学检查:(1)卵巢囊肿:5例患者的盆腔超声均提示双侧卵巢体积增大至10~15cm,双侧卵巢布满大小相似的囊性暗区,最大直径2~3cm;(2)垂体占位:5例患者垂体瘤手术前MRI检查提示垂体占位性病变的平均直径9.1~28.3mm,平均值17.7mm。垂体MRI检查见图1。
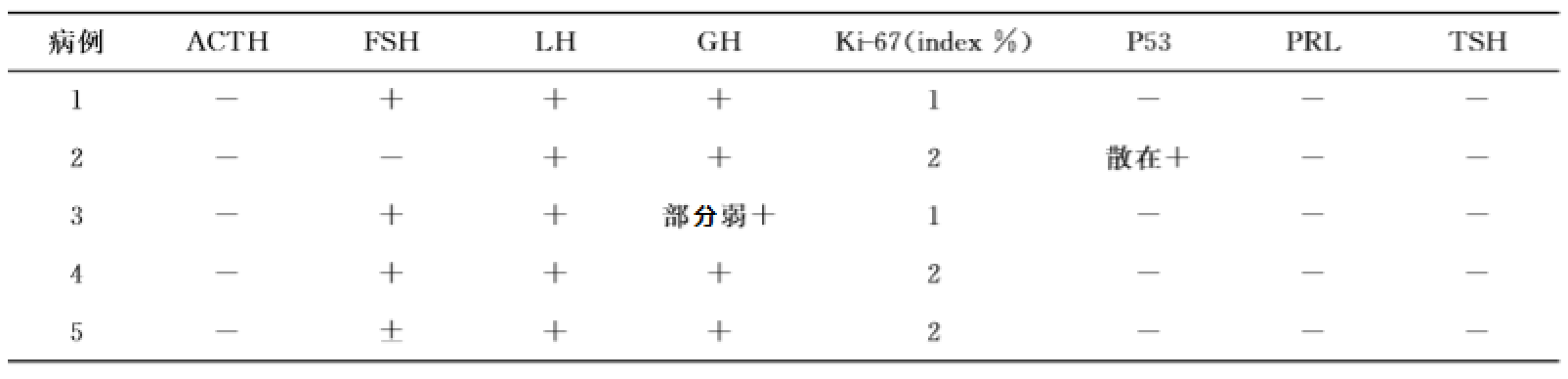
3.术后病理诊断:5例患者术后病理诊断为垂体腺瘤,免疫组化检查见表2。
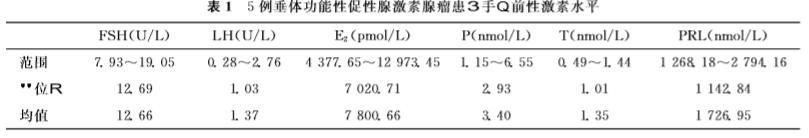
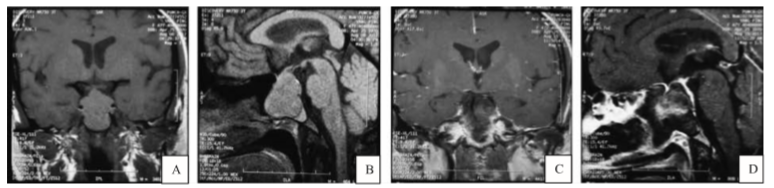
A、B: 垂体冠状面及矢状面, 箭头示手术前垂体大腺瘤; C、D:垂体冠状面及矢状面, 箭头示手术后第2天垂体腺瘤切除术后 图1垂体大腺瘤手术前后冠状面及矢状面 MRI
表2 垂体腺瘤术后肿瘤组织的免疫组化检查
四、术后随诊情况
5例患者术后至今随访3~5年,除1例患者手术后回当地随诊外(电话随访),其余4例均定期返回我院随诊,随诊内容包括患者的症状、体征、垂体分泌的激素及性激素水平检测、子宫双附件超声、垂体MRI。术后患者均很快恢复了自然规律月经,性激素水平恢复到正常范围。垂体瘤手术前有双侧卵巢多发囊肿但未经卵巢囊肿剔除术的患者,在垂体瘤手术后卵巢多发囊肿均消失,双侧卵巢恢复至正常状态。随访至今,未发现垂体促性腺激素腺瘤复发的病例。
讨 论
垂体促性腺激素腺瘤的发病率从影像学及活检估测约1%~30%,总体估测数据为16.7%[8]。垂体腺瘤根据是否分泌激素而分为功能性及无功能性。临床中近64%的无功能腺瘤在免疫组化检查时发现促性腺激素阳性[9]。功能性垂体促性腺激素腺瘤发病率极低,至今全世界仅报道34例[2,10],因无特异性的临床表现,以及临床医生对它认识不足,导致误诊漏诊率高。但从我院收治的这5例患者的诊疗过程来看,对于这类疾病的诊断也并非无迹可寻,只要了解了这类疾病的临床特点,在手术前给出准确判断,使患者避免不必要的卵巢囊肿剔除手术是可实现的。垂体促性腺激素腺瘤是良性肿瘤[11],垂体前叶的促性腺激素细胞分泌过多的FSH和/或LH。过度分泌FSH者称为垂体FSH腺瘤;同理,过度分泌LH者则称为垂体LH腺瘤。在临床中FSH腺瘤较LH腺瘤更常见,也更易引发临床症状。这些肿瘤细胞分泌FSH和/或LH,不受雌激素、抑制素A的影响,提示正常的负反馈作用消失[12]。促性腺激素腺瘤可见于任何年龄的男、女病患,女性主要表现为月经紊乱和OHSS[13],男性表现为睾丸增大[1],儿童以性早熟为主要表现[2],绝经后女性因卵巢萎缩无功能,对FSH刺激不敏感,而往往无临床症状,直至垂体腺瘤长大成大腺瘤出现神经系统压迫症状时才被发现[2]。本文仅以生育年龄的女性患者为主要讨论对象。
一、临床特征
发病年龄以中青年居多,老人及儿童发病率偏低[14]。本文收治的5例患者中,发病年龄均在生育期,平均38.8岁。文献报道绝经前女性常表现为月经紊乱[15]、月经稀发、阴道点滴出血、月经过多、不育、溢乳[16]、或垂体肿瘤压迫症状[17]。容易与异常子宫出血及垂体泌乳素瘤导致的高PRL血症相混淆。女性患者最常见的临床表现之一是月经紊乱,类似于使用外源性FSH的症状,由于促性腺激素的过度分泌,刺激多个卵泡同时发育,E2分泌过多而引发相关症状,如月经紊乱、继发闭经、不规则阴道出血等。本文5例患者均有月经紊乱的症状。由于多个卵泡同时发育,双侧卵巢明显增大,引起腹痛、不同程度的腹膜激惹症状、雌激素水平异常升高,甚至出现OHSS,严重的OHSS可导致胸腔积液、腹水和血栓等。偶见因卵巢多房囊肿引起双侧卵巢扭转的急腹症。本文中有1例患者就是因怀疑“卵巢囊肿蒂扭转”而进行卵巢囊肿剔除术。溢乳、PRL升高是另一个常见的临床症状[18],可能的机制有两点:(1)过高的雌激素是PRL的刺激因子,导致PRL水平升高;(2)肿瘤体积增大压迫垂体柄,抑制下丘脑多巴胺向垂体的输送,使多巴胺的抑制性调节受阻,而引起高PRL血症,临床表现为溢乳。本文中有2例患者以月经紊乱合并溢乳为主诉而就诊。本文中仅有1例患者出现了因垂体腺瘤增大压迫周围组织引发的神经系统症状,头痛、视物模糊、视野缺损等。这类症状仅当肿瘤体积发展到大腺瘤时才会出现,在出现这一症状前多数绝经前的女性已因月经异常等临床症状而就诊,由于症状不典型,加之医生对该疾病认识不足,常按异常子宫出血给予控制月经的治疗。绝经后的女性患者,由于卵巢萎缩对促性腺激素作用无反应,大腺瘤压迫引发的症状可能成为诊断的主要线索。
二、实验室及影像学检查
性激素检查可为诊断提供重要的线索。育龄期女性的月经异常是常见的就诊主诉,性激素检查时发现雌激素水平异常升高,但FSH及LH水平未表现出受抑制状态。本文中5例患者雌激素平均值为7 800.66pmol/L,同时FSH均值为12.66U/L,并未受到明显抑制。分析其原因可能是垂体促性腺激素腺瘤分泌过多的FSH刺激卵巢中多个卵泡同时发育,导致雌激素水平不同程度明显升高,本文中患者雌激素水平最高达12 973.45pmol/L,而由于垂体FSH瘤持续分泌FSH,负反馈的抑制作用消失,即使过高的雌激素水平也未能负反馈抑制垂体分泌FSH,血清FSH水平在正常范围或轻度升高;高雌激素负反馈抑制下丘脑的促性腺激素释放激素分泌,导致LH水平低,如果同时存在垂体LH腺瘤时,LH水平亦不呈现降低状态;过高的雌激素也是PRL的刺激因子,另外大腺瘤压迫垂体柄阻碍下丘脑多巴胺向垂体的输送均是导致PRL升高的原因;卵泡上的颗粒细胞长期受到FSH刺激,成熟后分泌少许孕激素,血清孕酮水平轻度升高;子宫内膜长期受到雌激素作用,继而发生内膜病变。综上所述,最典型的激素变化特点就是高雌激素水平的同时未见促性腺激素的受抑制状态。影像学检查:盆腔超声检查5例患者均可见双侧卵巢均匀增大,可见多房无回声囊肿。这是因高FSH持续刺激卵巢使多个卵泡同时发育所致,其表现类似于行体外受精-胚胎移植过程中外源性FSH作用后的卵巢多卵泡同时发育的现象。垂体平扫+增强MRI是另一个主要的诊断手段,MRI扫描中可见鞍区占位性病变,呈现等T1、稍长T2信号,增强显示为类圆形强化减低区。如肿瘤体积过大,可见对周围组织的压迫现象。盆腔超声的改变有一定的特征性,但垂体MRI的改变仅能提供垂体瘤的影像学诊断依据,无垂体促性腺激素腺瘤的特征性表现。文献报道与我们5例患者的表现相同[3]。
三、治疗
手术治疗、放射治疗及化疗是主要的治疗手段。由于病例数较少,治疗方法是依据个案报道或小样本量得出的结论。外科手术切除垂体腺瘤是首选的治疗方法,术式主要采用神经内镜下经鼻蝶入路垂体腺瘤切除+鞍底重建术,手术可达到切除病灶、解除视神经压迫、改善内分泌功能障碍,并提供最终的病理诊断证据。术后免疫组化检测是主要的诊断依据。如手术成功可使促性腺激素分泌正常化,重建垂体正常的分泌功能,同时缓解高促性腺激素引起的临床症状[3]。我院收治的5例患者经垂体瘤切除术后,均恢复了正常的月经周期,相应的临床症状消失。文献报道过经垂体瘤切除术后月经恢复并成功受孕的患者[19-20],而我们这5位患者均无生育需求。垂体瘤切除术后3~4d,雌激素水平就可降至正常范围,随着FSH、LH水平下降,卵巢多房囊肿无需任何处理即可缩小直至消失,月经恢复正常。与文献报道的相符[21-22]。有文献报道手术治疗后发生低促性腺激素的情况[23]。我院收治的5例患者均未发生该情况。药物在垂体促性腺激素瘤肿瘤的治疗方面无肯定疗效。患者通常对于多巴胺激动剂或生长抑素类似物等药物治疗无反应[24]。少数病例尝试使用促性腺激素释放激素激动剂(GnRH-a)和拮抗剂治疗,也未获得能够使肿瘤体积缩小的证据[3]。虽然复方口服避孕药可达到控制月经的目的,多巴胺受体激动剂可降低PRL、控制溢乳,但这类药物仅能起到控制症状的作用,对于控制垂体肿瘤的生长及治疗作用无明显效果。如基础病变未去除,这些药物的治疗效果有限。故不推荐任何形式的药物治疗。由于垂体促性腺激素腺瘤是良性肿瘤,如手术中尽可能干净的去除病灶,手术后不需要任何形式的辅助放疗。
在这里强调的是如果能在患者就诊伊始就给出准确的判断,可使患者避免不必要的卵巢手术。本文5例中的4例患者均经历了腹腔镜下的双侧卵巢囊肿剔除术,有1例患者甚至进行了两次双卵巢囊肿剔除术。仅1例因在我院给予了及时的诊断,而避免了这一不必要的手术治疗。我院的临床观察及文献报道均证实[13],对于因垂体功能性促性腺激素瘤引起的卵巢多房囊肿,在去除了垂体腺瘤后,双侧卵巢多房囊肿可自行消失,无需任何手术或药物治疗。由于该病的非典型性和临床医生对该疾病的认识不足导致了误诊,给患者带来了本无需实施的手术治疗。因此认识这一疾病的特点就显得很重要。我院收治的5例患者随诊至今无复发。这些患者中有1例曾在外院完成第一次垂体瘤手术切除,但术后3年症状复发,4年发现肿瘤复发,在我院二次手术后随访至今3年多,无复发迹象。这例患者的垂体腺瘤复发的原因不得而知,不能完全排除首次手术未能切除干净的可能性。我院的病例术后随访时间尚短。文献报道中,有随诊5年无瘤生存的报道[3,25],也有肿瘤复发的报道[13]。预后究竟如何,仍需要大样本长时间的随访观察。总之,垂体功能性促性腺激素腺瘤是一种非常罕见的异常分泌FSH和/或LH的肿瘤,基于目前的认知及临床特点和有限的临床数据,做到早期诊断和给予正确的治疗,避免不必要的卵巢手术操作是完全有可能实现的。当绝经前女性出现月经紊乱、溢乳、头痛、视野缺损、反复发生的卵巢多房囊肿、雌激素异常升高的同时促性腺激素未被负反馈抑制时,应行垂体MRI检查,如发现垂体肿瘤,应考虑垂体功能性促性腺激素腺瘤的可能。垂体腺瘤切除术是首选的有效的治疗手段,术后应长期随诊性激素水平、盆腔超声及垂体MRI。
参考文献略。
原始出处:
王含必,姚勇,邓成艳,幸兵等,垂体功能性促性腺激素腺瘤临床病例分析[J], 生殖医学杂志,2020,29(2)。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#促性腺激素#
77
#功能性#
48
#促性腺激素腺瘤#
71
#临床病例分析#
59
#垂体#
81