Cell:特稿!50年儿童癌症研究历史,突破和展望!
2024-04-23 儿童肿瘤前沿 儿童肿瘤前沿 发表于陕西省
文章回顾了五十年来儿童癌症治疗和研究领域的重要进展,更是对未来提出了展望和建议。
近日,在创刊五十周年之际,Cell 发布了癌症特刊。来自美国科罗拉多儿童医院的 Lia Gore 和Maureen O’Brian 联合撰写了题为 Only the beginning: 50 years of progress toward curing childhood cancer 的评论,回顾了五十年来儿童癌症治疗和研究领域的重要进展,更是对未来提出了展望和建议。

五十年前的七十年代,儿童罹患癌症几乎是被判处了死刑。五十年后的今天,儿童癌症的总体存活率已经超过85%。由于基因组学、免疫学、外科技术、放射治疗、免疫治疗等领域的巨大进步,多种儿童癌症的存活率有了大幅提高。但同时,也有少数病种,如婴儿急性淋巴细胞白血病、转移性骨肉瘤、扩散型内因性脑桥神经胶质瘤等,患儿预后仍然不理想。另外,一些高危神经母细胞瘤和髓系白血病虽然存活率提高,但治疗产生的毒性对患儿后续生活质量产生严重影响(如下图)。故而,过去五十年成功经验的总结,也是下一个五十年许多工作的基础和开端。
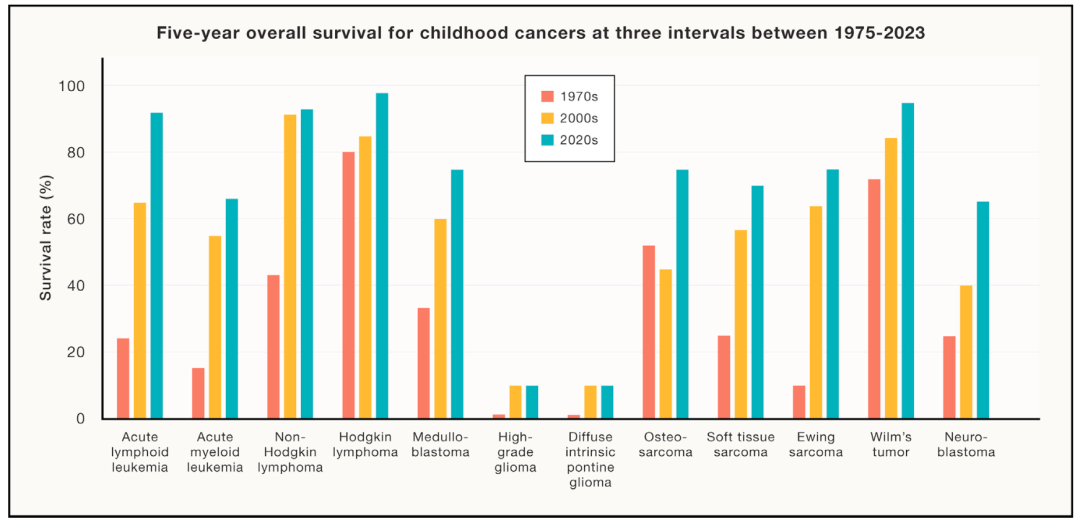
过去五十年:关键进展和里程碑
1. 多中心的联盟组织和工作组
儿童癌症相比成人癌症,发病率低,病人数量少。癌症在15岁以下发病率为10万人17.4例,15-39岁为10万人75.3例,40-64岁为10万人534.4例。在全球,每年新增癌症患儿大约为30万人。虽然这不是一个小的数字,但细分到各癌症种类,不一定能满足当下研究需要的人数。建立合作组对招募患儿、开展有效的研究至关重要。
上世纪八十年代,美国的儿童癌症工作组(Children’s Oncology Group, COG)成立,发展至今有超过200所成员机构。2007年,欧洲的国际儿童癌症组织(Societe Internationale d’Oncologie Pediatrique Europe)成立,在欧洲有35个成员国。这些组织通过多中心甚至多国联合招募患者,在近年进行了大量的大规模研究,在寻找驱动基因突变、优化治疗方案、新药试验和预后追踪等领域都作出了大量贡献。
2. 危险度和预后的细分
随着肿瘤组织学,特别是基因组学和转录组学的研究成本降低,结合对药物的反应,可以对每一种癌症进行更细致的危险度细分。低危组可以尝试更低剂量的治疗,减轻毒性;高危组则需尝试更激进或新的治疗方案,以提高生存率。
髓母细胞瘤是儿童中最常见的脑瘤:过去是按照是否有转移和切除范围来划分危险度;而如今,在大量研究的基础上,髓母细胞瘤则根据转录组学表现,分为WNT、SHH、group 3和group 4,同时考虑TP53突变和MYC/MYCN扩增,在此基础上进行危险度划分。这个分子学疾病分类和危险度分层已经正式写入WHO的髓母指南。
在急性白血病的治疗中,曾经通过在光学显微镜下看血液涂片来判断用药后的缓解情况。而如今,标准操作是运用流式细胞技术和聚合酶链反应,这类高精度高敏感度的技术能检测到极低的残留灶,准确判断疾病对药物的反应程度。
对高风险的神经母细胞瘤,若干联盟组织的临床试验显示,半定量的间位碘代苄胍(MIBG)扫描得到的居里值(Curie Score)和预后相关性很高。
3. 阐明驱动基因突变
找到一个癌症的驱动基因突变,对理解其病理发展和对其进行靶向治疗具有重大意义。
TARGET项目(Therapeutically Applicable Research to Generate Effective Treatments,由NCI发起)和类似的荷兰发起的研究项目,发现具有费城染色体的急性淋巴细胞白血病是一个特殊的亚型。费城染色体阳性的患儿,其转录组学和其他急淋患儿有所不同,预后也较差。根据这一基因突变特点,现在有若干临床试验正在测试靶向药酪氨酸激酶抑制剂(TKI)是否可以针对性提高这一亚型的存活率。
类似的,拉罗替尼(larotrectinib)是一种原肌球蛋白受体激酶(TRK) 抑制剂,在TRK融合突变阳性的患儿组显示出良好的效果。
间变性淋巴瘤激酶(ALK)抑制剂在ALK融合突变阳性以及ALK驱动的神经母细胞瘤患儿身上显示了较好的效果。
4. 优化治疗,减轻毒性
除了发展靶向治疗,研究人员也在不断优化现有的治疗方案,包括对有生物毒性的化疗的剂量和组合的优化,调整放疗、手术,以及血液干细胞移植的方案。
通常来说,儿童比成人更能耐受高毒性的治疗,因为他们的器官受到的时间和环境造成的累积毒性更小。但同时也必须考虑儿童癌症康复者的长期预后。
上世纪七十年代,圣裘德儿童医院在儿童急淋治疗上做出了一个重大进步。他们运用颅内放疗来预防急淋在中枢神经系统的复发,大大提高了患儿的生存率。但是,颅内放疗带来了长期的神经认知功能、内分泌和血管并发症,以及继发的癌症。此后,颅内放疗被强化脊椎腔内和全身化疗取代。由此可见,治疗方案随着人们的认识在不断进步。
另一个例子是将半定量的间位碘代苄胍(MIBG)用于神经母细胞瘤治疗。以及运用质子束来精准放射治疗癌症,减少放射物质的散射,减少对患儿短期和长期的毒性。
5. 开创性的免疫治疗
免疫系统在癌症发生、发展过程中都有重要作用,同样也可以用于治疗。免疫治疗的发明无疑是开创性的。
著名的CAR-T(Chimeric Antigen Receptor)嵌合抗原受体T细胞疗法,在部分复发性B细胞急淋患儿身上实现了长期治愈。
除此之外,其他类型的免疫疗法也值得关注:
-
单克隆抗体(Monoclonal antibodies,moAbs):模仿身体免疫系统产生的抗体,对癌细胞进行攻击。代表:利妥昔单抗(rituximab)可用于成熟B细胞非霍奇金淋巴瘤;达妥昔单抗(dinutuximab)可用于神经母细胞瘤。
-
双特异性T细胞衔接器(Bispecific T cell engagers,BiTEs):可以识别两种单链可变区,激活T细胞杀死癌细胞。代表:贝林妥(blinatumomab)可用于复发的B细胞急淋。
-
抗体药物偶联物(Antibody-drug conjugates,ACDCs):将单克隆抗体和强效高毒性小分子毒物偶联,靶向清除癌细胞。代表:布妥昔(brentuximab)可用于霍奇金淋巴瘤。
6. 不可遗漏的康复者研究
由于癌症治疗常具有生物毒性,对康复者,特别是儿童癌症康复者的研究,对提高患儿长期的生活质量尤为重要。
癌症治疗中以及治疗后,患儿会受到来自各种治疗的短期和长期的毒性影响,包括但不限于神经认知功能障碍、骨坏死、心脏毒性、继发癌症、生育和内分泌障碍等等。
对急淋患儿的针对性追踪研究是一个好例子。如前所述,由于追踪研究中发现的各种毒性,医生们弃用了高效的颅内放疗。另外在使用蒽环类药物化疗时,医生会加用右雷佐生来保护患儿的心脏功能。
在霍奇金淋巴瘤患儿中,医生们减少了烷化剂的使用,保护患儿的生育功能。
在青少年急淋患者中,医生们将地塞米松的用量调整到中等,以减少骨坏死发生的可能性。
下一个五十年:挑战和机遇
虽然在过去的半个世纪,儿童癌症的研究和治疗上取得了很多进步,总体生存率提高到了85%。但现实中,仍有不少患儿死于癌症,部分癌症种类的生存率较50年前没有明显改善。要改善这最后15%患儿的预后,将比治愈前85%的患儿更困难。
需要的是国际层面上,包括基础研究、生物技术、生物制药以及监管部门紧密协调的合作;也需要更先进的生物信息技术,癌症和宿主基因组学研究,以了解相关癌症基因的致病倾向、药物基因组学以及肿瘤微环境;还需要注重控制医疗费用,提高新疗法的可及性。而挑战主要有:
1. 新技术的运用与瓶颈
现在,全外显子组测序和单细胞转录组测序的价格已经越来越可负担。大量的数据被采集和储存,理想情况下可用于指导治疗。
药物基因组学有一个例子,对于硫嘌呤代谢相关基因有突变的患者(TPMT,NUDT15),应当调整用药剂量。
但总体来说,如何在肿瘤和患者层面,将这些大数据和治疗方案直接联系起来,仍没有解决。在欧洲和美国,若干个大型倡议组织致力于收集和分享大数据,从中了解如何用基因组学数据指导治疗。
2. 进一步了解突变
生殖系突变发生于早期胚胎,存在于全身每一个细胞,决定了癌症基因的致病倾向。不仅要在已经被诊断的患者身上了解他从遗传中得来的基因突变,也应当为其家庭提供相关咨询,并且监测其他可能有风险的亲属。由此,我们将可能更好地做到早诊断、早治疗,从而提高患儿的生存率和预后。
体细胞突变则是发生在部分细胞中的突变,在癌症研究中常指导致癌症或在癌细胞中发现的突变,对于癌症的发生、癌症干细胞、肿瘤代谢、肿瘤微环境、免疫反应以及对治疗的反应都有重要作用。在这些方面,我们所知的还远远不够。
虽然在白血病和淋巴瘤上,免疫治疗取得了巨大的成功。但要将其推广到其他目标细胞,多种目标细胞,实体肿瘤甚至中枢神经肿瘤,我们还需要大量的相关性分析,来寻找和理解免疫治疗需要的“正确的细胞种类”。同时,免疫治疗高昂的费用也是此类研究的一个巨大障碍。
3. 穿越血脑屏障
儿童癌症治疗通常较成人更注重对中枢神经系统的预防性治疗,以避免神经系统受累。因而,药物如何越过血脑屏障,对治疗中枢神经系统原发肿瘤、转移肿瘤以及白血病都很重要。
目前,人们正在研究质子束治疗是否可以使部分病人减少被照射的组织,以减少长期的毒副作用。
新兴的免疫治疗对中枢神经系统作用能力不一:如CAR-T很有效,但ADCs和BiTEs则几乎无效。
因而,如何运用有机或无机微颗粒,通过细胞运载,或对流增强递送,来加强药物对中枢神经系统的作用,治疗和减少中枢转移,减轻中枢放疗的副作用,是未来一个重要的议题。
4. 分子诊断和细分病种
分子生物学和基因组学研究证明,目前的病种分类仍然过于粗糙。根据分子诊断进一步细分是不可避免的趋势。
儿童癌症本身已经是罕见病,要将病例进一步细分,必须通过全球合作招募患者,才可能增加临床试验的样本数量,达成有效的研究。
这需要监管部门对全球性的儿科临床试验进行鼓励。经济上,由于儿童癌症市场过小,研究常落后于同类疾病在成人中的研究,一些小公司可能无法支撑到盈利就已被迫退出。政治上,国家之间的政策的不稳定,也可能对国际研究造成重创。这些都需要监管部门的协作和努力。
5. 利益至上的大环境
在2020 年,研制一种新的癌症药物需要花费7.65亿到46亿美元。若要在一种罕见的儿童癌症上收回投资,基本是不可能的,除非该药可以大量用于其他疾病。因此,尽管研究领域尽力前行,我们在实际药物研发上需要大量金钱和技术的投资。
另外,当药物的专利期结束后,由于利润降低,厂家可能选择停止生产,这对一些患者来说是致命的;监管部门的政策激励和引导在这个环境下非常重要。
现在很多癌症需要多种药物组合治疗,有1+1>2的效果。若这些药剂来自不同厂家,而厂家并不想共享药剂,则可能阻碍运用组合治疗的临床试验。针对这一困境,监管部门、癌症倡议者、欧洲和美国的学界正努力从各方面促进多药组合临床试验。这将大大拓展儿童癌症治疗的可能性。
6. 青少年和年轻人患者隐身
目前,青少年和年轻人(15-39岁)的癌症相关研究和临床试验都严重缺乏。对这一群体来说,缺乏经济支持、缺乏保险保障较其他年龄组更严重。
近期的霍奇金淋巴瘤研究试图改善这个问题。研究证明有针对性地提供资源和支持,能改善青少年和年轻人患者的预后。
7. 地域之间的不平等
总体来说,儿童癌症生存率最高是在高度发达的国家。这些地区不仅为患儿提供了良好的医疗环境,也在经济、社会、教育和家庭需求等各个方面提供相对好的支持。
而地域之间的不平等是多层次的,不仅发生在发达的国家地区和不发达的国家地区之间,也发生在同一个国家内部,更发达和相对欠发达的地区之间。中低收入国家/地区,癌症患儿的弃诊率和死亡率都显著高于高收入国家/地区。
必须竭力推进癌症治疗的可及性、尽力解决这种不平等性,否则总体理想的儿童癌症治疗和预后是无法达成的。
结语
我们达成了很多成就,但还有更多需要做的,为了那些尚无法治愈的患儿,以及那些因治疗而承受短期或长期毒副作用的康复者。
一种癌症如果对药物不抵抗也不转移,它是不会致命的。而关于药物抵抗和癌症的转移,还有许多需要研究的。我们需要更好的指标来监测治疗效果和预测复发可能。
简言之,需要大型的国际性临床试验来确定生物学或基因组学的指标对疾病和对治疗的意义,来定义新的亚型,定义某一小组患儿应该接受什么程度的治疗,才能得到最好的疗效,且副作用最小。
在全球范围改进儿童癌症治疗是个巨大的挑战,地理、经济、基础设施、医疗条件都可能是巨大的障碍,但这是我们必须面对和致力改变的。
希望在Cell的下一次特刊,我们可以写一篇:“儿童癌症:从全员死亡到全员治愈”(Pediatric Cancer: From uniformly fatal to uniformly cured)。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#儿童癌症# #研究领域#
30