免疫识别理论的演变
2024-12-11 小药说药 小药说药 发表于陕西省
文章回顾免疫学中多种免疫识别理论,包括克隆选择理论、双信号理论等,分析各理论优势及局限性,指出目前虽有微观层面理论,但缺乏解释免疫系统整体行为的通用理论,期待未来能有新突破。
免疫系统的进化是为了保护宿主免受病原体、肿瘤和毒素的侵害,并促进组织修复。为了应对宿主每天面临的威胁,免疫系统必须识别并阻止或减轻来源广泛的攻击物,保护自身结构(即必须有自我耐受性)和外来非攻击物(即必须对共生和互惠生物有耐受性)。此外,免疫系统还会对过去的攻击物反应更快、更强、更特异,这一特征被称为免疫记忆。
目前,克隆选择理论(CST)是当前用于解释免疫识别和免疫记忆的基础和核心。然而,CST对许多问题,比如自身免疫耐受的局限、抗原变异和多样性以及交叉反应等无法做出完美解释。在过去的几十年里,人们对CST理论做出了扩展和修改并提出新的理论,以解释一些新的实验证据,例如抗原呈递细胞(APCs)、T细胞和B细胞之间的相互作用、T细胞无能以及佐剂诱导免疫反应。虽然到目前为止,还没有一个提出的理论能够完全解释免疫现象的全部,但免疫识别理论的发展已经极大地促进我们对免疫学和相关疾病的认知,也将推动自身免疫、肿瘤免疫药物以及疫苗的开发。
克隆选择理论的前提是,在生理条件下,免疫系统能够耐受自身成分,并通过调节淋巴细胞的数量、类型、成熟程度和反应阈值来产生对外来抗原的免疫力。淋巴细胞由于其抗原结合受体上存在独特的可变区而具有抗原特异性。免疫球蛋白(Ig)和T细胞受体(TCR)是两种类型的抗原结合受体,分别定义了两种主要类型的淋巴细胞,即B细胞和T细胞。
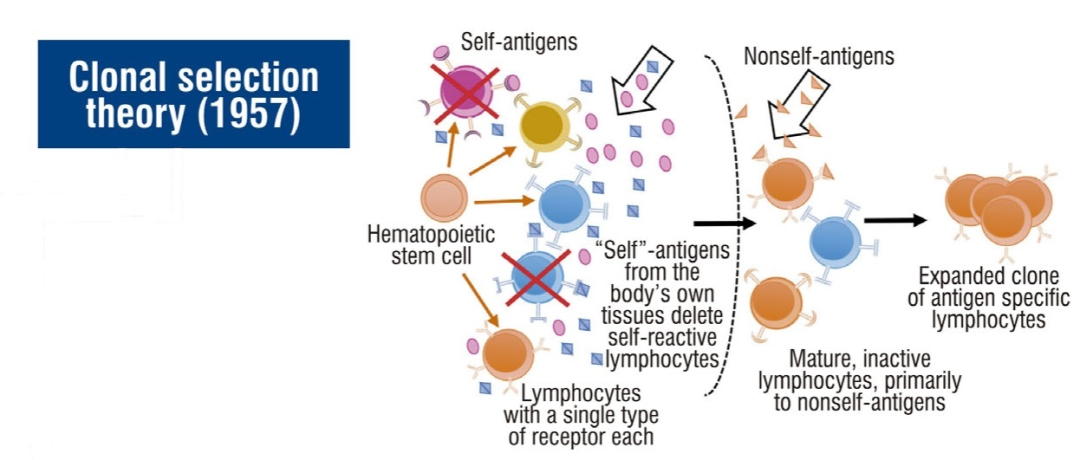
CST最早由Burnet于1957年提出,它基于Jerne的自然选择理论和类似于Talmage提出的概念。CST解释了免疫系统如何对抗原作出反应并形成记忆:(A)每个淋巴细胞及其克隆后代都携带一个抗原结合受体的单一克隆,该克隆具有独特的特异性,是由基因片段的重组和抗原结合受体可变区的突变随机产生的;(b) 抗原结合受体诱导细胞活化、增殖和分化,否则不会活化;(c) 被招募的细胞负责对抗感染或癌细胞,并产生处于休眠状态的记忆细胞,该记忆细胞准备在与抗原进一步接触时被再活化;(d)在初级淋巴器官的个体发育过程中,携带自身分子受体的淋巴细胞都会被清除,或者在外周受到其他机制的抑制。根据最后一个假设,可以得出结论,根据CST,免疫系统通过不检测或在意外检测时忽略自身分子来区分自我和非自我。
然而,CST并没有完全解释以下免疫现象:(一)T和B细胞的阳性选择;(ii)天然自身抗体和天然自身免疫;(iii)致病性抗原的低剂量和高剂量耐受性;(iv)无能;(v) 需要佐剂和T细胞-B细胞协同诱导免疫反应;(vi)独特型网络。
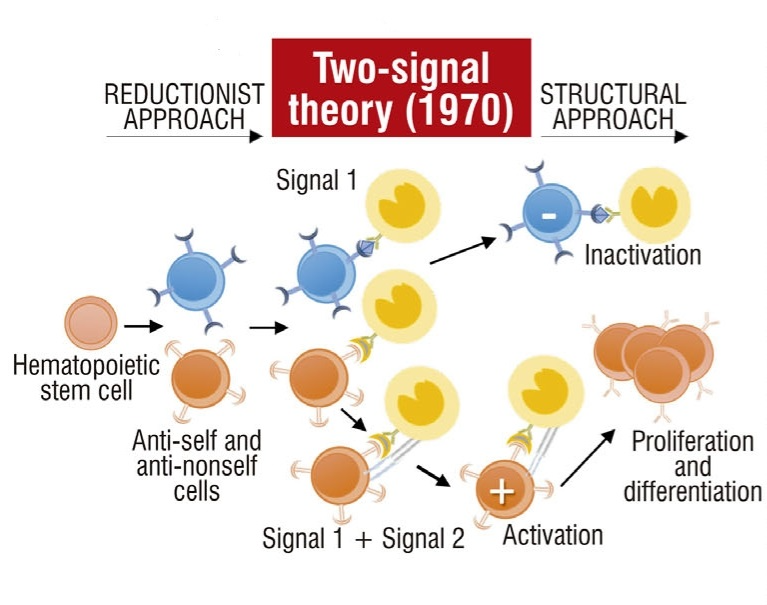
Bretscher和Cohn的“两个信号”/“抗原的关联识别”理论接受了大多数CST框架,包括自我-非自我辨别的需要,但认为淋巴细胞激活有以下限制:(i)为了被激活,淋巴细胞必须接收两个信号:来自其抗原结合受体的信号1和来自效应调节细胞(T辅助细胞)的信号2,效应调节细胞“告诉”第一个细胞其行为应该是什么;(ii)如果淋巴细胞仅接收信号1,则其无法激活。因此,对自身抗原具有特异性的新出现的克隆将通过接收信号1立即失活,这解释了无能的机制和必要性,这一理论主要基于实验证据。
然而,双信号理论并不能解释以下现象:(a)过继转移到主要组织相容性复合体(MHC)缺陷个体的幼稚T细胞寿命显著缩短;(b) 成熟B细胞和T细胞中细胞表面Ig或TCRα链基因的有条件敲除也会导致细胞快速消除;(c) 骨髓中的B细胞输出大大超过了存活进入幼稚B细胞再循环池的细胞数量;(d) 缺乏或存在寡克隆B细胞的小鼠TCR Vβ多样性大大降低,注射多克隆而非单克隆、Ig或Fab片段可以恢复T细胞多样性;(e) 健康个体中存在“病理性”抗自身T和B细胞,如抗dsDNA和类风湿因子,以及在感染或非特异性炎症期间其滴度的增加;(f) 独特型网络。
Janeway和Matzinger的模型也接受了大多数CST模式,并基于双信号模型。然而,他们假设刺激免疫反应的主要因素是通过先天免疫机制识别“危险”或“陌生人”信号以及抗原。APC通过模式识别受体(PRRs)识别这种“危险”或“陌生人”信号,一旦激活,APC向淋巴细胞提供信号2。因此,根据陌生人/危险信号理论,免疫系统进化为区分自我和传染性非自我,免疫系统的破坏性效应器功能仅针对危险因素。更具体地说,APC中存在的PRRs对病原体相关分子模式(PAMP)的识别将激活这些细胞,然后这些细胞将吞噬和处理病原体,并将相关的MHC肽呈递给幼稚T细胞。
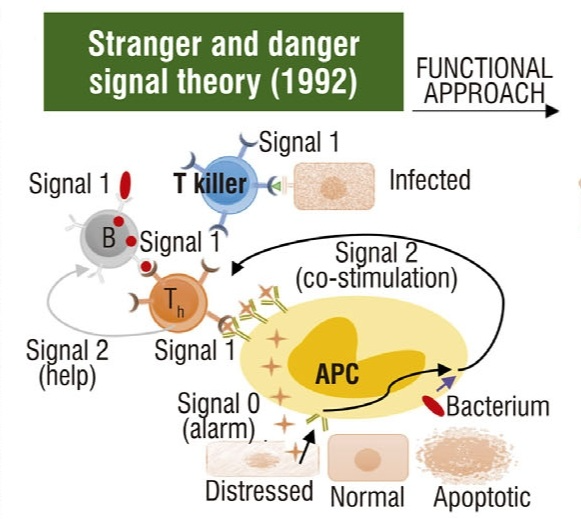
Janeway关键性地假设PAMP在本质上是非自我的。然而,后来的研究表明,自身分子也可以激活PRRs,PAMPs也存在于非感染性生物体中,如正常的肠道菌群。因此,Janeway关于“陌生人”只存在于传染性非自我中的假设并不成立。为了解决这个问题,Matzinger声称,免疫反应不仅是由外来分子触发的,而且是由“来自受损细胞的内源性细胞警报信号”触发的。因此,如果自身成分发出危险信号(如细胞压力或破坏),它们可能会引发免疫反应;如果非自身成分不危险(例如胎儿或共生细菌),则可以耐受。此外,危险信号理论还声称,在存在危险的情况下发生的自身免疫不会持续,因为在危险信号消除后,外周耐受机制将迅速启动以控制免疫系统。
然而,反对危险信号理论的人认为,危险的概念是拟人化的,没有得到很好的定义。例如,细胞可以因坏死而死亡,而不会对生物体的组织造成损伤,并且可以对无害抗原(如过敏原或食物抗原)产生免疫反应。此外,如果免疫系统使用物理因素(注射途径、浓度、聚集、定位等)或PRRs作为触发免疫反应的主要决定因素,它就无法做出抗原特异性免疫反应所需的躯体选择决定。最后,损伤是由免疫系统本身引起的,然后生物体很容易进入无限的免疫激活正反馈回路。
功能识别理论是危险信号理论的延伸,该理论提出免疫识别可以在没有抗原特异性结构识别的情况下发生。在识别出攻击行为后,免疫系统会触发效应机制来维持体内平衡。根据免疫细胞活化和细胞因子释放的特征,将反应分为Th1、Th17或Th2型。Th2反应由蠕虫、毒素和过敏原诱导,由先天2型淋巴细胞和CD41 Th2细胞协调,产生细胞因子IL-4、IL-5、IL-9和IL-13。Th2免疫原不具有共同的结构特征,似乎不能被PRRs直接识别。功能识别理论提出,Th2免疫原通过其功能特性被识别,例如促进损伤相关分子模式的释放和激活感觉神经元的能力。因此,具有相同性质(蛋白酶、碳水化合物活性酶、配体结合蛋白等)但结构不同的Th2抗原会引发相同的免疫反应。
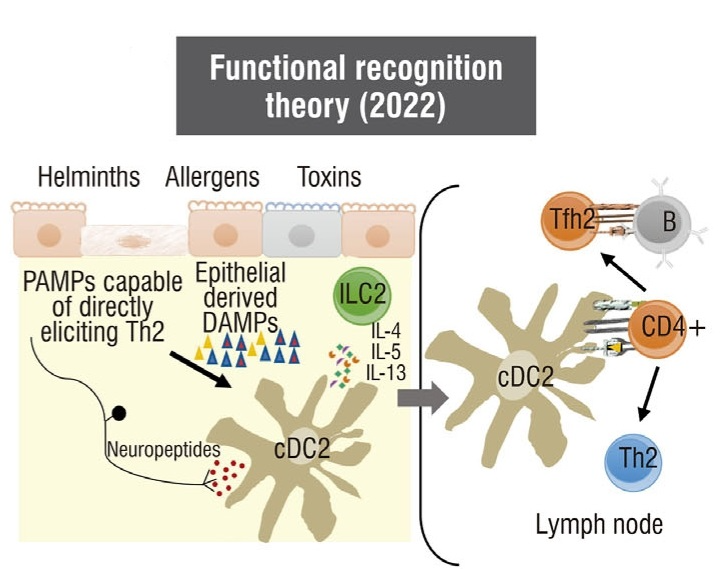
然而,功能识别理论存在不确定性,例如缺乏内在佐剂性的抗原如何产生适应性Th2免疫反应?先天性和适应性2型反应如何在体内被不同地激活?以及屏障部位的功能识别如何诱导组织驻留记忆?并且这种记忆在炎症后会持续变化。
Pradeu和Carosella设计了“连续性准则”,试图更好地解释有悖于“自我-非自我”辨别的免疫原性概念。CST根据对外来物的识别解释了为什么以及何时发生免疫反应,然而,CST的自我概念并不能解释为什么自我成分经常引发免疫反应,而许多外来成分被生物体耐受。为了解决这个问题,他们提出免疫系统耐受一组内源性和外源性抗原,每天以一定的频率与这些抗原接触,免疫反应是由这些抗原模式的不连续性引发的。不连续性被定义为:[1]某种抗原数量的变化;[2] 新抗原和系统已经适应的抗原之间的分子差异程度;以及[3]新抗原模式的出现速度(接触频率的变化)。因此,连续性标准与自我-非自我理论的区别在于,免疫原性标准不是抗原的来源,而是相关组织的变化速度。
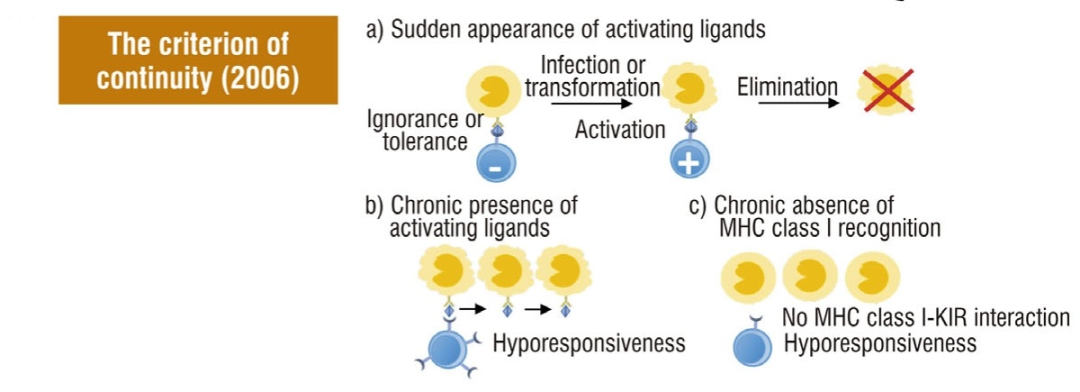
然而,这个理论潜在的问题是,连续性准则在定义触发免疫反应的“抗原模式改变”的构成方面缺乏特异性。此外,连续性准则仍需要更多的实证验证,以证明其在不同免疫背景下的有效性和适用性。
在20世纪60年代初,两个独立的研究小组表明,抗体也可以作为抗原发挥作用,引发针对其可变区域的特异性Igs的产生。然后创造了独特型和抗独特型,分别指代免疫球蛋白可变区上的抗原决定簇和针对这些结构的抗体。
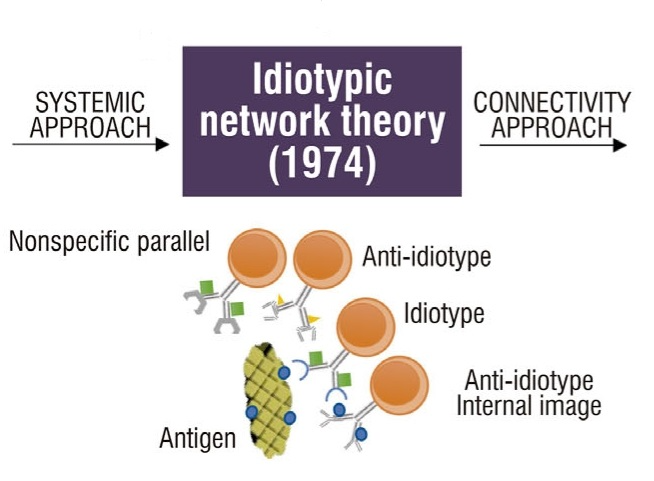
十年后,Jerne提出了“免疫网络假说”,该假说认为,识别其他免疫球蛋白不同部分的抗免疫球蛋白的存在将使网络中生物体的所有淋巴细胞相互连接。当时,Jerne根据每个人能识别的Ig可变区部分预测了两种抗独特型抗体子集。一个子集将针对不负责抗原结合的独特位,称为抗独特型集。另一个子集将针对与抗原结合位点重叠的独特位,因此,其独特位类似于抗原的构象结构。Jerne将第二个子集称为抗原的“内部图像”。已经表明,内部图像不仅在形状上而且在功能上都与抗原相似,在某些实验条件下,它们可以刺激针对抗原的特异性抗体的产生。此外,Jerne提出,独特型网络理论(INT)将是解释免疫前库选择、自然自身免疫、记忆和外周耐受的关键,因为抗抗体的反馈控制足以在不与抗原接触的情况下确定和维持免疫库,并抑制自身免疫性疾病的发展。因此,对于INT,耐受性和免疫反应是网络的特性,当与抗原接触时,它能够控制具有自身独特型的克隆,并激活其他抗原特异性的克隆。
INT引入的系统网络视图也允许在免疫系统和中枢神经系统之间进行比较。免疫系统和神经系统之间的相似性在成分水平上似乎并不显著,但在系统行为水平上却很强。两者都构成了由大量相互连接的细胞组成的网络,这些细胞通过刺激和抑制相互作用相互连接;这两个系统遍布全身,可以对各种各样的环境刺激做出反应;两者都能区分自成分和非自成分;神经元和淋巴细胞都表达神经递质和Ig表基因家族(如TCR)的基因;最值得注意的是,这两个系统都能够学习(记忆),而不能通过遗传机制将获得的信息直接传递给下一代。由于这些相似之处,自20世纪70年代初以来,许多INT信徒一直在提出,理解免疫系统的进展可能会为理解大脑带来新的想法。
然而, INT的反对者强调了以下几点问题:(a)它没有提供详细的机制来解释免疫系统如何对抗原做出反应;(b) 它没有说明在T和B细胞个体发育、无能、自然自身免疫、背景(注射途径、佐剂等)和先天免疫(树突状细胞、PRRs等)中的阳性和阴性选择在免疫反应中的作用;(c) 没有提出任何机制来确保INT工作所需的高连接级别,并且无法调节未连接的克隆;(d) 在小鼠中注射抗体并不总是产生抗独特型抗体;(e) 该理论并没有导致其在免疫学方面提出的任何实际改进,例如使用内部图像开发疫苗。
INT的继承者们对INT进行了扩展和修正,他们试图解决原始理论中没有解释的问题。然而,INT的所有这些后验理论发展都是使用系统方法进行的,在细胞或分子免疫学水平上没有提出可测试的机制。
Coutinho创造了“完全”一词来解释抗体库的形成和网络的高度连接性。对他来说,独特位之间的交叉反应性是如此之高,以至于每个细胞都会被至少另一个细胞识别,每个抗原都会在系统中找到一个交叉反应的独特位。这种高连接性将产生一个完整的免疫库,能够识别所有自身和非自身抗原。然而,Coutinho的哲学完全性概念是不可检验的。Langman和Cohn认为,“完全”一词只能意味着无限,由于小鼠只有大约108个淋巴细胞,其受体库不能是无限的。此外,他们指出,高交叉反应性无助于这一论点,因为如果一个结合位点对很多不同的分子都有亲和力,那么它就没有真正意义上的特异性。此外,由于可证伪性是将科学与非科学区分开来的一个划分标准,因此可以认为,不可检验的完全性概念也是不科学的。
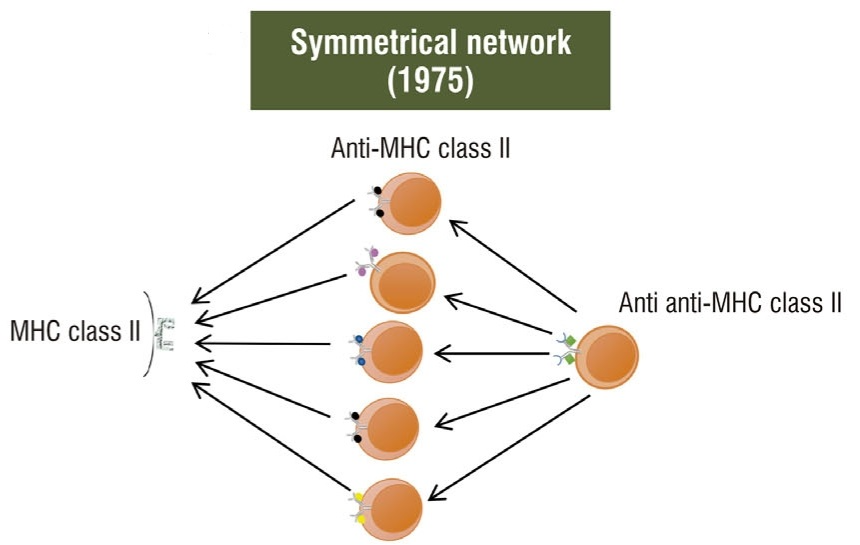
“对称网络理论”最早由霍夫曼于1975年提出,并在接下来的几年里进行了修改,以适应新的实验证据。对称网络理论修改了Jerne的各种抗独特型抗体,认为对于可以形成免疫反应或耐受的每种抗原,免疫系统中都存在两组相应的独特型:(a)通过互补相互作用(互补图像)识别抗原的独特型;(b) 识别抗原抗体可变区的独特型,因此在功能上与抗原相似(内部图像)。换句话说,只有当抗原与至少一个独特位基因相似时,它才是抗原。从这一假设中可以得出,免疫系统只会识别、处理和响应系统中编码为内部/互补图像集的抗原,独特型网络是决定免疫库大小和多样性的一个因素。
Cohen提供了一种处理自身免疫的替代范式。他的“认知范式”基于INT和二阶控制论原理,即任何收集和处理信息的系统都会通过对其主体的内部表示来最有效地完成工作。他还认识到克隆选择的发生,以及在锻造免疫系统中最重要的力量是由传染性病原体施加的力量,但他认为免疫系统的目的是提高生物体对环境的适应性,而不是区分自我和非自我或对抗危险。
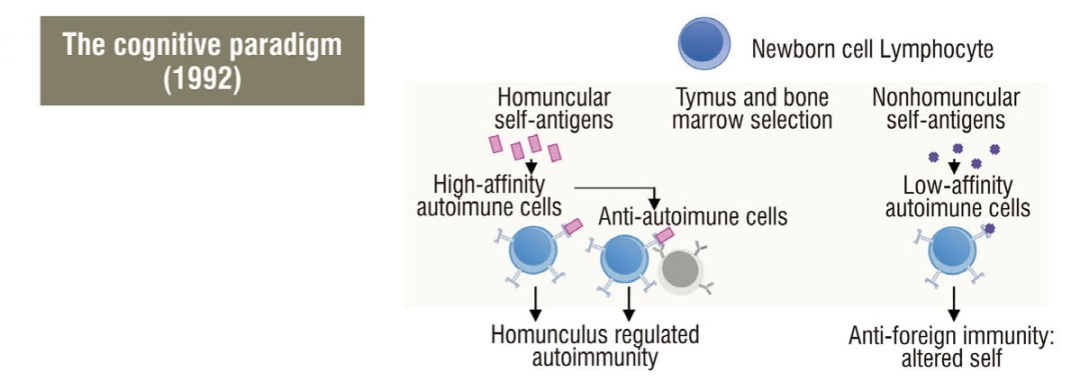
Cohen的认知范式可以概括为以下假设:(i)病原体、自身和炎症背景的原始内部表征在基因组中编码,独立于淋巴细胞的抗原受体(例如toll样受体、细胞因子和补体成分);(ii)APC使用这些受体(原始内部表征)来感知抗原;(iii)APC分解抗原,以破坏分子噪声,并将淋巴细胞的注意力集中在与背景一起呈现给它们的特定分子信号上;(iv)淋巴细胞库是在体细胞上产生的,但在个体发育过程中形成,以记录后来的抗原体验,并不旨在产生自我耐受。因此,它可能包括对一些自我识别细胞的积极选择,以及对不识别自我的细胞的消极选择;(v) 在早期发育阶段,母亲还通过胎盘和乳汁转移抗体和细胞,为后代的淋巴细胞库提供直接外部环境和自身的图像;(vi)背景和感染的种系图像、自我图像和母亲对环境的图像构成了一个参考点,定义了系统应该寻找和记住哪些抗原;(vii)该系统由至少三个不同的相互连接的网络组成:先天免疫细胞(APC、补体、自然杀伤细胞等)、T细胞和B细胞。这三个细胞网络共同作用,就像大脑或计算机一样,使用并行处理来分析接触时病原体的不同特征,并作为一个团体决定做出何种反应。
认知范式也没有提供细胞或分子水平的详细机制,解释免疫系统如何处理抗原并整合其背景以产生免疫反应,无能在认知过程中的作用是什么,以及免疫记忆是如何形成和储存的。免疫反应无疑是多因素的、复杂的和情境性的,但免疫学家需要的是一个合适的解释和预测框架来设计和进行研究。
在这里,我们回顾了当今主导免疫学框架的主要理论和假设。所提出的大多数概念有助于对这一科学领域的基本理解,并有助于更好地理解自身免疫性疾病和癌症治疗的疾病病理生理学和临床进展。然而,完全了解免疫系统对人类的潜在益处仍然远远超出了我们目前的能力范围。
大多数实验免疫学家都同意这样的观点,即不需要一个事实或概念适用于所有可能的情况。此外,同一问题可能有多种解决方案,有时进化已经测试并指导了同一生物体中存在多种解决方案。因此,免疫学史上充满了两种对立理论被证明部分正确的例子。一个很好的例子是Ehrlich和Metchnikoff的发现之间的明显对立,这引发了“二分法思维”,以发现免疫反应是先天的还是适应性的,或是细胞的还是体液的。
到目前为止,我们有很好的理论来解释免疫学在微观层面上是如何起作用的。我们可以详细描述抗原是如何被免疫系统识别的,以及它是如何触发效应器反应的。然而,我们并没有在同一水平上理解更一般的问题,比如当宿主接触到病原体、毒素或过敏原时,他会对哪些抗原做出反应或耐受。这表明,免疫学需要一个更一般的理论来解释免疫系统的整体行为,类似于物理学的“统一理论”。这一理论可能是未来新的实验证据衍生出的全新概念的产物,让我们期待未来能给我们答案。
参考文献:
1.Theories of immune recognition: Is anybody right? Immunology.2024 Oct;173(2):274-285
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#肿瘤免疫# #免疫识别理论#
9