克罗恩病内外科治疗决策1例分享
2013-07-27 北京大学第一医院 姜勇 汪欣 王化虹 王鹏远 李俊霞 中国医学论坛报
克罗恩病(CD)的治疗目前以内科治疗为主,但相当部分CD患者最终难以避免手术干预,因此CD治疗过程中,需要内科医师与外科医师密
 |
  |
 |
克罗恩病(CD)的治疗目前以内科治疗为主,但相当部分CD患者最终难以避免手术干预,因此CD治疗过程中,需要内科医师与外科医师密切配合,开展多学科综合治疗(MDT),准确评估有无CD并发症、手术风险,力求在最佳时机施行最有效的手术。本期栏目介绍一则内科治疗效果欠佳,两次出现肠穿孔并接受外科急诊手术患者的诊治过程,探讨CD药物治疗策略、手术治疗指征和时机以及术后复发预防策略(D4~D5版)。
病历摘要
患者女性,24岁,反复发作腹痛5年,确诊克罗恩病(CD)2年,内科常规药物治疗效果有限,临床诱导缓解期短,炎症导致明显的肠壁解剖组织学结构破坏,两次出现肠穿孔行外科急诊手术治疗。
患者诊断及治疗过程
2008、2009年
5年前患者无明显诱因出现上腹痛,伴恶心、呕吐,无腹泻、腹胀,当地医院予抗感染、抑酸治疗后好转。
4年前患者出现腹痛、腹泻、血便。当地医院查腹部超声、CT未见异常(具体不详),胃镜示“反流性食管炎”,予口服凝血酶、抗感染等治疗后症状好转,便血停止。
2011年3月
2年前(2011年3月)腹痛再次发作,并逐渐加重。外院胃镜示“慢性浅表性胃炎”,予抑酸、抗感染等治疗,腹痛症状无改善,并逐渐出现腹泻、血便、发热,体温最高38.9℃,伴畏寒、寒战。红细胞沉降率(ESR)、结核感染T细胞酶联免疫斑点试验(T-spot)、抗核抗体(ANA)谱、结核抗体、肿瘤标志物未见异常,结核菌素试验(PPD)阴性。腹部CT:回盲部及回肠末端肠壁增厚水肿,黏膜强化。肠镜提示回盲部CD可能。3月25日开始给予甲泼尼龙30 mg,静点5天,患者症状明显好转,便血停止,发热、腹痛减轻,之后改为泼尼松口服30 mg,qd,加用美沙拉嗪。口服激素剂量逐渐减量,每周减少5 mg。
2011年4月
4月23日,患者腹痛加重,就诊于我院。实验室检查:血常规未见异常,ESR17 mm/h,结核菌抗体(TB-IgM)阳性,IgG及补体阴性,C反应蛋白(CRP)50.9 mg/L。腹部超声:回盲部肠壁轻度增厚性病变,炎症性肠病。肠镜显示(图1):回肠末端及回盲部溃疡。肠镜病理:回肠末端及回盲部小肠黏膜组织急慢性炎,伴纤维素变性、炎性渗出及肉芽组织增生。给予激素及美沙拉嗪,症状好转,出院1月后停用激素,口服美沙拉嗪维持治疗 。
2011年8月
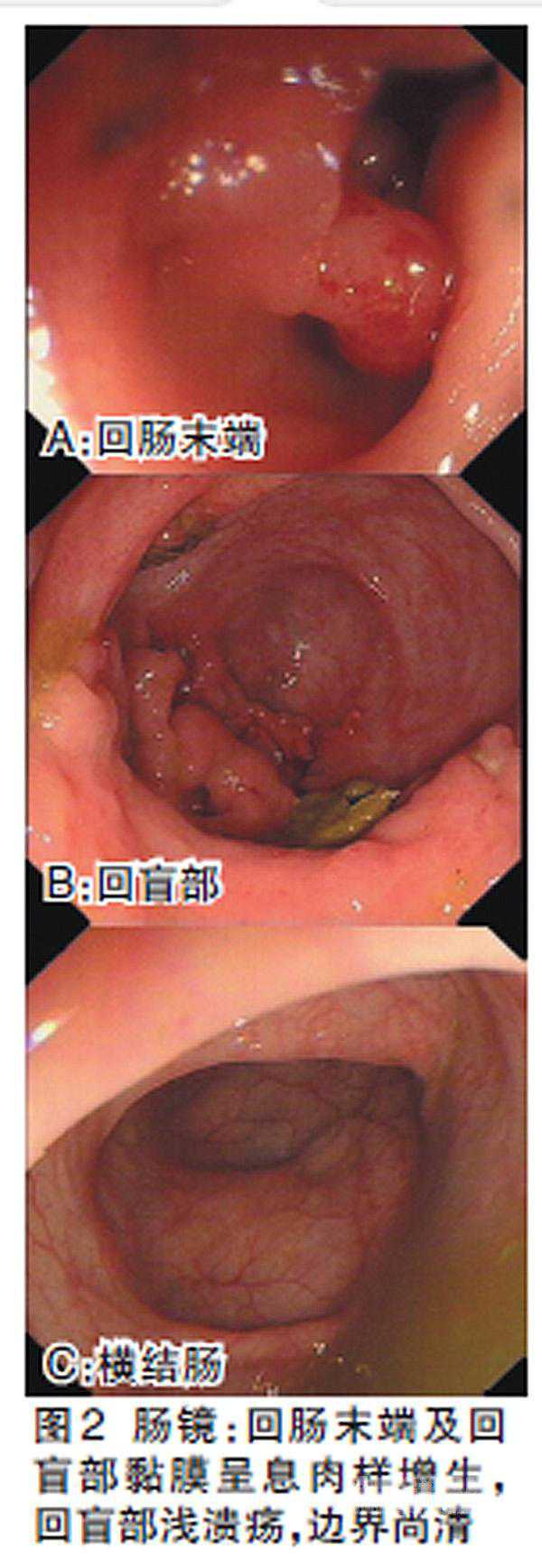
患者门诊复查:血、尿、便常规、生化全项、结核抗体、IgG、补体、血沉等均未见明显异常。肠镜示(图2):回盲部黏膜溃疡。肠镜病理:回盲部大肠黏膜固有层弥漫性急、慢性炎性细胞浸润。自诉近期内曾有左膝关节、左踝、双手近端指关节疼痛,后自行好转。
2012年1月
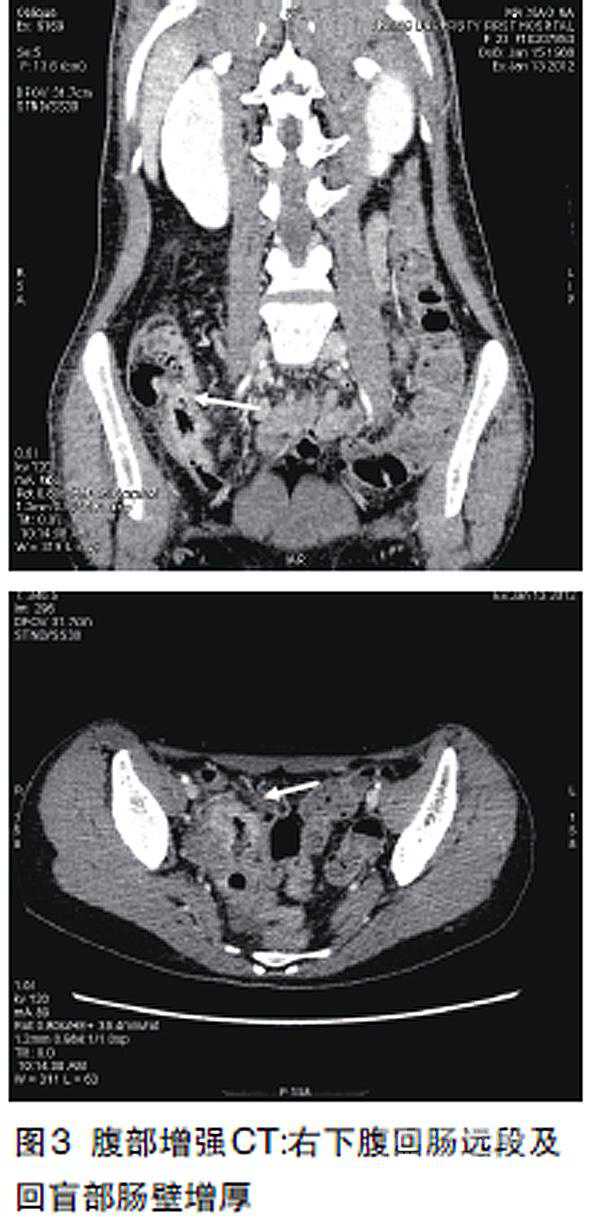
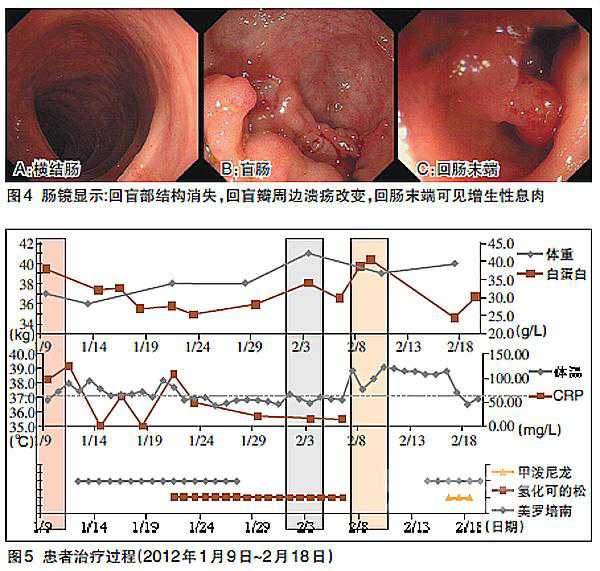
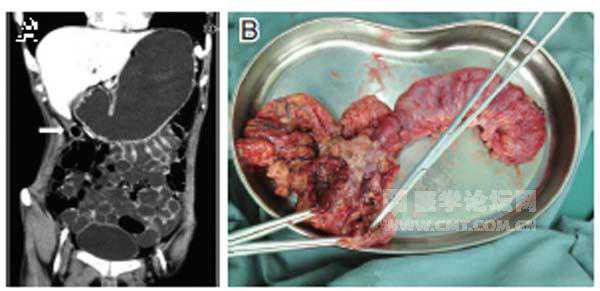
2012年1月,患者出现发热、腹痛,伴恶心、呕吐,无便血等。腹平片检查可见少量气液平。临床考虑CD合并感染及不全肠梗阻。于我院予禁食、营养、激素、抗生素、解痉止痛等治疗。腹部增强CT(图3):右下腹回肠远段及回盲部肠壁增厚及强化,结合临床考虑炎症性肠病改变。肠镜(图4)示:回盲部结构消失伴黏膜溃疡。肠镜病理:肠黏膜急慢性炎。患者入院后给予抗菌药物治疗,体温、CRP改善不明显;联合使用激素后,体温及CRP明显改善,但不全肠梗阻缓解不明显;内外科联合查房后决定手术治疗,为保证手术安全,建议先停用激素再行手术。停用激素后,患者临床症状明显恶化,复又联合应用激素及抗生素治疗(图5)。
2月18日患者全腹剧烈疼痛,腹部查体腹肌紧张,可疑板状腹。立位腹平片示:双侧膈下可见游离气体,考虑肠穿孔可能。急诊行开腹探查、粘连松解、右半结肠切除术。术中见回盲部多发穿孔,腹腔污染严重。手术标本病理组织学检查示CD。术后患者未腹痛,并接受英夫利西单抗治疗6次,治疗期间无明显临床症状。
 |
 |
2012年12月~2013年3月
2012年12月患者入院准备行第7次英夫利西单抗治疗,受凉后流涕、发热,白细胞计数升高,考虑上呼吸道感染,后出现腹痛。查C反应蛋白(CRP)17.1 mg/L。腹部CT:右中腹回结肠交界处肠管壁增厚,考虑克罗恩病(CD)复发。肠镜显示:吻合口可见深大溃疡约半个肠腔,近吻合口处直径2 cm×3 cm深溃疡。肠镜病理:肠黏膜急慢性炎。考虑不除外腹腔感染,给予抗感染治疗,并停止第7次英夫利西单抗治疗,加用美沙拉嗪。2013年1月10日患者腹痛剧烈,腹部查体可疑腹膜炎。立位腹平片未见膈下游离气体。腹部CT肠间隙可见游离气体,提示肠穿孔。急诊开腹探查:近吻合口处小肠3处穿孔,切除穿孔所在小肠及部分横结肠,术中小肠镜未见剩余肠管异常,封闭横结肠断端,末端小肠造口。患者术后恢复顺利。
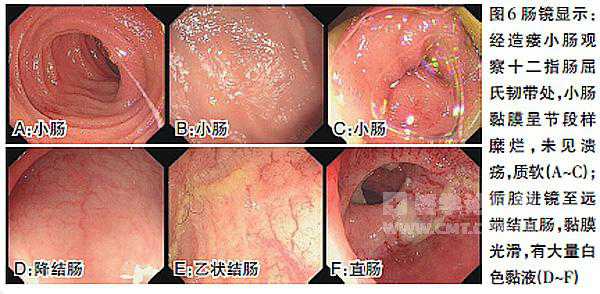
考虑患者为CD活动期,且之前使用英夫利西单抗时有过敏症状,2013年2月给予阿达木单抗。2013年3月28日复查肠镜(图6)。
分析与点评
CD好发于青年,发病高峰年龄为18~35岁。临床表现多样,消化道表现主要有腹泻和腹痛,可有血便;全身性表现主要包括体重减轻、发热、食欲不振、疲劳和贫血等。腹泻、腹痛和体重减轻是CD的常见症状,如果患者出现上述症状,特别是年轻患者,应该考虑本病的可能。
本例患者符合上述临床表现,如果医生能提高对该疾病的认识,或许可使患者在早期明确诊断和治疗方法。
活动性克罗恩病临床药物治疗策略
CD是一种消化道慢性、复发性、炎性反应性疾病。临床药物治疗主要针对炎性反应、炎性介质和炎性分子等靶点进行,其治疗目标为诱导和维持缓解,防治并发症,改善生活质量,减少手术干预。如果患者因肠道黏膜溃疡引起穿孔、瘘管或纤维瘢痕导致狭窄等并发症,则多需要接受手术治疗。因此为减少手术干预,CD患者应尽早开始正规药物治疗,降低并发症发生率。
常规药物治疗 轻度活动性CD治疗常选择氨基水杨酸类制剂:结肠型可选用柳氮磺吡啶(SASP)或其他5氨基水杨酸(5-ASA)制剂,末段回肠型和回结肠型可选用美沙拉嗪。
中度活动性CD的治疗首选糖皮质激素,激素依赖或无效时可以加用免疫抑制剂(硫唑嘌呤或甲氨蝶呤等)。生物制剂用于激素及免疫抑制剂治疗无效或激素依赖者、不能耐受治疗者,常用药物有英夫利西单抗和阿达木单抗。
重度活动性CD病情严重、手术比例及死亡率高,应及早采取积极有效措施处理。可全身应用糖皮质激素。生物制剂可在激素无效时应用,亦可在起始治疗时应用。
升阶梯和降阶梯治疗目前活动期CD治疗包括升阶梯(step up)和降阶梯(step down)两种治疗策略。
1. 升阶梯治疗策略首先采用不良反应较低的5-ASA治疗,将激素和生物制剂作为需要进一步强化治疗的后备药物。其治疗优点在于价格低廉,药物不良反应轻,而缺点是有时疗效较差,从而导致疾病进展风险高、手术干预率高、可诱发淋巴瘤等。目前国内外大多数治疗指南对于活动期CD多推荐升阶梯治疗策略。
2.在对于一些“病情难以控制(disabling disease)”的患者建议疾病早期采用降阶梯治疗,优点是治疗效果确切、黏膜愈合率高、并发症发生率低、可有效降低手术干预风险及肠道致残风险、住院时间短, 而缺点是费用高昂,容易诱发感染。
综合分析病情,应属于病情难以控制者。因此,患者在第1次穿孔后选择生物制剂,但在治疗期间出现第2次穿孔,考虑单用生物制剂效果有限,此时临床应考虑加用硫唑嘌呤类免疫抑制剂。
手术治疗指征和手术时机决策
CD治疗目前以内科治疗为主,但相当部分CD患者最终难以避免手术干预,文献报道,70%的CD患者在诊断后10年内需要接受外科手术。因此,在CD治疗过程中,需要外科医师密切配合,开展多学科综合治疗(MDT),准确评估有无CD并发症、手术的价值和风险,力求在最佳时机施行手术。
外科手术指征 ① 肠梗阻:机械性肠梗阻多由肠道纤维瘢痕导致,视病变部位和范围行肠段切除术或狭窄成形术;② 腹腔脓肿:可在B超引导下行经皮脓肿引流,必要时手术处理病变肠段;③ 瘘管形成。④急性消化道穿孔;⑤ 大出血:内科保守治疗无效、出血不止危及生命者,需急诊手术;⑥ 癌变;⑦ 内科治疗无效。
该患者穿孔前内科治疗效果不佳,有不全梗阻,每日须阿片类镇痛药控制症状,生活质量差,有外科治疗指征。患者肠道穿孔后出现急性弥漫性腹膜炎,有绝对手术指征。
手术时机选择 多数CD患者有长期使用糖皮质激素病史,病情迁延导致营养不良、合并感染,因此手术风险较大。
回顾性来看,第1次穿孔前,该患者手术时机有3个时间窗可以选择(图5),分别是刚入院、激素治疗期间以及停用激素后早期。在这3个时间窗内患者病情较平稳,手术风险相对较小。最佳手术时机应该是刚入院时,原因是此时患者未接受激素治疗;其次是激素治疗期间,此时患者营养状况改善、体温及炎性反应指标正常,但由于使用激素,手术风险升高;停用激素后早期患者症状开始反弹,但尚未进一步加重,此时手术风险较大,但相对于急诊手术,手术风险尚可接受。
然而,在患者刚入院时决定手术治疗,对临床医师的临床决策是一个很大的考验。从该病例来看,临床医师对此应有足够认识,以避免盲目治疗而贻误手术时机、增加手术风险。
CD术后复发预防策略
研究显示,CD肠切除术后3年内复发率为34%~68%,术后20年内再手术率70%。如何有效预防CD术后复发,是临床亟待解决的难题。CD术后复发可分为内镜复发和临床复发。内镜复发指无临床症状,内镜检查发现吻合口或肠管黏膜炎性改变。临床复发指出现腹痛、腹泻等临床症状, CD活动指数(CDAI)>200。CD回结肠切除术后早期复发的高危因素包括:吸烟、肛周病变、穿透性疾病(穿孔、瘘管、脓肿)、肠切除术史等。
研究证明美沙拉嗪、硫唑嘌呤类药物、咪唑类抗生素(甲硝唑)及生物制剂对预防内镜及临床复发有一定疗效,糖皮质激素对预防CD术后复发无效。甲硝唑因长期使用可导致患者出现严重并发症,故其临床应用受限。嘌呤类药物疗效略优于美沙拉嗪,但不良反应多,适用于具有术后早期复发高危因素的患者。抗肿瘤坏死因子单克隆抗体在控制CD临床症状、维持缓解和预防术后复发中发挥重要作用。
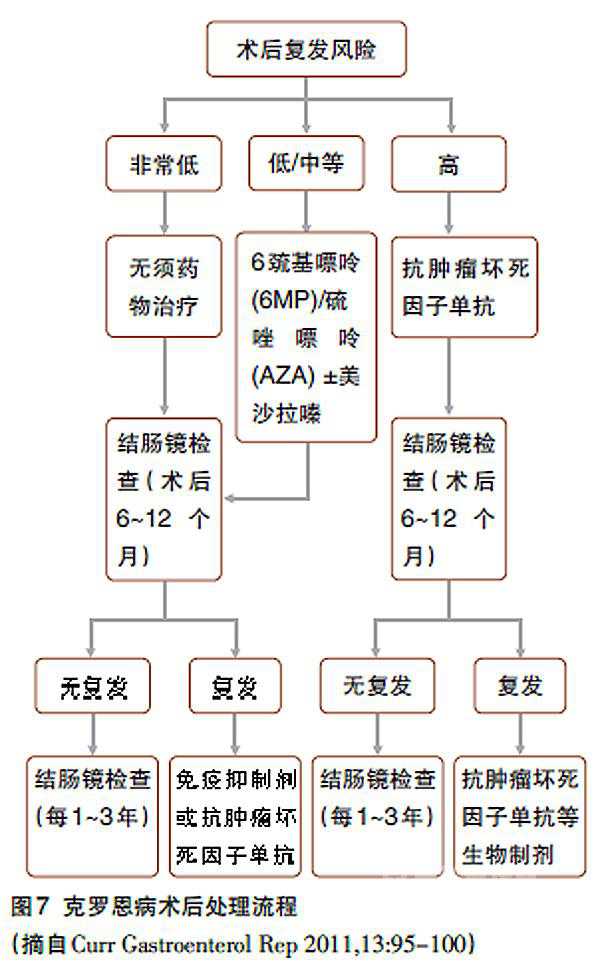
{nextpage}关于术后患者是否都要常规接受预防复发药物治疗、药物选择、治疗开始时机、治疗时间等问题,目前尚无共识,相对一致的意见是:① 对伴有术后早期复发的高危因素患者,宜尽早(术后2周)积极干预;② 术后定期复查肠镜,根据内镜复发与否以及严重程度给予或调整药物治疗方案(图7)。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








不错哦!
120
#治疗决策#
85
#决策#
99