罕见病例:这种结合胃肠息肉与脱发的疾病你了解吗?
2018-04-16 MedSci MedSci原创
Cronkhite-Canada综合征(Cronkhite-CanadaCronkhite-Canada综合征(CCS)是一种罕见的非家族性综合征,以皮肤和胃肠道上皮病变为特征, 多见于50-70岁男性. 近期我科收治1例。病例如下: 患者, 男, 66岁, 高分子化工技术人员,2月前无明显诱因下出现间断腹泻,呈黏液水样便, 每日5-6次, 无脓血便, 不伴腹痛, 口服思密达、黄连素、奥
Cronkhite-Canada综合征(Cronkhite-CanadaCronkhite-Canada综合征(CCS)是一种罕见的非家族性综合征,以皮肤和胃肠道上皮病变为特征, 多见于50-70岁男性. 近期我科收治1例。病例如下:
患者, 男, 66岁, 高分子化工技术人员,2月前无明显诱因下出现间断腹泻,呈黏液水样便, 每日5-6次, 无脓血便, 不伴腹痛, 口服思密达、黄连素、奥硝唑及静脉滴注抗生素等药物, 腹泻不能缓解, 伴毛发渐脱落、四肢掌侧色素沉着、四肢乏力、食欲差、少言懒语、消瘦(体质量下降5 kg). 入院前2 天, 因腹泻加重, 每天10-20余次, 伴恶心、呕吐, 即来我院治疗. 家族中无类似疾病史。
门诊未能确诊疾病,拟“腹泻、脱发待查”收住入院,入院后查体: 体型瘦, 营养不佳, 头发稀少, 眉毛、腋毛、阴毛完全脱落。手(趾)指甲萎缩, 凹陷; 心肺无异常, 肝脾未触及; 双下肢轻度水肿, 手掌及脚掌皮肤可见色素沉着。
辅助检查:
(1)血常规: 血红蛋白131 g/L、白细胞5.28×10^9/L、血清白蛋白29.4 g/L(34-55g/L)、血小板213×10^9/L; 血钾3.16(3.50-5.50)mmol/L、血钙1.53(2.00-2.60) mmol/L、血镁0.59(0.65-1.20)mmol/L、血清铁30.3(6.6-28.3)μmol/L、血磷0.54(0.80-1.50) mmol/L, AB型Rh阳性血;
粪便常规: 黄色稀水样, 黏液(+)、红细胞(+)、白细胞(++)、脓细胞(-)、巨噬细胞(-)、肠滴虫(-)、蛔虫卵(-)、鞭虫卵(-)、钩虫卵(-)、吸血虫卵(-)、阿米巴滋养体(-)、阿米巴包囊(-)、酵母样孢子(-)、隐血(++)。粪便培养未见沙门氏菌与志贺氏菌;
肿瘤标志物: 癌胚抗原6.0(0-3.7) μg/L、甲胎蛋白3.7(0.0-8.0) μg/L、CA153 6.76(0.00-30.00)U/mL、CA125 8.96(0.00-30.00) U/mL、CA199 15.26(0.00-19.00) U/mL;
血清免疫球蛋白及补体: 免疫球蛋白G 6.11(8.00-16.00)g/L、免疫球蛋白A 3.16(0.70-3.30) g/L、免疫球蛋白M 0.40(0.50-2.20) g/L、补体C30.34(0.80-1.60) g/L、补体C4 0.15(0.10-0.40)g/L、C反应蛋白4.53(0.00-5.00) mg/L;
肝纤维化指标: 透明质酸956.97(0-100) μg/L、Ⅲ型前胶原N端肽113.88(<120) mg/L、层粘连蛋白199.20(101.7-135.3) μg/L、Ⅳ型胶原102.18(46.5-90.5) mg/L;
自身免疫检测: 抗核抗体阴性、抗双链DNA抗体阴性、可提取的核抗原阴性。甲状腺系列游离三碘甲状腺原氨酸<1(1.5-4.1) μg/L, 游离甲状腺素、促甲状腺激素、甲状腺微粒体抗体、甲状腺球蛋白抗体均正常。生长激素0.50(0.003-0.235) nmol/L, ACTH与血皮质醇正常;
影像学检查: 腹部B超肝、胆、胰、脾、双肾未见异常; 头颅CT示脑梗塞.胃镜示食管光滑, 胃底局部充血水肿, 胃窦广泛充血水肿糜烂, 小弯侧可见息肉样隆起, 息肉表面分叶(图1);

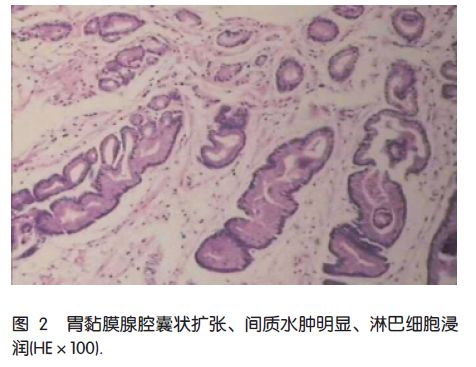
活检结果: 胃黏膜小凹变浅、胃黏液腺增生、部分腺腔囊状扩张、间质水肿明显、淋巴细胞浸润(图2);
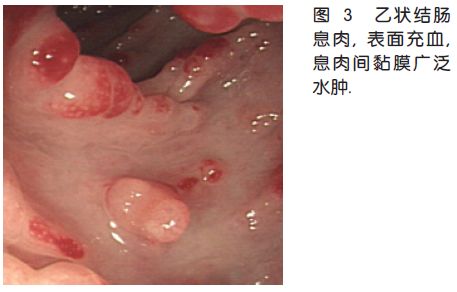
结肠镜检: 直肠至回肠末端密布0.4-1.0 cm大小不等亚蒂或扁平状息肉, 部分息肉表面充血糜烂; 息肉间黏膜广泛水肿(图3).
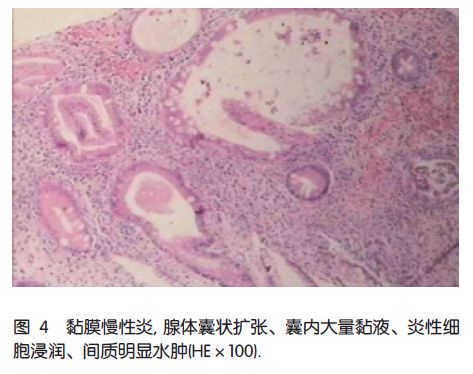
病理报告: 黏膜慢性炎, 腺体囊状扩张、囊内大量黏液、炎性细胞浸润、间质明显水肿(图4)。
根据患者检查及症状,诊断为CCS,目前疾病机理不明,尝试予奥曲肽皮下注射、结肠宁(主要药物组成: 蒲黄、丁香蓼)灌肠, 艾迪莎口服及补钾、补镁、补钙, 输入人血白蛋白治疗16天, 腹泻好转, 大便黄色成形, 每日1-2次, 电解质恢复正常出院。出院后4周死亡, 死因不详。
讨论:
CCS是一种罕见的非家族性综合征, 以皮肤和胃肠道上皮病变为特征。 皮肤病变包括脱发、指(趾)甲萎缩、色素沉着外胚层三联征。 胃肠道改变一般以错构瘤息肉为主, 黏膜广泛水肿、增生导致消化腺体分泌异常, 吸收障碍、营养不良、胃肠道出血及外科并发症。 皮肤病变和胃肠道病变可同时或相继发生。 本病1955年由Cronkhite和Canada首先报道2例, 国内通常称之为胃肠道息肉-色素沉着-秃发-指(趾)甲萎缩综合征, 目前国外文献报道超过400多例, 胃肠道息肉恶变发生率在10%左右。 小儿很少报道,有75%为日裔人种。 1985年国内首次报道本病, 至2009-06共报道病例42例。 曹晓沧等分析了35例中国人CCS临床特点, 发现患者以胃肠道多发息肉伴外胚层三联征为主要表现, 慢性腹泻、腹痛、体质量下降、贫血、水肿等症状最为常见, 2例患者合并癌变。 中国人病例发病年龄多为50-70岁, 男女之比为1.3-2.3。 本例患者以慢性腹泻为主。 而国外文献报道首发症状以味觉减退和腹泻为多。 贾岩等分析了33例中国人CCS, 根据内镜检查及消化系造影见息肉累及除食管外的全消化系, 分布以胃和大肠为多; 直径0.1-3.0 cm不等; 单发或多发、有蒂或无蒂、形态不一。 息肉病理组织学分类包括炎症性、增生性、腺瘤性和错构瘤性息肉; 8例息肉癌变。 实验室检查示不同程度的低蛋白血症、少数患者免疫球蛋白下降、甲状腺功能减退。治疗方法除一般治疗、营养支持治疗以外, 目前对CCS的治疗主要包括激素、内镜下治疗及外科手术治疗。 患者常因肠吸收不良引起电解质紊乱、维生素缺乏、低蛋白血症, 最终因营养不良、贫血、感染、全身衰竭等死亡, 本病预后不良。 本例患者死亡原因可能为全身衰竭。
CCS主要依据临床症状体征结合内镜检查综合诊断, 目前内镜检查是确诊CCS的主要手段, 临床上CCS主要与Peutz-Jeghers综合征、幼年性息肉(juvenile polyposis syndrome)、家族性结肠息肉病、Gardner综合征、Turcot综合征等肠道息肉病和Menetrier病鉴别。 现在仍没有统一的临床分型, 日本学者[8]根据初发症状和体征,将其分为5型: Ⅰ型: 腹泻型(35%); Ⅱ型: 味觉减退型(40.9%); Ⅲ型: 口腔干燥型(6.4%); Ⅳ型: 腹部不适型(9.1%); Ⅴ型: 毛发脱落(8.2%)。 本例患者为腹泻型。
CCS病因尚不十分清楚, 有研究表明CCS患者存在高滴度抗核抗体和IgG4水平升高, 并同甲状腺机能减退和自身免疫性疾病相关。 因此, CCS病因可能与自身免疫异常有关。 也有研究认为可能与感染、过度劳累有关。


本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#罕见病例#
86
#胃肠息肉#
73
能治疗么
89
学习了
100
#罕见#
66
学习学习学习
99
罕見病例!记住了!谢!
96
学习了
90