Cardiovasc Res:谢峻团队揭示心-肠交互调控对心梗后再灌注损伤严重程度的调控机制
2024-05-12 论道心血管 论道心血管 发表于威斯康星
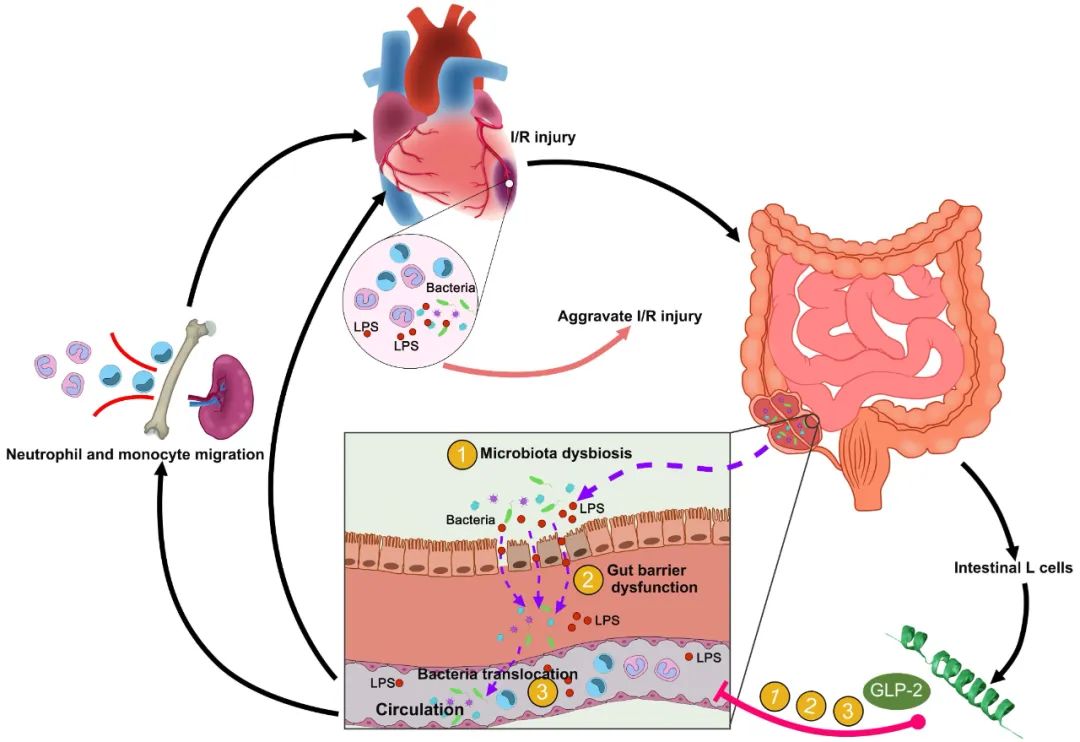
首次揭示了心脏-肠道-微生物群-免疫轴的双向调控在心肌缺血再灌注后炎症风暴中的重要作用,为日后开发针对菌群移位的AMI靶向治疗策略提供了新思路。
急性心肌梗死(AMI)是常见的心血管急危重症之一,具有较高的致残率和致死率。急性心肌梗死后的再灌注(I/R)损伤是目前心梗治疗的痛点和难点。大量证据表明,心肌缺血再灌注后炎症反应的过度激活是患者预后不良的重要原因。尽管对于心肌缺血再灌注后炎症反应激活和消散的规律和机制已有了一定的了解,但何种原因导致心肌炎症反应的过度激活仍亟待进一步深入研究。肠道作为人体最大的免疫器官,在控制局部和全身免疫方面扮演着重要角色。近年来肠道微生物在心血管疾病和代谢紊乱中的作用逐渐引起关注,相继有研究指出心肌梗死后存在肠道菌群结构的紊乱及比例的失衡。然而,在心肌缺血再灌注的病程中,肠道与心脏间是否存在交互调控进而影响炎症反应的激活和消散最终影响再灌注损伤的严重程度尚不清楚。
2023年5月13日,安徽医科大学第一附属医院谢峻教授团队在Cardiovascular Research杂志上在线发表了题为“Heart-gut microbiota communication determines the severity of cardiac injury after myocardial ischaemia/reperfusion”的研究论文,首次揭示了心脏-肠道-微生物群-免疫轴的双向调控在心肌缺血再灌注后炎症风暴中的重要作用,为日后开发针对菌群移位的AMI靶向治疗策略提供了新思路。

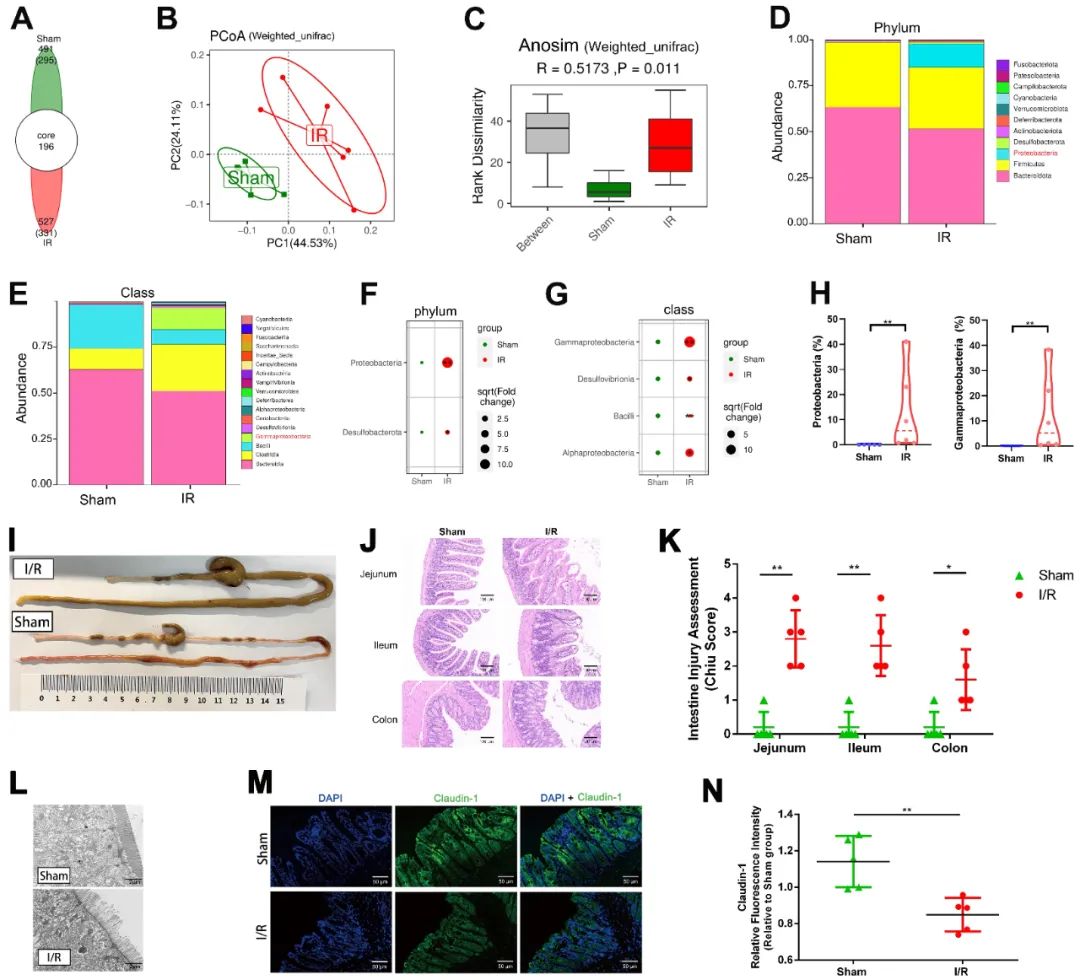
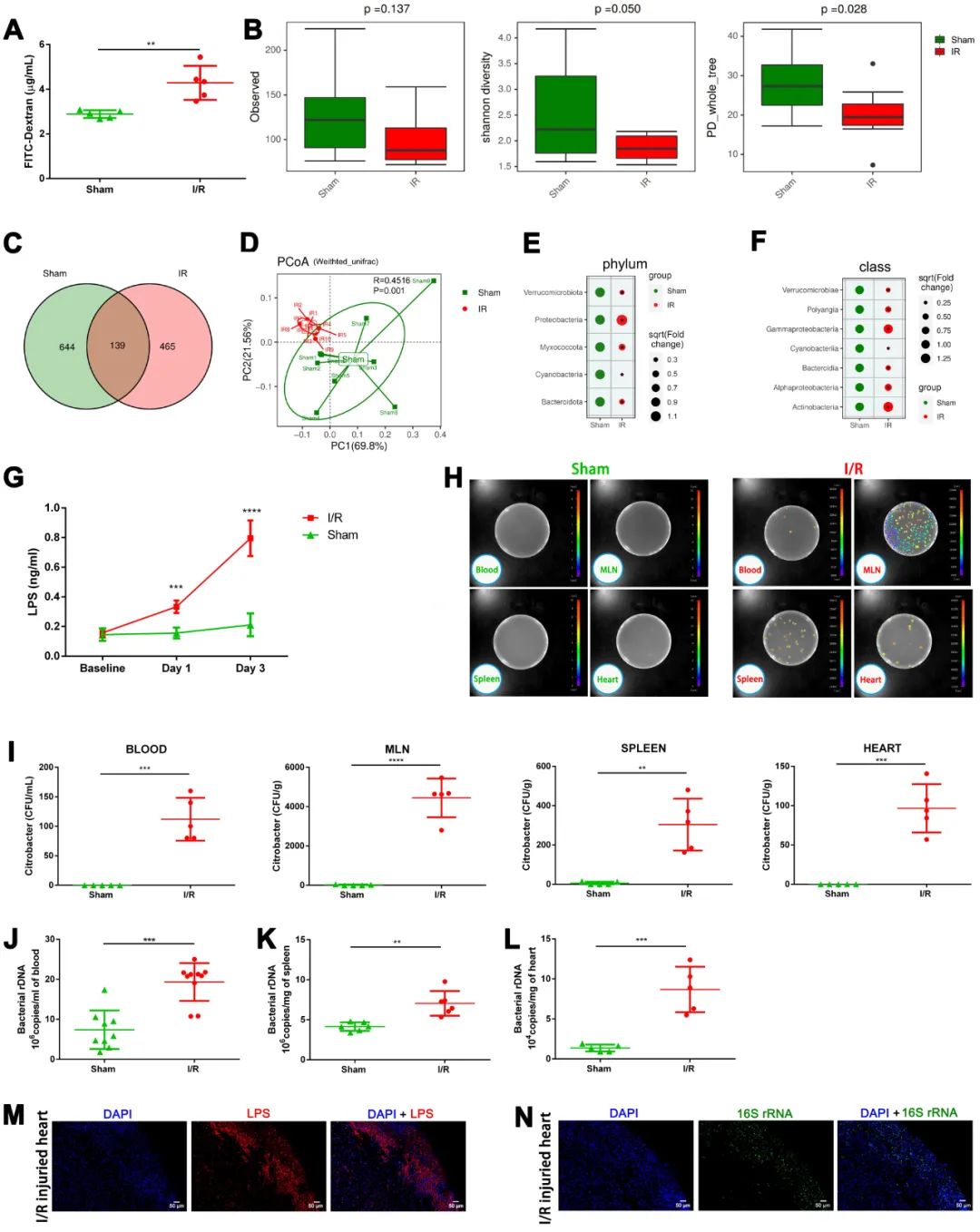
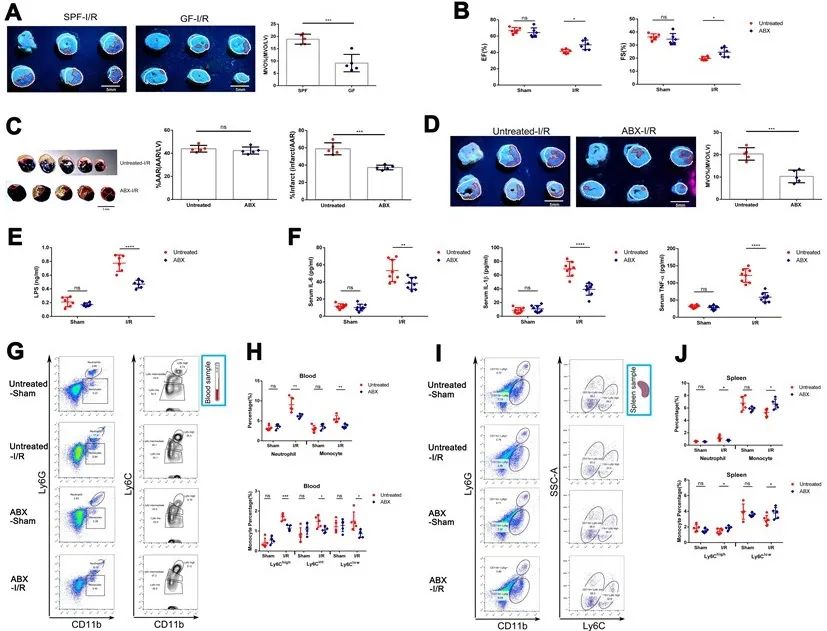
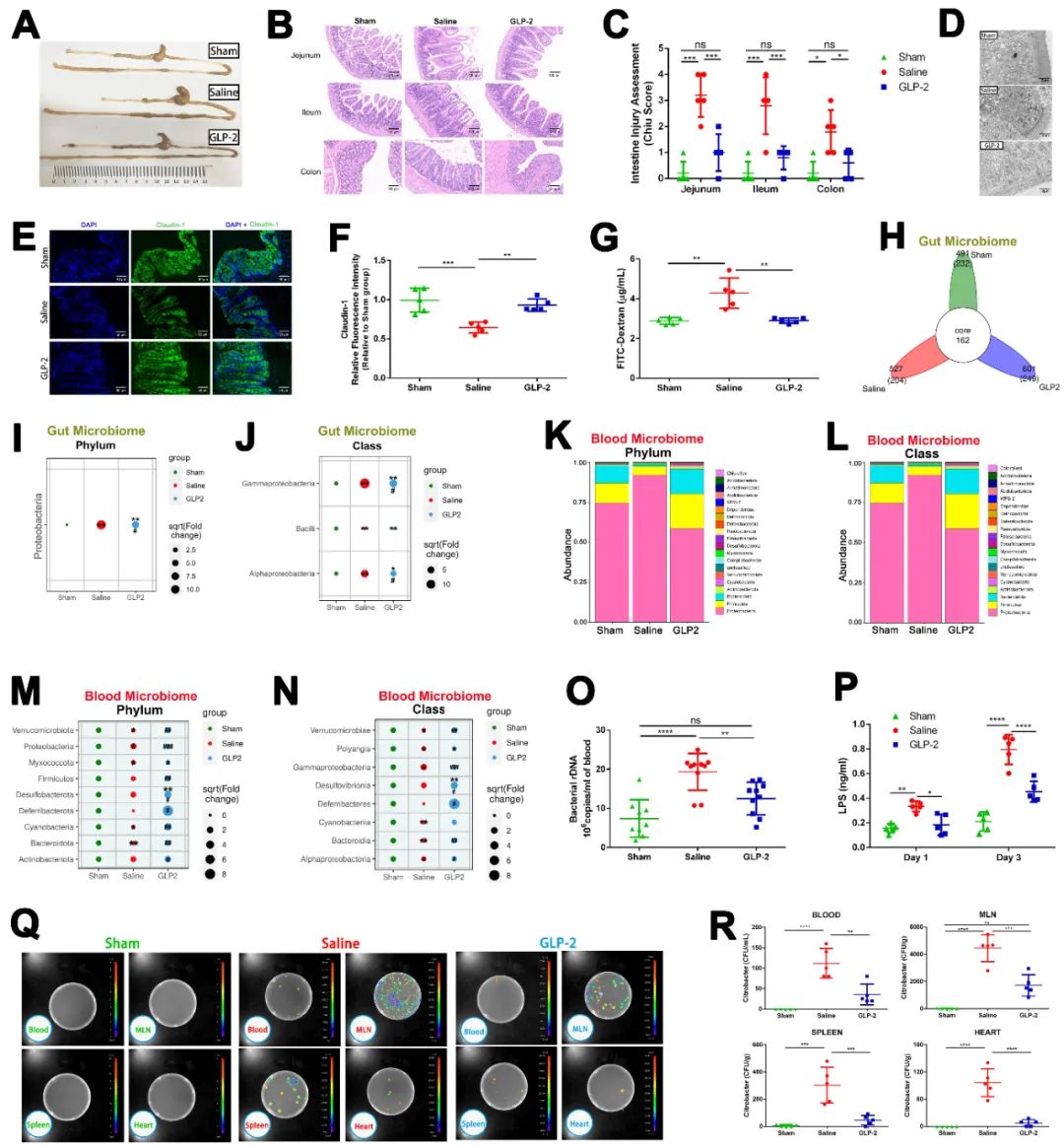
首先,作者通过一项急性ST段抬高型心梗(STEMI)的队列研究以探讨STEMI患者肠道细菌移位产物与炎症标志物和I/R损伤严重程度的关系,结果发现STEMI患者肠道菌群移位的标志物循环LPS水平、循环细菌DNA载量与炎症过度激活和I/R损伤的严重程度密切相关,且是心梗血运重建后微循环障碍(MVO)的独立危险因素。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#心肌梗死#
26