姜黄素抗AD老生常谈?它的衍生物效果更佳!
2023-02-07 brainnew神内神外 brainnew神内神外 发表于安徽省
自噬-溶酶体途径是降解和回收细胞成分的高效方法,包括有毒蛋白的聚集体和受损的细胞器。
自噬-溶酶体途径是降解和回收细胞成分的高效方法,包括有毒蛋白的聚集体和受损的细胞器。2020年2月,香港浸会大学Min Li团队在Aging Cell上发表了一篇发现一种新的TFEB(靶向转录因子EB)激活剂姜黄素类似物C1,且有望成为预防或治疗AD药物的文章。文章认为TFEB是自噬溶酶体途径重要的调节剂,而姜黄素类似物C1可直接结合并激活TFEB,增强自噬和溶酶体活性,减少APP、APP C末端片段、Aβ和tau聚集体,从而改善突触和认知功能。
 1C1激活TFEB,促进磷酸化tau聚集体的降解,改善P301S小鼠运动功能
1C1激活TFEB,促进磷酸化tau聚集体的降解,改善P301S小鼠运动功能
作者首先发现,经过C1处理的P301S鼠模运动能力改变,由此检测鼠脑p-tau、总tau等水平,结果表明C1主要减少鼠模脑中不溶性tau聚集体。进而从分子水平探究其作用机制,结果表明C1处理可激活TFEB并促进鼠模大脑自噬和溶酶体的发生,而不抑制MTOR途径。
2C1激活TFEB,降解APP/Aβ,改善5xFAD鼠模的突触和认知功能
经C1处理的鼠模全长APP、CTF-α和Aβ水平下降,TFEB活化,自噬增加,且没有性别差异。同时,作者比对了姜黄素和C1的作用,发现C1在TFEB介导自噬和溶酶体影响时活性优于姜黄素。以上结果表明,C1通过促进鼠模脑内TFEB介导的自噬和溶酶体生物发生而促进APP片段的降解并降低Aβ,改善突触和认知功能。
3C1减弱APP和tau病理,改善3xTg-AD鼠模认知功能
研究进一步探索C1对鼠模的神经保护作用。实验表明,经过C1处理的鼠模在旷场实验、Morris水迷宫实验、空间探索实验显示出优势,且同时确定APP、tau、TFEB和自噬分子变化。结果表明,C1通过促进TFEB介导的自噬和溶酶体生物发生,有效促进APP片段化、Aβ和磷酸化tau聚集体的降解,产生神经保护作用。
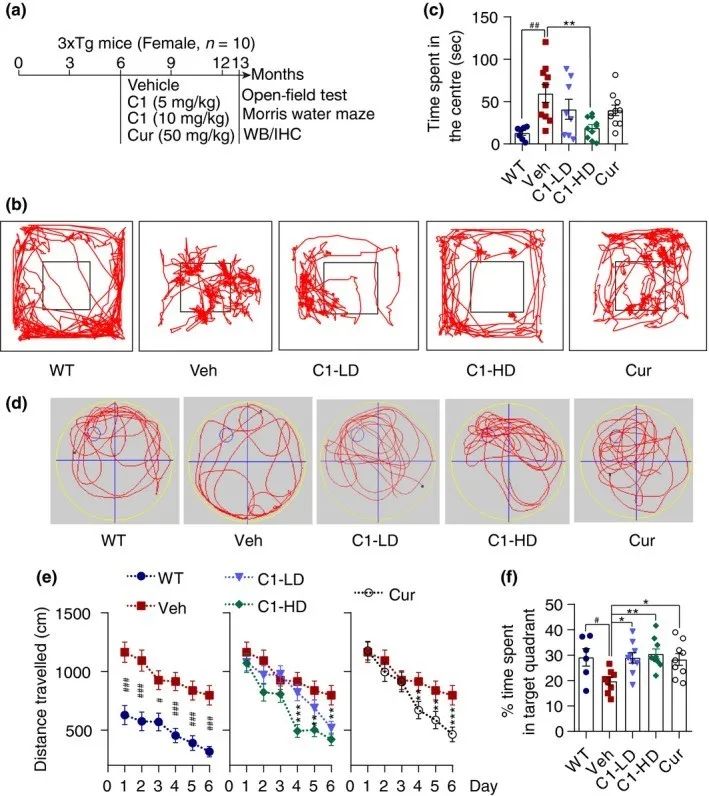
图1. C1改善3xTg-AD鼠模的认知功能
4体外实验表明C1通过TFEB降解APP和MAPT/tau
体外实验进一步验证C1的抗AD功效主要由TFEB介导。在过表达APP695的N2a细胞中,C1促进了TFEB的核易位和降低FI-APP、CTF-β。在表达P301L-tau的N2a细胞中,C1降低了总tau,此作用被溶酶体和TFEB抑制。这些结果表明,C1通过TFEB激活促进APP/CTF-β和tau的溶酶体降解。
越来越多的证据表明自噬溶酶体通路(ALP)的缺陷是AD发病的早期机理,ALP的逐步破坏可导致神经元中APP代谢物和tau聚集物的大量积聚,因此TFEB靶向调节ALP是开发治疗神经退行性疾病如AD的一种新型方法。该研究系统评估了C1在AD动物模型中的神经保护作用,且证明C1可通过TFEB促进自噬和溶酶体活性,从而减弱Aβ和tau,预防AD的记忆障碍。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言