Leukemia:大B细胞淋巴瘤CD19-CAR-T治疗失败后的一线治疗及结局
2022-11-13 聊聊血液 网络
CD19-CAR-T改变了复发/难治性大B细胞瘤淋巴瘤(r/r LBCL)的治疗格局,达到前所未有的70%高缓解率,然而仍有60%的患者会在CD19-CAR-T治疗后最终复发或进展。
CD19-CAR-T
CD19-CAR-T改变了复发/难治性大B细胞瘤淋巴瘤(r/r LBCL)的治疗格局,达到前所未有的70%高缓解率,然而仍有60%的患者会在CD19-CAR-T治疗后最终复发或进展。在这种情况下,Polatuzumab、tafasitamab、塞利尼索和 loncastuximab 已获得 FDA 批准,而免疫检查点抑制剂、来那度胺、双特异性抗体、研究性 CAR-T 产品和异基因造血细胞移植以及挽救性化疗则是额外的选择。
但问题在于,目前还不清楚CAR-T 暴露后应该如何利用上述治疗手段。有小样本研究报告了治疗 CAR-T 细胞治疗后复发的经验,但治疗策略各不相同。
为了报告 CD19-CAR-T 治疗后复发或进展的 LBCL 患者的特征和结局、分析CAR-T 治疗后一线干预的缓解和总生存期,识别不良结局的风险因素,并开发 CAR-T 治疗后接受治疗患者的死亡风险分层模型,纪念斯隆凯特琳癌症中心Miguel-Angel Perales和Roni Shouval教授等开展了一项回顾性观察性分析,共纳入两家中心305例CD19-CAR-T 治疗的LBCL患者,其中182例疾病复发或进展,135例接受了后续抗癌治疗。研究结果近日发表于《Leukemia》。

研究设计
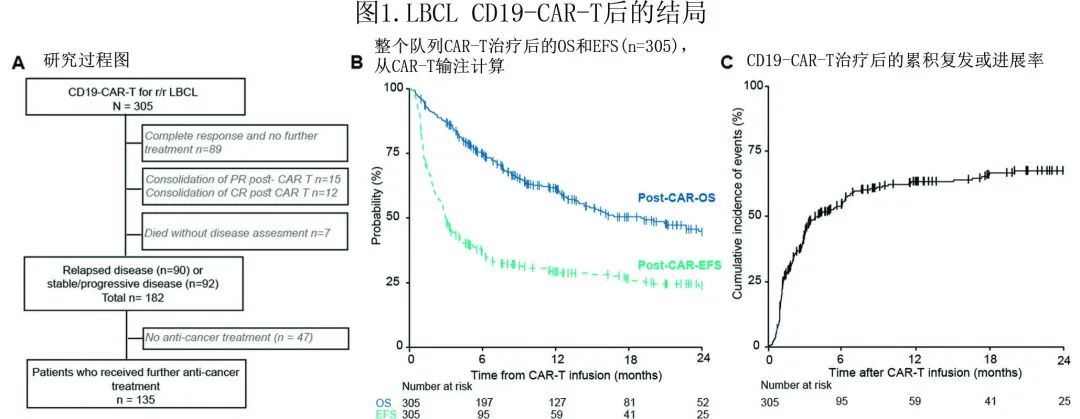
作者回顾性分析纳入了2016年4月至2021年5月期间在纪念斯隆凯特琳癌症中心(MSKCC)和Sheba医学中心(以色列)接受CD19 CAR-T细胞治疗的成人(年龄≥18岁)r/r LBCL患者(图1A),CD19-CAR-T 产品包括:axicabtagene ciloleucel (axi-cel)、tisagenlecleucel (tisa-cel)、lisocabtagene maraleucel (liso-cel)或POC CD28 为基础的产品 (NCT02772198)。
研究结果
患者特征及结局
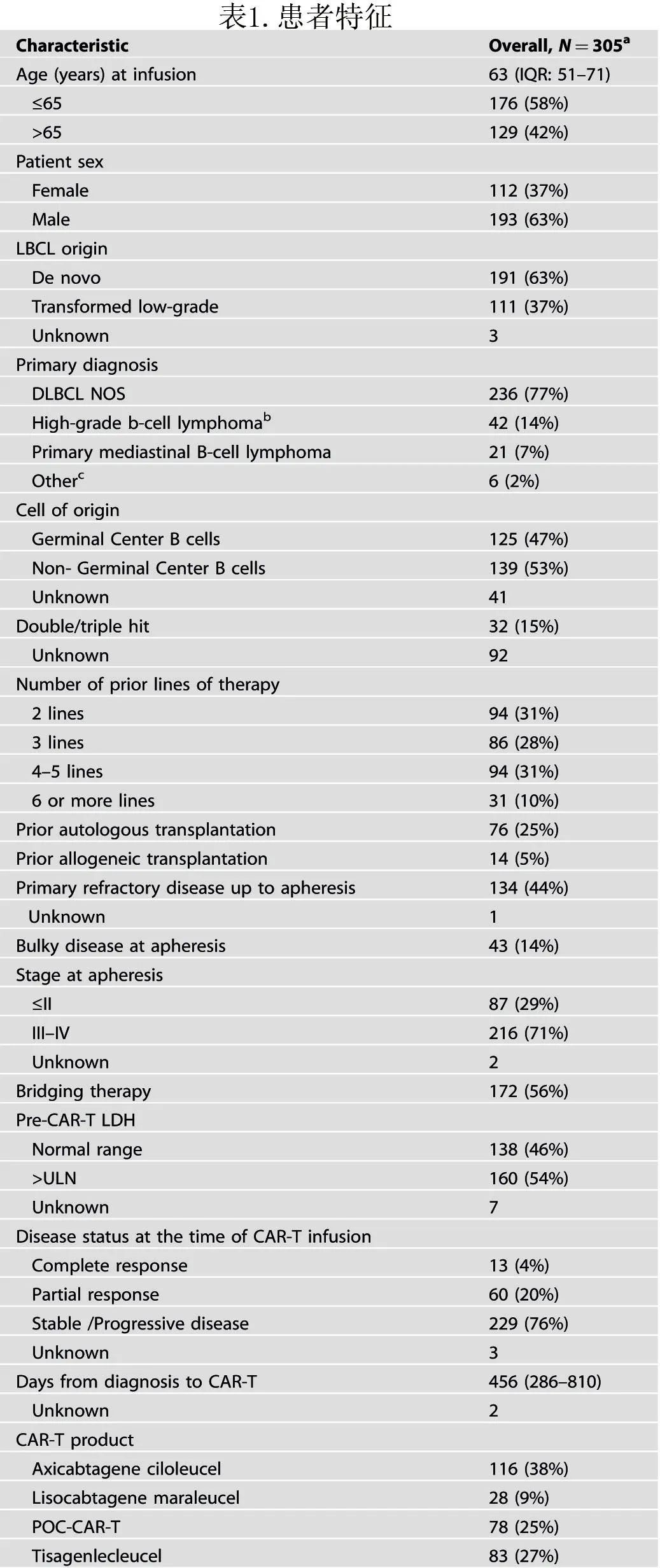
两家中心共有305例患者(表1)接受了 CD19-CAR-T 治疗 (axi-cel [n= 116,38%];tisa-cel [n= 83,27%];lisocel [n= 28,9%];POC-CAR-T [n= 78,26%]),中位年龄为63岁,LBCL 的主要组织学亚型为弥漫性大 B 细胞淋巴瘤非特指型 (n= 236,77%)。大多数 (211,69%) 既往接受过≥3线治疗,125例患者 (41%) 接受> 3线线治疗,大多数为III–IV期 (216,71%),分别有134例 (44%) 和43例 (14%) 患有原发性难治性疾病和大包块肿瘤(存在任何单个直径> 10 cm的包块)。
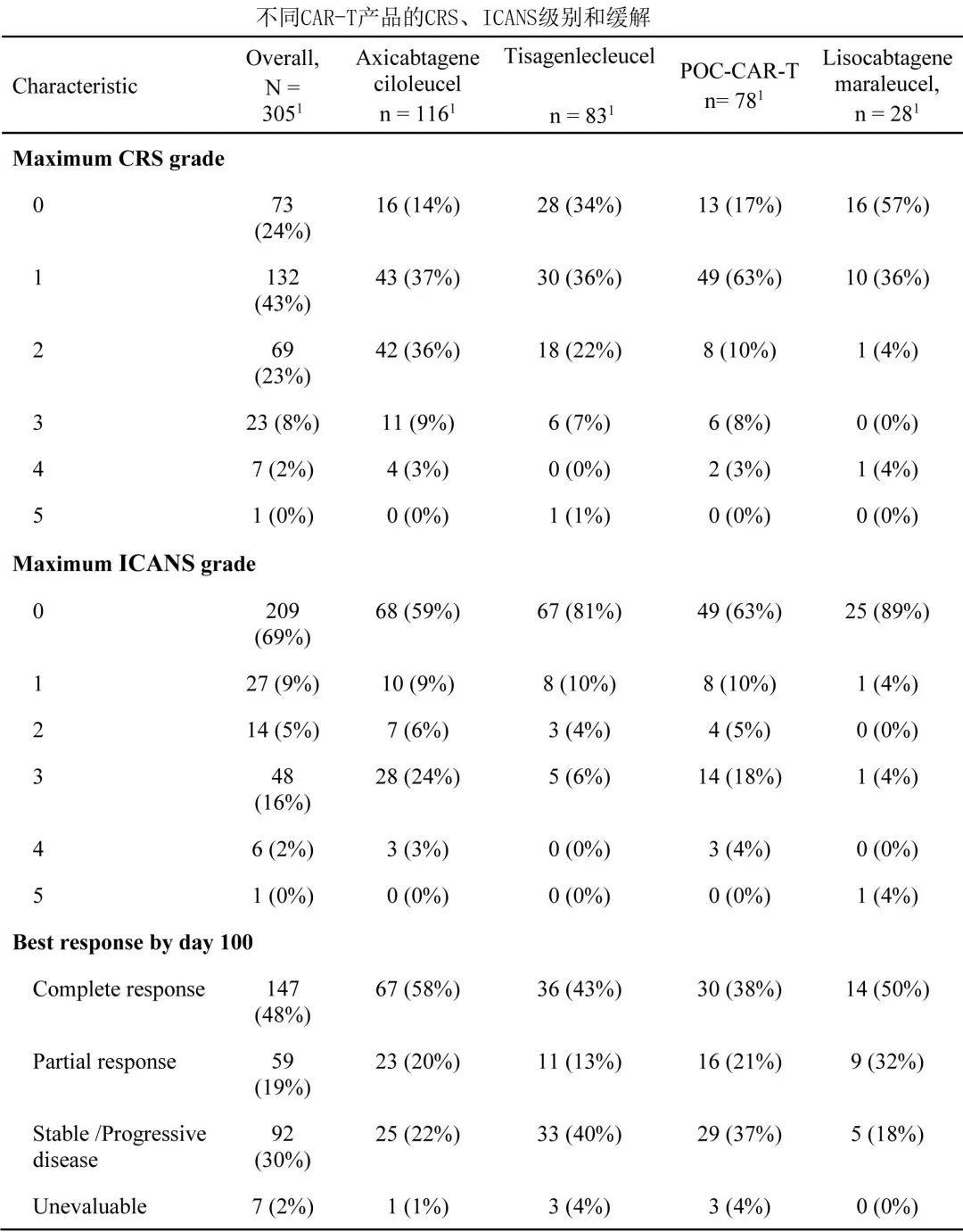
分别有76%和32%的患者发生任何级别的 CRS 和ICANS, 33%和23%为重度(≥2级)CRS和ICANS。大多数患者对 CAR-T 治疗有反应(最佳ORR为67%,其中48% CR、19% PR)。CAR-T 产品特异性毒性和缓解见下表。
中位随访20个月,CAR-T后1年OS和EFS率分别为62%和29%(图1B),1年累积复发或进展率为63%(图1C)。
CAR-T后EFS的预测因素
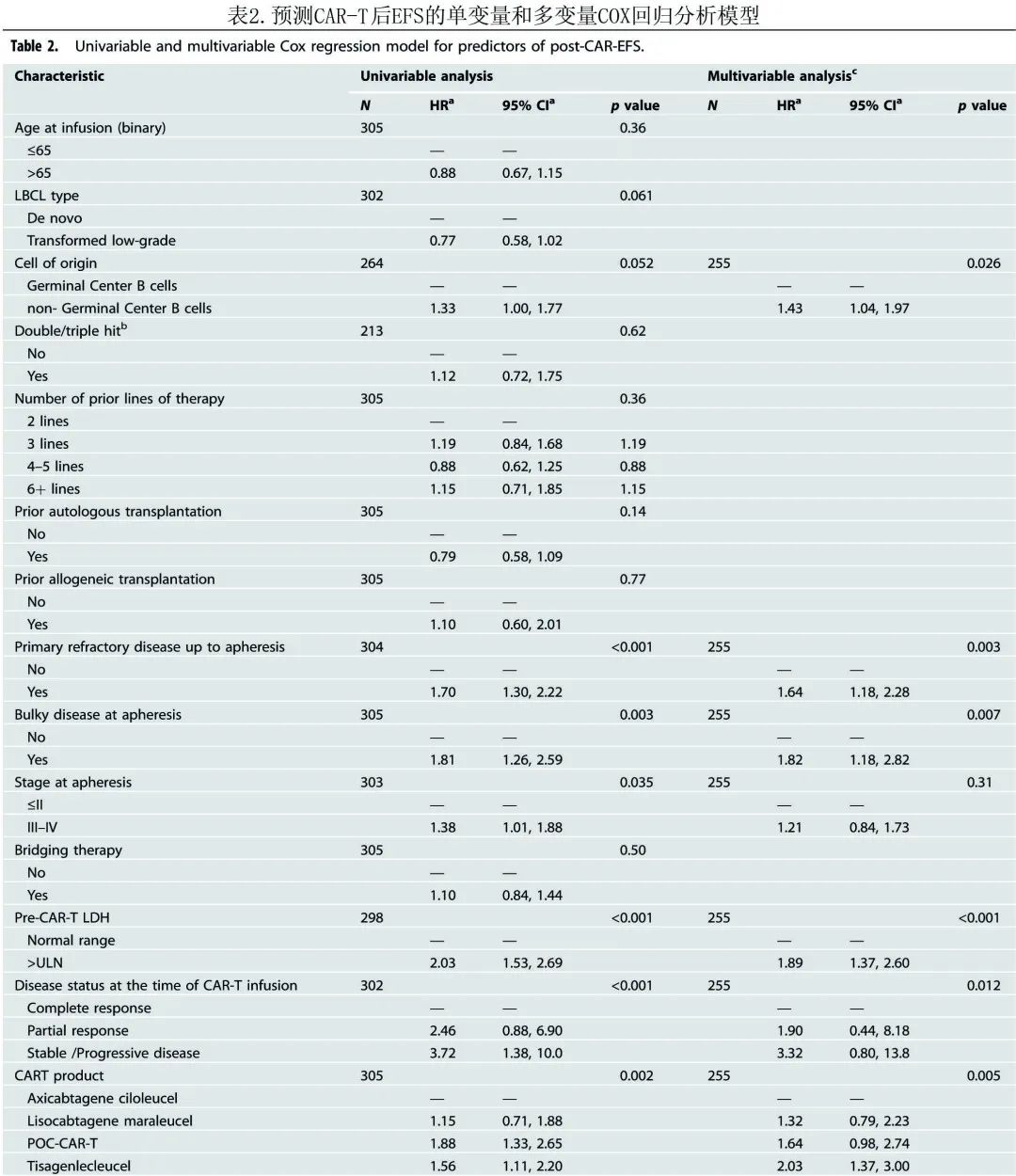
作者在单变量分析中筛选了候选预测因素。将符合P<0.1显著性标准的受试者引入多变量 Cox 回归模型(表2)。结果发现,非生发中心淋巴瘤(HR= 1.43;P= 0.026)、单采前原发难治性疾病 (HR= 1.64;P= 0.003)、CAR-T前 LDH 升高 (HR= 1.89;P< 0.001)、CAR-T 输注时存在活动性疾病(相对于完全代谢缓解,PR HR= 1.90,SD/PD HR= 3.32;总体P= 0.012)是EFS的负面影响因素;除这些传统风险因素外,Tisa-cel的治疗失败风险也高于axi-cel (HR= 2.03;P= 0.005)。
CAR-T治疗失败时的疾病特征
在182例 CAR-T 后疾病复发或持续的患者中,51%的患者为 CAR-T 难治性疾病,49%的患者最初对 CAR-T 有反应但随后复发。77例患者进行了组织活检以确认疾病持续或复发。由于抗原逃逸是 CAR-T 耐药的潜在机制,作者评估了52例肿瘤活检组织中的 CD19 表达。有趣的是,CD19表达(图2A)仅在3/52(6%) 中缺失,而其余样本为dim (14/52,27%) 或正常 (35/52,67%) 表达。
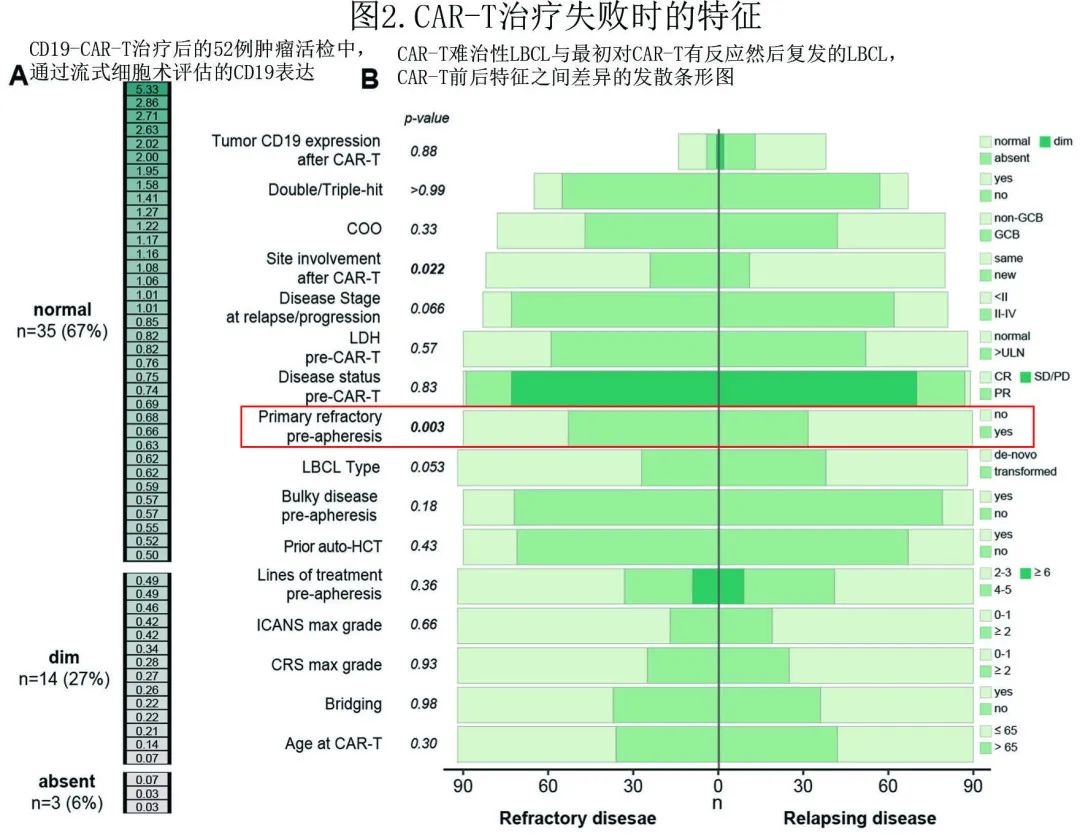
作者比较了 CAR-T 后难治患者与复发患者的基线特征,以确定可能与 CAR-T 治疗失败类型相关的特征(图2B)。结果发现单采前的原发难治性疾病是各组之间唯一不同的CAR-T前因素:CAR-T难治性人群中的百分比更高 (58% vs. 36%,P= 0.003,见图2B红框)。
为进一步明确这两种疾病(难治VS复发)对 CAR-T 反应模式之间的差异,作者研究了 CAR-T 输注后的额外变量。与复发组相比,难治性组患者在疾病评估时更容易出现新的疾病累及部位 (14% vs. 30%,P= 0.017)。CAR-T耐药患者在疾病进展时的 CD19 表达与疾病复发患者相似,无论考虑表达类别(缺失/dim/正常;P= 0.88)还是 MFI 比值(相对于参考值)作为连续协变量 (P= 0.60)。总的来说,本研究结果表明,疾病耐药和复发都是 CAR-T 治疗失败的常见模式,需要更好的生物标志物来描述它们之间的生物学差异。
CAR-T治疗失败后的治疗
CAR-T 后复发或稳定/进展的182例患者中,135例患者 (74%;图1A) 在 CAR-T 输注后接受后续抗癌治疗,CAR-T 输注后中位时间为83天。大多数患者 (75/135,56%) 是在 CAR-T 缓解(CR 32%,PR 24%)后因疾病复发接受治疗;其余患者 (60/135,44%) 则是因 CAR-T 未缓解接受治疗。
在 CAR-T 治疗失败后接受进一步治疗的患者中,总缓解率为39% (CR 20%;PR 19%)。CAR-T后疾病进展或稳定的患者从 CAR-T 至下一线治疗的中位时间短于最初缓解然后复发的患者(50天 vs. 123天,p< 0.001)。从CAR-T 后一线治疗开始的中位随访时间为15个月,治疗后中位OS 和EFS分别为8.5个月和1.9个月(图3A),这些不良结果强调了迫切需要改善 CAR-T 后需要抗癌治疗的患者的治疗现状。
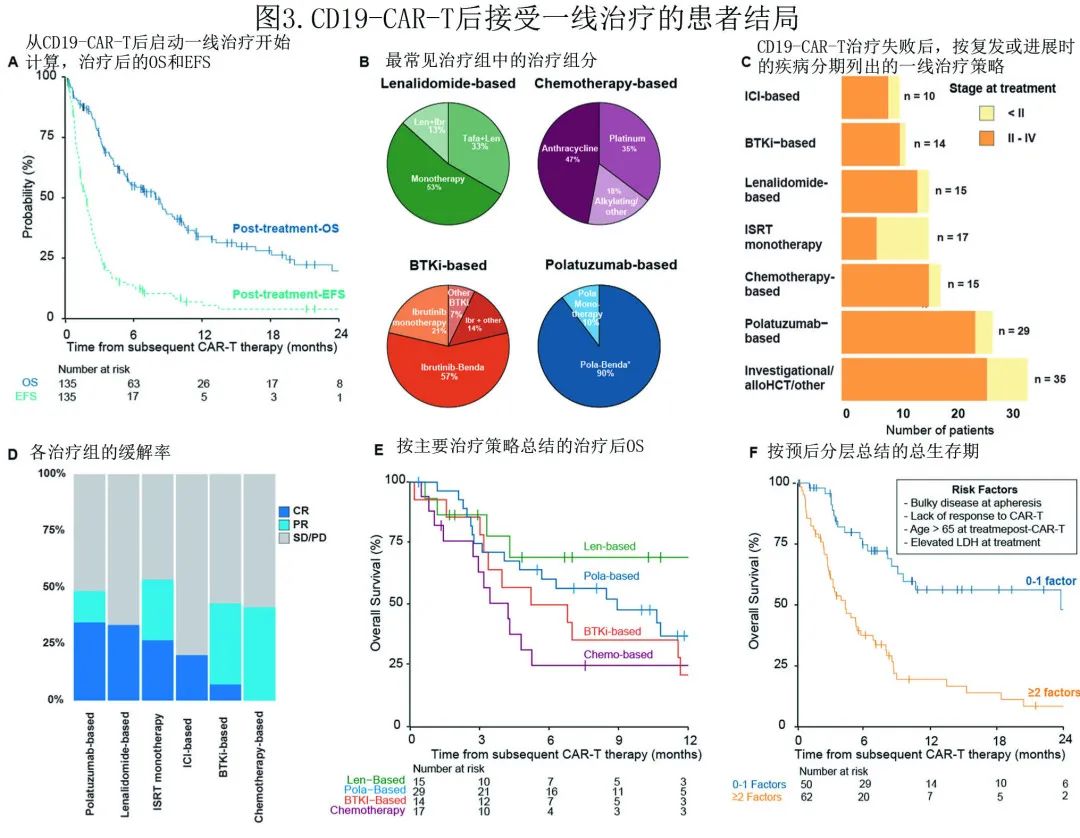
CAR-T 后的一线治疗采用了多达30多种不同的治疗策略,按主要药物类别或药物对治疗进行的分组见下表。

主要治疗类别(图3B)包括polatuzumab为基础(n= 29)、化疗(n= 17;蒽环类药物或铂类为基础)、来那度胺为基础(n= 15)、受累部位放疗 (ISRT) 单独治疗 (n= 15) 和BTK抑制剂为基础 (BTKi;n= 14)。治疗分配由治疗医生自行决定,并因研究中心而异;局部疾病主要给予单独ISRT(图3C)。
不同治疗策略的患者特征存在有意义的差异:化疗组更侵袭性疾病特征更多,如大包块疾病、单采前原发难治性疾病和对 CAR-T 的缓解率较低;与其他治疗组相比,接受来那度胺治疗的患者年龄更大、治疗线更多,同时 CAR-T 缓解更佳、治疗前 LDH 更低(即CAR-T后治疗的给药前);接受 polatuzumab 和BTKi 为基础策略的患者通常年龄<60岁,其中超过70%的患者治疗前 LDH 升高。全身治疗的 CR 率从化疗的0%到以来那度胺和 polatuzumab 为基础的30%以上(图3D)。
最常见的全身治疗策略治疗后的一年生存率范围,介于 BTKi 的 21%、化疗的 25%至来那度胺为基础治疗的69%(图3E)。Polatuzumab 为基础的策略可实现48%的ORR (CR n= 10/29[34%],PR n= 4/29[14%]),但缓解未转化为治疗后1年 OS 延长 (37%)。考虑到治疗后 OS 率的差异,作者进行了探索性分析以对比主要的治疗策略。在按中心分层并校正治疗选择的潜在驱动因素(包括年龄、治疗时 LDH 和既往 CAR-T 应答)的多变量 Cox 回归模型中,与标准化疗相比,来那度胺为基础的治疗与治疗后 OS 改善相关 (HR= 0.25,P= 0.027)。表明新药可在 CAR-T 治疗失败后诱导缓解。
CAR-T后的风险分层系统
鉴于 CAR-T 治疗失败后一线治疗后的结局较差,作者试图确定此时死亡率的关键预测因素,在单变量和多变量 Cox 回归模型中研究了疾病、患者和治疗相关特征与治疗后 OS 之间的相关性。在单变量分析中,高龄(> 65岁)、单采时病变体积较大、治疗前 LDH 升高、CAR-T至治疗之间的时间较短(<100天)、治疗时疾病分期较晚和 CAR-T 难治是治疗后 OS 较短的候选预测因素(表3)。

CAR-T失败后一线治疗OS的多变量 Cox 模型(包括候选预测因素)证实了大包块疾病 (HR= 2.27)、年龄较大 (HR= 2.65)、LDH升高 (HR= 2.95) 和 CAR-T 难治(HR= 2.33)的独立相关性。为了对这些患者的死亡风险进行分层,作者提出了包括这4个因素(单采前大包块疾病、CAR-T难治、年龄> 65岁和治疗前LDH)的预后系统,分为0-1个因素与≥2个因素,1年生存率分别为56%和19%(图3F)。
结论
本研究通过305例接受CD19-CAR-T治疗的LBCL患者中, 182例疾病进展/复发患者的数据,填补了与 CAR-T 治疗失败患者结局和后续治疗相关的知识缺口。本研究也反映了 CAR-T 后淋巴瘤持续存在的令人沮丧的后果,并强调了仍存在的未满足需求。尽管如此,新药在 CART 暴露后仍可显示出活性,值得进一步探索。最后,作者提出了一种预后工具来识别 CAR-T 后早期死亡风险最高的患者,可能有助于对患者进行分层,以便未来在 CAR-T 后中进行研究。
参考文献
Tomas AA,et al.Outcomes of first therapy after CD19-CAR-T treatment failure in large B-cell lymphoma.Leukemia . 2022 Nov 5. doi: 10.1038/s41375-022-01739-2.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







