STTT | 特瑞普利单抗联合化疗一线治疗晚期非小细胞肺癌:最终总生存期分析及生物标志物探索
2024-12-27 daikun MedSci原创 发表于陕西省
该研究评估了PD-1单抗特瑞普利单抗联合化疗在未经治疗的晚期NSCLC患者中的疗效和安全性,特瑞普利单抗联合化疗作为晚期NSCLC的一线治疗方案,显著改善了OS,尤其是在非鳞状NSCLC亚组中。
非小细胞肺癌(NSCLC)是全球癌症死亡的主要原因,免疫治疗和化疗的组合为晚期NSCLC的治疗带来了革命性的进展,PD-1/PD-L1抑制剂联合化疗已被证明可以显著改善NSCLC患者的无进展生存期(PFS),并逐渐应用于一线治疗。然而,除了Keynote 189和407研究外,大多数比较化疗和ICIs联合治疗晚期NSCLC的III期临床试验都将总生存期(OS)作为次要终点,缺乏长期生存数据的全面分析。此外,尽管PD-1/PD-L1抑制剂联合化疗比PD-1或PD-L1单药治疗或化疗单独治疗更有效,但仍然需要开发生物标志物来指导免疫化疗的治疗决策。PD-L1表达和肿瘤突变负荷(TMB)的预测价值主要针对PD-1和/或PD-L1单药治疗,而它们对联合化疗和免疫治疗的预测价值有限。基于组织样本的WES和基于血液的ctDNA检测之间的关系已被研究,特别是用于估计TMB。然而,目前还没有前瞻性样本收集和通过III期随机临床试验验证从ctDNA和基于组织的WES中得出的疗效预测生物标志物之间的一致性。CHOICE-01研究是一项III期随机双盲临床试验,评估了PD-1单抗特瑞普利单抗联合化疗在未经治疗的晚期NSCLC患者中的疗效和安全性。
方法
CHOICE-01研究是一项在中国59家医院进行的随机双盲III期临床试验,纳入了未经治疗的局部晚期或转移性NSCLC患者。患者以2:1的比例随机分配到特瑞普利单抗组或安慰剂组,并根据基线PD-L1表达状态、组织学类型(鳞状细胞癌vs.非鳞状细胞癌)和吸烟状态进行分层。鳞状细胞癌患者接受纳武利尤单抗、卡铂和特瑞普利单抗或安慰剂的治疗方案;非鳞状细胞癌患者接受培美曲塞、顺铂或卡铂和特瑞普利单抗或安慰剂的治疗方案。主要终点是由研究者评估的无进展生存期(PFS)。次要终点包括由独立评审委员会(BIRC)评估的PFS、总生存期(OS)、客观缓解率(ORR)和安全。探索性终点旨在评估特瑞普利单抗的免疫原性反应与其安全性和疗效之间的关系,并通过生物标志物分析(包括但不限于PBMCs、PD-L1、WES等)识别具有最佳疗效预测的亚群。
研究结果
主要终点:特瑞普利单抗组的中位OS为23.8个月,安慰剂组为17.0个月(HR=0.69,95%CI:0.57-0.93,名义P=0.01)。特瑞普利单抗组的1年、2年和3年OS率分别为74.0%、49.8%和32.5%,安慰剂组分别为72.8%、37.5%和18.4%。
亚组分析:非鳞状细胞癌亚组中,特瑞普利单抗组的中位OS为27.8个月,安慰剂组为15.9个月(HR=0.49,95%CI:0.35-0.69,P<0.001)。鳞状细胞癌亚组中,特瑞普利单抗组的中位OS为19.6个月,安慰剂组为18.1个月(HR=1.09,95%CI:0.77-1.56,P=0.65)。PD-L1表达≥50%亚组中,特瑞普利单抗组的中位OS为30.0个月,安慰剂组为28.4个月(HR=0.91,95%CI:0.491-1.797,P=0.7791)。
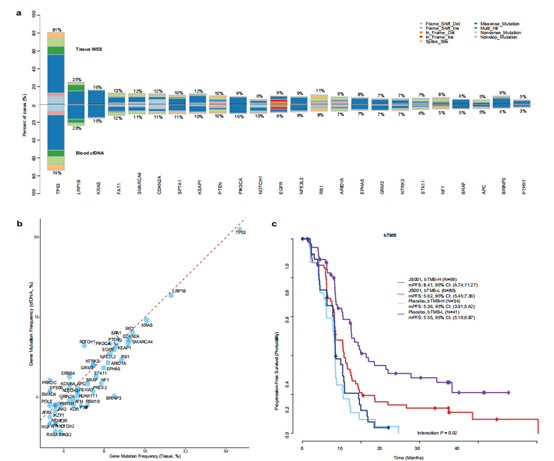
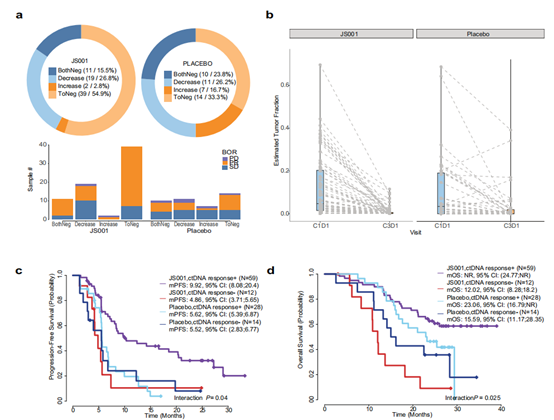
生物标志物分析:组织WES和ctDNA测序结果显示,特瑞普利单抗组的FA-PI3K-Akt和IL-7信号通路突变与OS改善相关。基线ctDNA阴性与PFS和OS改善相关,但并不能预测特瑞普利单抗治疗的反应。基线bTMB与特瑞普利单抗组的PFS改善相关。第3周期第1天ctDNA反应与特瑞普利单抗组患者的PFS和OS改善相关。

安全性
两组的3级及以上不良事件(AEs)发生率相似(78.9% vs. 82.1%),严重不良事件(SAEs)发生率也相似(46.4% vs. 35.3%)。特瑞普利单抗组的AE导致治疗中断的发生率更高(15.3% vs. 3.2%),研究者评估的免疫相关不良事件(irAEs)发生率也更高(50.6% vs. 21.2%)和3级及以上irAEs发生率更高(16.9% vs. 3.2%)。
结论
特瑞普利单抗联合化疗作为晚期NSCLC的一线治疗方案,显著改善了OS,尤其是在非鳞状NSCLC亚组中。基于ctDNA和组织WES的分析结果表明,高TMB、FA-PI3K-Akt和IL-7信号通路突变的患者更能从特瑞普利单抗治疗中获益。此外,第3周期第1天观察到的ctDNA反应与联合治疗患者的临床结果改善相关。
原始出处
Zhong, J., Fei, K., Wu, L. et al. Toripalimab plus chemotherapy for first line treatment of advanced non-small cell lung cancer (CHOICE-01): final OS and biomarker exploration of a randomized, double-blind, phase 3 trial. Sig Transduct Target Ther 9, 369 (2024).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#NSCLC# #特瑞普利单抗#
0