LANCET ONCOL:胃癌术后辅助化疗敏感患者的鉴别
2018-03-23 慧语 肿瘤资讯
对于II、III期可进行手术的胃癌患者,术后进行辅助化疗能够延长患者的生存时间。但这种生存获益总的看来不是很明显,提示我们可能并非所有的患者都适合这种治疗方案。最新发表在Lancent Oncology一项研究,研发了一种能够区分II、III期可进行手术的胃癌患者术后化疗敏感性的判别方法,并通过测试队列进行了确认,小编带您一探究竟。
对于II、III期可进行手术的胃癌患者,术后进行辅助化疗能够延长患者的生存时间。但这种生存获益总的看来不是很明显,提示我们可能并非所有的患者都适合这种治疗方案。最新发表在Lancent Oncology一项研究,研发了一种能够区分II、III期可进行手术的胃癌患者术后化疗敏感性的判别方法,并通过测试队列进行了确认,小编带您一探究竟。
背景:
基于两项III期临床试验(ACTS-GC和CLASSIC),NCCN指南将术后进行辅助化疗作为II、III期可进行手术的胃癌患者的标准治疗方案。但目前尚无研究对术后化疗敏感患者的预测指标进行独立的验证。本研究是第一项揭示出某种预测方法与胃癌根治术后患者的化疗敏感性之间存在显着联系的研究,并且在另外一个独立的测试队列中进行了验证。
方法:
在这项多队列回顾性研究中,采用了一种多阶段的策略来开发基于基因检测的个体患者预后分类器(危险因素)和预测分类器(是否对术后辅助化疗敏感)。具体步骤如下:
① 探索性分析阶段:探索性的生物信息学分析的目的是在胃癌转录组数据库中确认出生物学功能相关候选基因。选取5个队列共计1259个患者样品的转录组数据(4个来自于GEO数据库,一个来自于内部数据库)进行分析。选取这5个数据库的原因是样本量大、数据质量好、能够获得基于基因表达的分子类别和患者的临床数据;但由于这些数据均来自于2010年之前的患者,彼时还未有标准的治疗方案,完全由主治医师自由定夺,因此不易得到这5个队列中患者的治疗信息。
② 发现分析阶段:2005年1月1日至2010年12月31日在韩国延世癌症中心接受治疗的310名II、III期可进行手术的胃癌患者的肿瘤组织(经福尔马林固定石蜡包埋,FFPE处理)进行分析,包括193个术后加化疗患者的样品和117个单纯手术治疗患者的样品。在本阶段,研发了一种实时的RT-PCR检测试剂,能够在众多基因中筛选出与胃癌相关的生物学功能相关候选基因。
③ 评价分析阶段:第二阶段的310份样品中3份由于质量问题被排除,最终纳入307份经FFPE处理的样品进入第三阶段,包括II-III期经胃癌D2根治术患者(单独手术)114例,以及合并术后辅助氟尿嘧啶为基础化疗的患者193例。本阶段患者的样品采用上一阶段筛选出的特征基因进行了分层,并进行了预测和预后因素的分析,主要是根据每个患者的分类基因状态与其5年OS之间的关联性进行判断。
外部验证分析阶段:验证集中625名患者的样品来自于另一项III期临床试验,即CLASSIC试验(NCT00411229),包括胃癌D2根治术联合卡培他滨和奥沙利铂化疗患者323名,以及单独手术的302名患者。在本阶段进行实时RT-PCR实验室检测的人员不允许接触到该患者的临床数据,只允许两名独立的统计分析人员进行验证分析时才可以接触到临床数据。整个研究的流程图见图1。主要终点指标为5年OS。
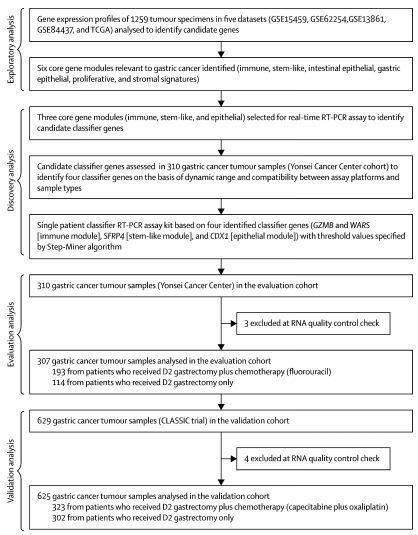
图1. 整个研究的流程图,分探索性分析、发现分析、评价分析、验证分析4个阶段完成
结果:
① 在探索分析阶段,开发了一种实时RT-PCR探针,能够检测3种基因模块的239个基因。对此239个基因进行平台与样本类型的兼容性的综合评价后筛选出12个候选基因。
② 在发现分析阶段,对这12个基因的动态表达范围及其在310个FFPE样品中的异质性进行了分析,最终确定了4个分类基因,即代表免疫功能模块的GZMB和WARS基因;代表干细胞类型模块的SFRP4基因;以及代表肠上皮模块的CDX1基因。此外,还有5个基因(ACTB, ATP5E, HPRT1, GPX1,UBB)被确定下来用于内部标准化的定量PCR分析。采用这9个基因制成的实时RT-PCR探针检测试剂盒,达到GMP标准,能够用于对个体患者进行分类判别。
③ 在评价分析阶段中,310个样品有3例由于质量问题被剔除,因此采用Step-Miner确定4个基因的分割点时使用了307个FFPE样品,最终确定GZMB, WARS, SFRP4, CDX1四个基因表达水平的分割点分别为-5.18,-2.14,-3.63,-2.69。由此,可以将患者分成各种类型的亚组(图2)。
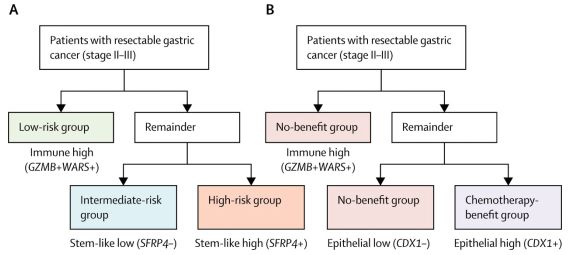
图2 根据4种基因的界值将患者分为不同亚组
④ 在验证评价分析中,625例患者包括323名手术加化疗以及302名单纯手术患者(图3A),中位随访时间为61月(IQR 43-74)。基于GZMB, WARS, SFRP4三个基因建立的患者预后分类器将625名患者中的79人(13%)鉴别为低危组,296人(47%)鉴别为中危组,其余250人(40%)鉴别为高危组。低、中、高危组患者的5年OS分别为83·2% (95% CI 75·2–92·0), 74·8% (69·9–80·1), 66·0% (60·1–72·4), P=0·012(图3B)。
基于GZMB, WARS, CDX1三个基因建立的患者预测分类器将625名患者中的344人(55%)鉴定为化疗获益组,其余为非获益组。化疗获益组中,接受过术后辅助化疗的患者5年OS显着高于单纯手术的患者[ 80%(95% CI: 73.5-87.1)vs. 64.5(56.8-73.3),HR=0.47(0.3-0.75),P=0.0015](图3C)。但在非获益组中则没有这种差异(P=0.71)。在内部测试队列中也得到相似的结果(图3D)。
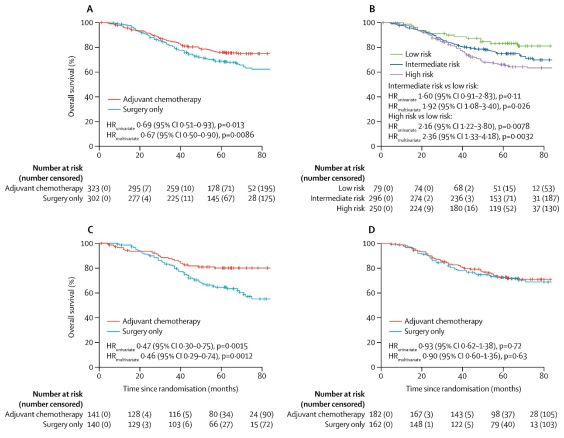
图3 验证数据集中各亚组OS的比较(A)术后辅助化疗 vs 单纯手术 (B)低、中、高危患者预后比较 (C)辅助化疗敏感组患者术后辅助化疗 vs 单纯手术 (D)辅助化疗不敏感组患者术后辅助化疗 vs 单纯手术
结论:
针对II、III期可进行手术的胃癌患者,在控制TNM分期及传统的危险因素之后,本研究开研发的化疗敏感分类器能够将患者的预后状况进行良好的区分;并且还能够将术后化疗敏感的患者鉴别出来。因此,基于GZMB, WARS, SFRP4和CDX1基因建立的患者预后分类器能够作为传统TNM分期的有效补充,为确定术后适合进行化疗的患者提供有效的决策信息。但在进一步推广前,还应进行一系列前瞻性的临床研究来进一步确认本文提出的分类器的有效性。
原始出处:
Prof Jae-Ho Cheong, MD, Prof Han-Kwang Yang, MD, Hyunki Kim, MD,et al.Predictive test for chemotherapy response in resectable gastric cancer: a multi-cohort, retrospective analysis. LANCET ONCOLOGY. Published: 19 March 2018.DOI: https://doi.org/10.1016/S1470-2045(18)30108-6
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#Lancet#
54
#胃癌术#
0
#化疗敏感#
135
#Oncol#
67
学习了谢谢分享!!
103
学习了
95
好
80
很牛了.学习了
84
学习
101
学习一下谢谢
59