Nature:冯亮团队解析NCC蛋白结构及噻嗪类降压药的作用机制
2023-02-17 “小柯生命”公众号 “小柯生命”公众号 发表于陕西省
研究解析了人源钠氯协同转运蛋白NCC及其与噻嗪类降压药(NCC抑制剂)的复合物的电镜结构,揭示了NCC转运底物过程中的构象变化,阐明了噻嗪类降压药抑制NCC转运功能的分子机制。
高血压是很常见的慢性病,大约影响全球三分之一的成人,高血压使得罹患心脑血管疾病(如心肌梗死、中风等)和肾脏疾病等的风险大大增加。肾脏可通过控制水钠的排出量来调节血压,而位于肾脏远曲小管的NCC则在这个调节过程中起着关键作用,它可以通过重吸收钠和氯来精细调控离子和酸碱平衡。
NCC功能障碍可导致Gitelman综合症,其特征是低血压;而假性低醛固酮症II型则与NCC 活性过高有关,其特征是高血压。因此,NCC是药物治疗肾脏和心血管疾病的重要靶标,历史上第一款疗效和安全性都较好的口服降压药——噻嗪类利尿剂(目前仍是治疗高血压的一线药物)就是通过抑制NCC功能来实现降压的,但其背后具体的分子机制仍不清楚。
2023年2月15日,美国斯坦福大学医学院冯亮团队在 Nature 期刊发表了题为:Structure and thiazide inhibition mechanism of the human Na-Cl cotransporter 的研究论文。
该研究解析了人源钠氯协同转运蛋白NCC及其与噻嗪类降压药(NCC抑制剂)的复合物的电镜结构,揭示了NCC转运底物过程中的构象变化,阐明了噻嗪类降压药抑制NCC转运功能的分子机制。该结果为理解NCC的钠氯协同转运机制提供了重要的见解,并为未来设计靶向NCC的降压药奠定了坚实的基础。

这是继三年前冯亮实验室联合廖茂富实验室合作在 Nature 期刊发表了钠-钾-氯协同转运蛋白NKCC1的结构后,在阳离子-氯离子协同转运蛋白研究领域取得的又一次突破性进展。

在这项最新的研究中,经过大量的体外表达尝试,研究团队获得了两个能够提高人源NCC表达量和生化表现的构建。随后研究人员利用冷冻电镜解析了3.0 ?分辨率的处于内向型构象的NCC结构,以及2.8 ?分辨率的结合降压药聚噻嗪(polythiazide)的 NCC处于外向型构象的结构。
研究人员的NCC结构分析和功能实验暗示腺嘌呤核苷酸结合对NCC的功能起着重要的作用,并且N端结构域和C端结构域的相互作用对于其功能有重要影响。
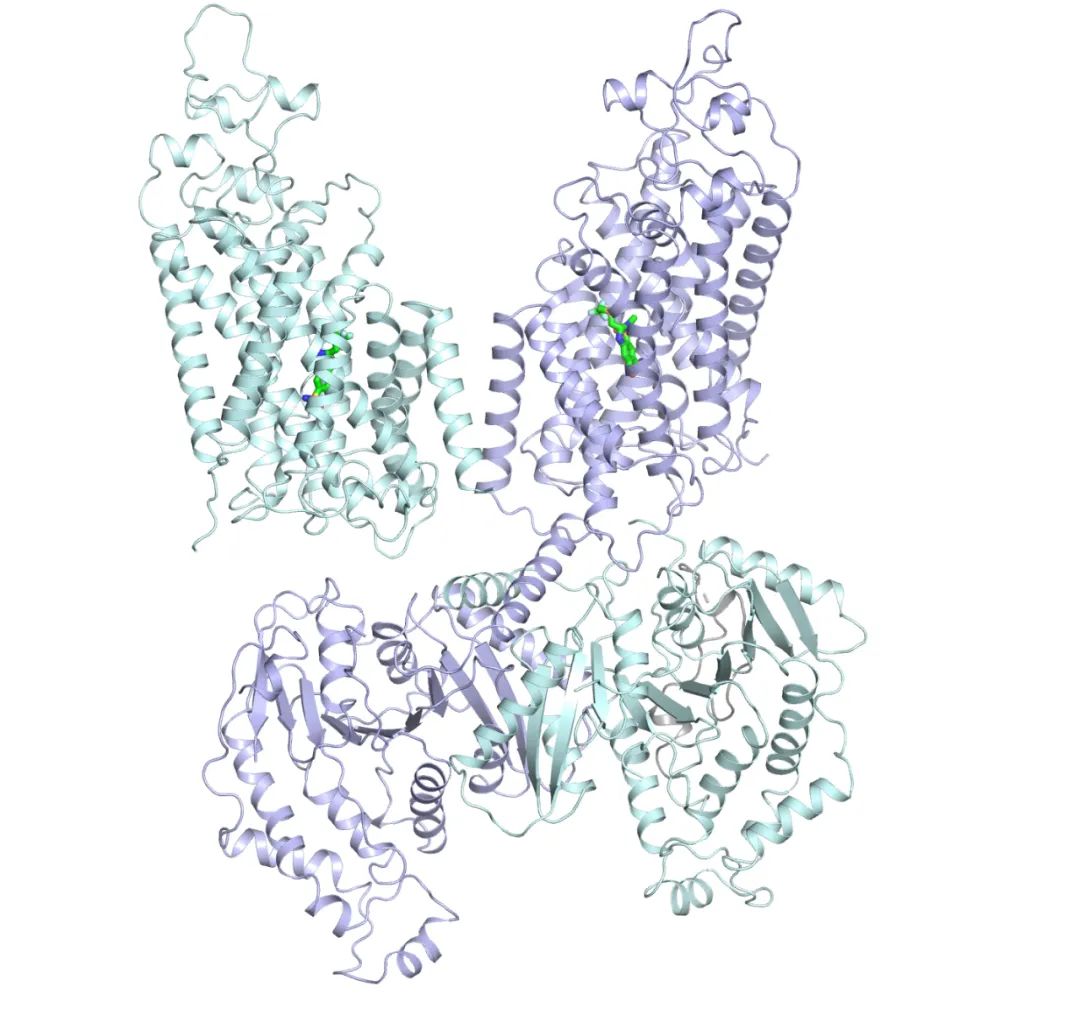
在NCC结构中,研究团队发现聚噻嗪结合在处于外向型构象的NCC的底物转运途径内。通过比较外向型和内向型构象的NCC结构,研究人员发现这两种状态之间的转变涉及NCC的胞外和胞内侧的协同构象变化。他们发现聚噻嗪可阻碍NCC从外向型构象转变为内向型构象,从而抑制其转运过程。此外,由于聚噻嗪与氯结合位点具有重叠性,聚噻嗪也会直接阻断氯结合。总之,聚噻嗪通过与底物结合竞争和阻碍构象状态转换来抑制NCC功能。
60多年来,噻嗪类利尿剂以肾脏钠氯协同转运蛋白NCC为靶点,一直是治疗高血压的重要方式之一。这项研究阐释了噻嗪类利尿剂的作用机理。该发现对于进一步优化提高当前噻嗪类降压药的特异性以及药效具有重要的指导意义。此外,NCC结构及其转运机制的阐明也为设计靶向NCC的下一代药物治疗方法奠定了基础。
范敏锐、张建秀、Chien-Ling Lee和张金儒为论文共同第一作者,冯亮为论文通讯作者。
原始出处:
Chew, T.A., Orlando, B.J., Zhang, J. et al. Structure and mechanism of the cation–chloride cotransporter NKCC1. Nature 572, 488–492 (2019). https://doi.org/10.1038/s41586-019-1438-2.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







