临床研究革新势在必行:以数字化转型加速药物开发创新
2019-05-25 生物谷 生物谷
药物开发创新是一个周期长、高投资、高风险的过程,药物开发通常需要10年到15年的时间,投入资金会达到5到10亿美元。这个过程对于药企来说都是一个巨大的挑战,同时也是沉重的负担。各个药企现在正在积极地探索利用新的创新手段,提高临床试验、临床开发的效率,以及提高新产品上市的概率,这是所有制药企业所面临的共同的挑战。作为全球领先的生物制药服务创新企业,精鼎医药致力于在中国和全球推动实施创新,其旗下的
药物开发创新是一个周期长、高投资、高风险的过程,药物开发通常需要10年到15年的时间,投入资金会达到5到10亿美元。这个过程对于药企来说都是一个巨大的挑战,同时也是沉重的负担。各个药企现在正在积极地探索利用新的创新手段,提高临床试验、临床开发的效率,以及提高新产品上市的概率,这是所有制药企业所面临的共同的挑战。
作为全球领先的生物制药服务创新企业,精鼎医药致力于在中国和全球推动实施创新,其旗下的多个项目,专注于解决全球药物开发面临的挑战,促进生命科学生态系统的发展,从而为患者提供更快更高效的治疗。日前,精鼎医药在北京举办圆桌会议,聚焦“数字化转型推动药物开发创新”进行深入探讨。
中国医疗健康数字化转型和革新
药物研发一直是创新发展的基石。随着近几年新药研发政策的不断放开,整个临床试验的开发进入到一个全面繁荣的阶段,特别是中国本土企业的创新,据数据显示,2018年本土创新药临床试验的的批件达到653个,比2017年增长了17%,再加之资本的涌入,整个中国市场的临床研究创新研发将势在必行。在数字化时代,数字化医疗健康科技无疑帮助建立了一个丰富的互联合作生态系统,改变了患者、医护人员和创新者之间的互动方式,以患者为中心的未来已经开始显现。
来自精鼎医药亚太区研发战略咨询技术副总裁程龙先生表示,“随着大数据和人工智能的发展和医疗政策的逐步开放,借助人工智能、互联网、物联网等技术发展,将打破传统医疗服务在空间和时间上的局限性。数字医疗的发展必将带来医疗健康服务模式的重大变化。在移动医疗方面,目前已广泛开展移动查房、移动护理、远程诊疗、移动挂号、移动支付、报告查阅、满意度反馈的O2O全流程闭环移动化服务等以各种移动健康管理APP。当然,数字医学设备创新开发与应用不断涌现,包括手术机器人,高清电子内窥镜,智能输液设备和呼吸睡眠监测仪等。因此,在数字医疗背景下,健康服务模式已经开始改变。”
在谈到未来行业机遇时,程龙先生提到,信息化转型使价值付费成为可能,现在的按人头付费和按病种付费等其实都是价值付费的一种体现,这种情况下,价值付费的要求对于药物的临床价值提出更高要求,也就是说我们的药物临床试验要能够做出来好的药物,满足未满足的临床需求,这样它的创新性才能真正体现出来。另外,创新药物研发需要考虑转型后疾病管理的需求,新药临床试验患者招募出现变化,传统临床试验随访模式出现挑战。同时,临床试验设计不断创新 ,临床试验有效性指标也不断改变,临床试验指标有了更多选择,包括可穿戴设备等一些新的指标出现。真实世界数据更加可靠,制药行业也会得到更好的信息化支撑。
应用创新型适应性试验设计,加速药物研发效率
创新试验设计对于提升药物上市概率和临床试验效率具有很大的积极影响,并且正在逐渐地被监管机构所接受,尤其是在全球第二大制药市场中国,推动创新的力度和速度都在加大。
精鼎医药生物统计公司副总裁Martin Roessner先生认为,“通过数字化手段去推进医疗机械和药物开发创新中的重中之重。我们曾做过一个研究,主要探讨不同的创新试验设计对临床试验带来的影响,包括适应性试验设计;精准医疗试验;以患者为中心的试验以及真实世界试验。 研究显示,创新实验设计大大降低了受试者招募的时间,也很大程度上提升了药物上市的可能性。”
同时,Martin Roessner先生强调,“适应性试验为提高临床试验效率提供了一个有吸引力的机会,但并不是唯一的机会。但无容置疑我们看到,适应性临床试验可极大地提高试验效率,减少所需要的费用,减少患者入组的时间,以及所需的患者数量,极大地提高我们药物成功开发的可能性。同时,从伦理道德角度来看,让患者在一个可能对他并没有好处的疗效对照组来讲,适应性试验可能更有利于患者的利益。”
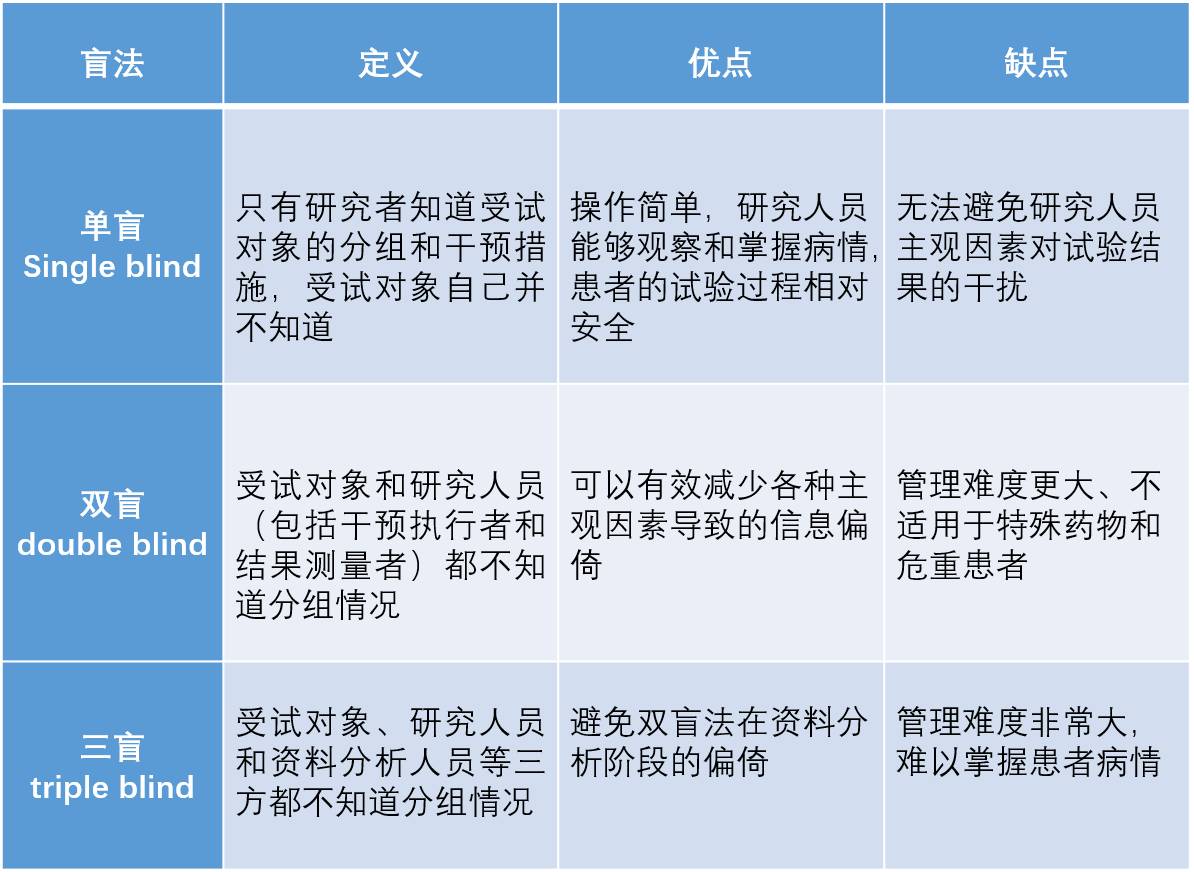
临床试验影像学标准指南更新,人工智能或将取代独立盲法评价
人工智能是计算机系统的理论和发展,能够执行通常需要人脑智能的任务,如视觉感应、语音识别、决策和翻译。 人工智能在临床的应用中已全棉落地开花,更多就是我们看到它在诊断方面应用的很多。比如乳腺癌的诊断,肺结核和肺炎的诊断,以及在诊断骨质疏松方面的应用,同样,人工智能在临床开发整个过程中展现出了无限的潜能。
“2018年美国FDA最新出版的临床试验影像学标准指南,涉及话题包括医疗实践标准 VS 临床试验的执行标准,在试验中的影像监测和章程修改及数据传输、存档和影像分析的注意事项等,同时,指南推荐了独立盲法中心评价,尤其是开放标签的临床试验。“精鼎医药临床信息技术副总裁Peter Steiger先生介绍到,在开放标签的临床试验中,因为临床特征与结果的预期关系是已知的,所以临床信息的可及性可能会影响基于站点的影像解译,因此基于站点的影像解读可能会引起对潜在偏差的担忧。 与多中心实验中基于站点的影像解读相比,我们认为集中的影像解读过程能够提供更多可验证的、统一的读片者培训以及读片者表现的持续管理,以确保影像的质量,减少影像解读中的易变性,从而能够更精确地估计治疗效果。我们相信FDA做这样的推荐,并不是不相信研究员的能力,只是想对影像最后结果解读方面的质量标准进行控制,从而进一步提高我们临床试验结果的可靠性。”
人工智能在临床试验中医学影像上的应用中机遇与挑战并存。Peter Steiger先生提到,人工智能擅长量化,能够搜索到人类无法察觉的特征,一经开发和验证,人工智能方法是快速、高效和可重复的。然而在一些为人为观察优化的评价标准,例如实体瘤的疗效评价标准(RECIST)并不适用于人工智能,需要监管和科学验证。
最后,Peter Steiger先生表示,“着眼于中国对高水平临床研究资源的巨大需求,精鼎医药一直致力于培养具有国际水准的本土临床研发人才,推动中国药物临床研发的全球化创新,并把全球的最佳实践介绍到中国市场。同时,我们也会聚焦在全球层面去看待客户的需求,在药品上市、获批、进入医保等环节为生物制药公司提供帮助。”
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#创新#
42
#数字化#
56
#药物开发#
66