10月10日全球新冠肺炎(COVID-19)疫情简报,确诊超3709万,美国疫情强烈反弹,全球聚焦疫苗研发进度
2020-10-10 MedSci原创 MedSci原创
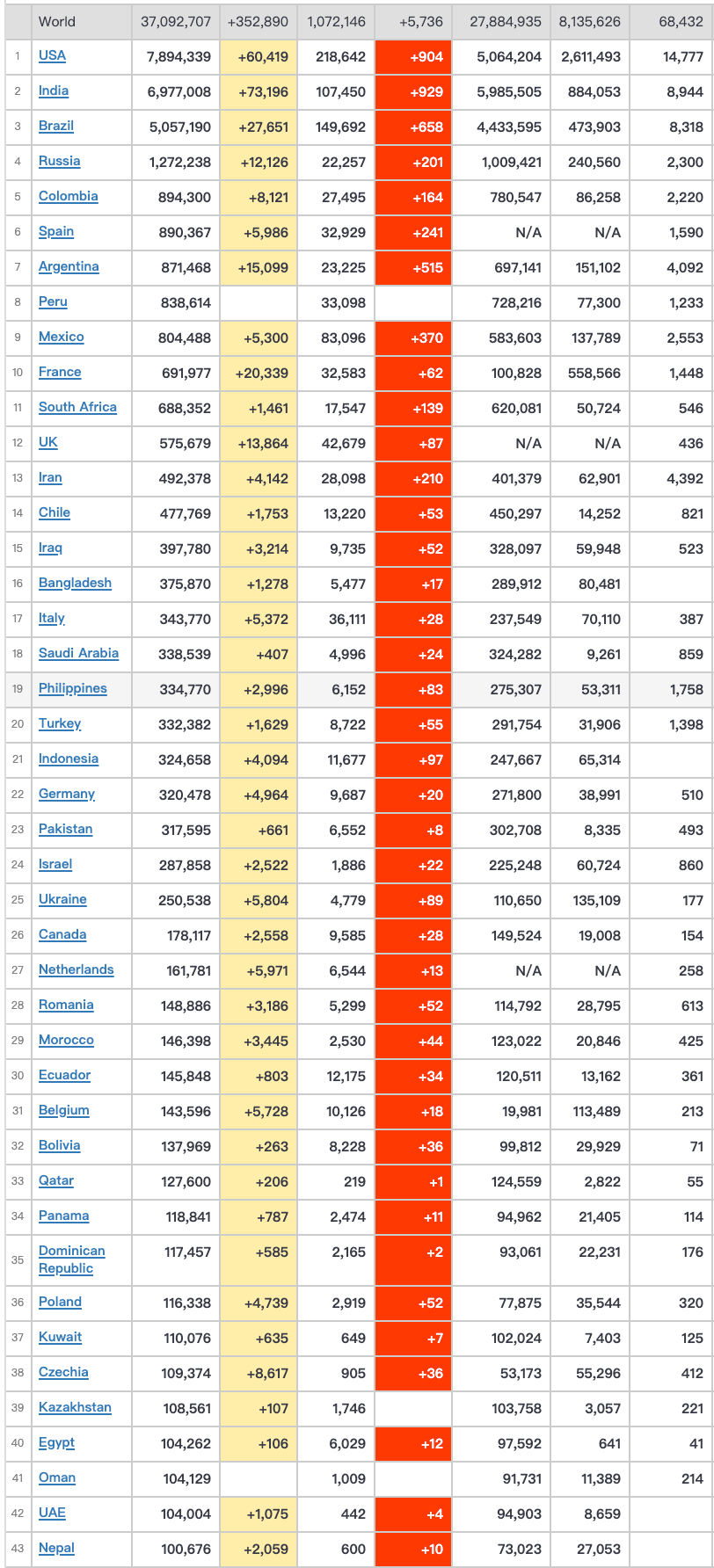
据Worldometers实时统计数据显示,截至北京时间10月10日09时20分,全球新冠肺炎(COVID-19)确诊病例达3709万例,新增352,890例至37,092,707例,死亡病例达107
据Worldometers实时统计数据显示,截至北京时间10月10日09时20分,全球新冠肺炎(COVID-19)确诊病例达3709万例,新增352,890例至37,092,707例,死亡病例达107万例,新增5,736例至1,072,146例,康复27,884,935例,活动 病例为8,135,626例,其中重症增长至68,432例。全球确诊病例超过10万例的国家增至43个。此外,瑞典和危地马拉的确诊病例已经超过9万。昨日报道:10月9日全球新冠肺炎(COVID-19)疫情简报,确诊超3673万,全球单日新再创新高,瑞典群体免疫能阻止第二波疫情吗?
一次染病后不会产生终身免疫
当地时间9日,世界卫生组织宣布,该机构当日收到了超过35万例新增确诊病例的报告,较本周初高出近1.2万例,欧洲疫情反弹严重,全球单日新增新冠病例数创下新高。
在9日举行的新闻发布会上,世卫组织紧急项目负责人迈克尔·瑞安表示,“世界上大多数人仍然容易感染这种疾病。”他说,各国不仅应将重点放在限制性措施上,还应着重于加强其监视系统、测试、接触者追踪以及确保民众参与防疫等方面的能力。
此外,世卫组织紧急项目技术主管科霍夫表示,许多研究显示,无论病情严重程度如何,人体感染新冠病毒后都会产生免疫反应,甚至无症状感染者也会产生免疫反应,但尚不清楚其强度和延续时间如何。而根据其他研究,一次感染不会产生终身免疫,所以抗体可能会逐渐衰退。
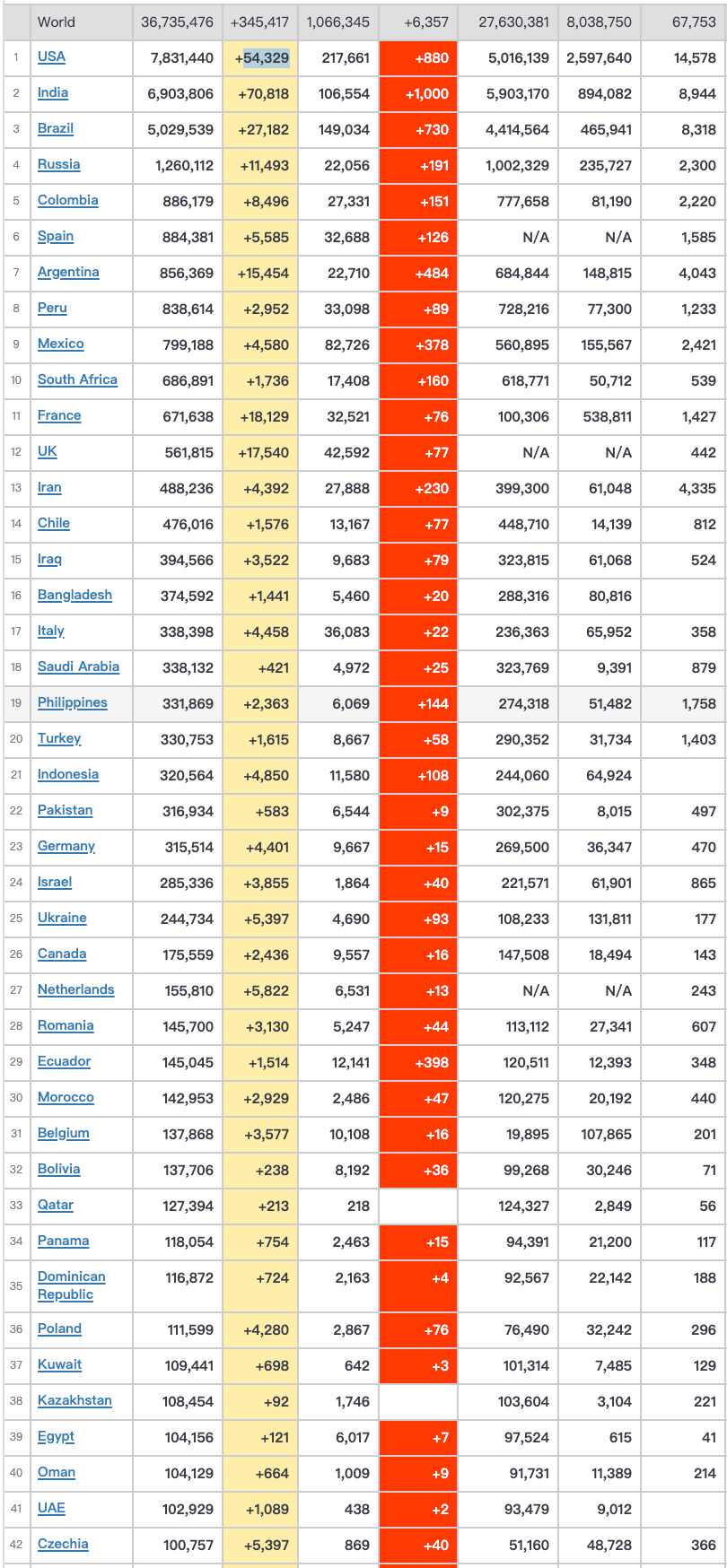
美国确诊人数快速反弹

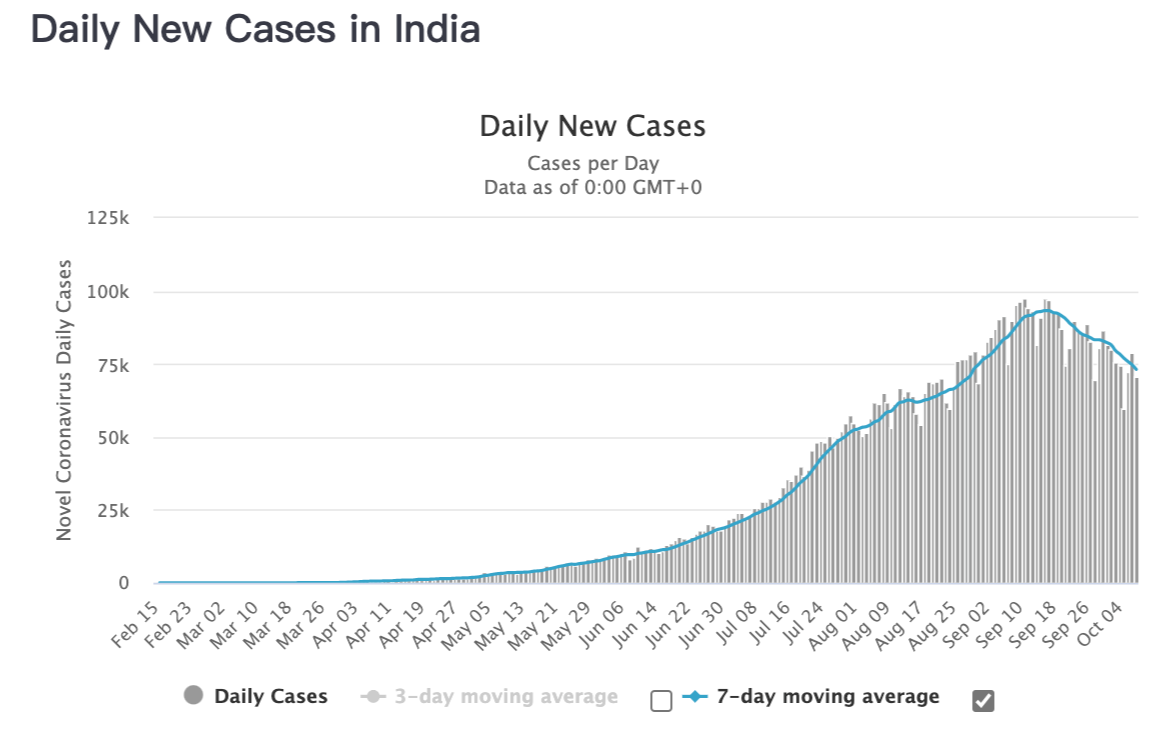
印度情况趋于好转
全球疫苗进度备受关注,最快年底前有望上市
在新冠肺炎疫情影响下,全球疫苗开发速度之快前所未有。当前,总共9款新冠疫苗正在开展Ⅲ期临床试验。新冠疫苗的上市时间一直是公众最关心的话题。来自世卫组织总干事10月6日的说法是,年底前可能会有新冠疫苗出炉。
事实上,全球第一款新冠疫苗已经被注册。8月11日,俄罗斯卫生部注册了由“加马列亚”流行病与微生物学国家研究中心研制的“卫星V”新冠疫苗。当地时间10月6日,俄罗斯总统普京表示,俄罗斯国防部领导层几乎已全部接种新冠疫苗。据报道,该款疫苗有望于11月向国外市场提供,乌克兰及白罗斯已向俄方寻求引进疫苗,巴西、埃及、印度等约40国也有意购买。不过,俄罗斯的这款新冠疫苗也尚未完成Ⅲ期临床试验,其约4万人参与的Ⅲ期临床试验预计将于12月31日完成。
欧美的新冠疫苗获授权使用的时间预计也不会早于11月。近日,美国食品药品监督管理局(FDA)发布文件称,疫苗制造商在寻求紧急使用授权许可之前,应跟踪试验参与者至少两个月,以排除任何潜在的安全问题。这一要求将导致在11月美国大选前几乎不可能推出疫苗。目前,欧美新冠疫苗研发进度最快的公司有辉瑞、Moderna和阿斯利康,它们都已经处于Ⅲ期临床试验过程中。根据摩根士丹利的预测,这三家公司的Ⅲ期临床试验结果有可能都在11月出炉,提交紧急授权使用的申请预计会在11月底。
在9款正在开展Ⅲ期临床试验的新冠疫苗中,有4款来自中国,包括3款灭活疫苗和1款腺病毒载体疫苗。在上月底国新办举行的吹风会上,据相关负责人介绍,4款进入Ⅲ期临床试验的疫苗目前进展顺利;Ⅲ期临床试验进展的快慢受很多因素影响,例如受试者人数、受试者组数以及结果等。研究人员将采取特事特办的原则,推动我国新冠疫苗尽快上市。
在进入Ⅲ期人体临床试验的新冠灭活疫苗中,国药集团中国生物技术股份有限公司(简称国药中生)的进展较快。8月份,该疫苗的招募人数扩大到了4.5万人。在9月24日的第十三届中国生物产业大会签约活动上,国药中生董事长杨晓明说,新冠灭活疫苗目前试验进展好于预期,快于预期,离最后成功还差一公里,2020年年底有望上市。
中国多条技术路线同时推进
在疫苗研发上,我国并行推进灭活疫苗、腺病毒载体疫苗、重组蛋白疫苗、核酸疫苗、减毒流感疫苗5条技术路线研发,目前5条技术路线均已推进到临床试验阶段。值得期待的是,在10月份,中国的多个新冠疫苗研发将取得积极进展。
最大的进展是,智飞生物的重组亚单位新冠疫苗或将在10月份启动Ⅲ期临床,成为我国第5款进入Ⅲ期临床新冠疫苗。该疫苗于7月10日进入Ⅱ期临床,Ⅱ期临床将在10月份结束。
三叶草生物的新冠疫苗也同属重组蛋白路线,与智飞生物不同的是,智飞生物与中科院微生物所合作的新冠疫苗以S蛋白的受体结合区独特二聚体作为抗原,而三叶草生物的新冠疫苗以S蛋白三聚体作为抗原。9月19日,在泰州举办的“中国创新疫苗论坛”上,三叶草生物表示,“S-三聚体”蛋白亚单位疫苗全球Ⅱ/Ⅲ临床试验计划于第四季度开启,公司于6月19日在澳大利亚完成了Ⅰ期临床试验首批志愿者的接种。
国际上新冠疫苗的开发策略以核酸疫苗技术为主,我国艾棣维欣和艾博生物布局的正是核酸新冠疫苗。在“中国创新疫苗论坛”上,艾棣维欣表示,其DNA新冠疫苗预计在10月初在美国启动Ⅱ/Ⅲ期临床试验,国内将同步启动Ⅱ期临床。艾棣维欣的DNA平台技术已经积累了大量的安全性数据,其基于DNA技术平台开发的新冠疫苗正在全球多地开展临床试验。康泰生物曾与艾棣维欣签署了新冠疫苗《战略合作协议书》,共同致力于研发新冠DNA疫苗。
6月,沃森生物和艾博生物合作的mRNA新冠疫苗进入了Ⅰ期临床。据了解,该mRNA新冠疫苗基于艾博生物开发的mRNA体外合成平台以及脂质纳米球制剂技术,其中mRNA及脂质纳米球均由艾博生物自主研发生产。对于疫苗产品而言,稳定性对于疫苗的运输和储存至关重要。目前,Moderna和BioNTech的mRNA疫苗运输温度分别是-20℃和-70℃,在大批量运输和储存中存在诸多不便,而沃森生物与艾博生物合作的mRNA新冠疫苗具备良好的热稳定性,运输温度为2~8℃。华泰证券预计沃森生物即将启动该疫苗的1b期临床试验,并公布1a期试验数据。
万泰生物与厦门大学、香港大学联合研发的鼻喷流感病毒载体新冠疫苗于9月1日启动Ⅰ期临床。该新冠疫苗是目前已获准开展临床试验的新冠疫苗中唯一采用鼻腔喷雾接种方式的疫苗,通过模拟呼吸道病毒天然感染途径激活局部免疫应答和全身性免疫应答而发挥保护作用。前期动物实验结果显示该疫苗具有良好的安全性和免疫原性。9月19日,在“中国创新疫苗论坛”上,厦门大学NIDVD副主任张军教授在介绍该疫苗的研究进展时称,目前已免疫了60多人,没有出现3级不良反应。按照入组人数推测,该疫苗Ⅰ期临床或已接近尾声,有望在10月进入Ⅱ期临床。
新冠疫苗需重点考虑肥胖人群,因为常规治疗对他们可能不太有效
2020年9月《Science》针对肥胖人群在新冠中的高发现象发表文章,题目为《Why COVID-19 is more deadly in people with obesity—even if they’re young》,中文译名为《为什么COVID-19在肥胖人群中更致命,即使是年轻患者》。

自疫情开始以来,数十项研究报告称,许多重症COVID-19患者都是肥胖患者。
最近几周,大量新的人口研究巩固了这一联系,并证明即使只是超重患者也有更高COVID-19患病的风险。
根据美国疾病控制与预防中心(Centers for Disease Control and Prevention)的定义,体重指数BMI(体重千克数除以身高米的平方)在25到29.9之间的人属于超重,体重指数在30或30以上的人属于肥胖。
8月26日发表在《Obesity Reviews》上的一篇研究中,一个国际团队收集了大量同行评议论文的数据,这些论文共涉及39.9万名患者。
这项研究发现,与体重正常的人相比,感染SARS-CoV-2的肥胖症患者住院的可能性高113%,住进ICU的可能性高74%,接受侵入性机械通气(IMV)治疗的可能性高66%,死亡的可能性高48%。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#疫苗研发#
75
共克时艰~
83
印度病例真多
126
#研发#
79
#反弹#
0
印度🇮🇳反超了#新冠肺炎#
143
新冠肺炎,疫情何时才能消失
83
学习
152